嘉峪检测网 2020-07-13 09:31
导读:医药研发每天最新资讯汇总
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
智飞生物新冠病毒疫苗启动Ⅱ期临床。7 月 10 日,智飞生物与中国科学院微生物研究所联合研发的重组新冠病毒疫苗启动Ⅱ期临床试验,对疫苗安全性和免疫原性进行评估。据悉,该疫苗采用重组DNA技术,以新冠病毒刺突糖蛋白(S 蛋白)的受体结合区(RBD)独特二聚体作为抗原,再辅以传统佐剂研制而成,为国内首个获批进入临床试验的重组亚单位新冠疫苗。目前该公司新冠疫苗的生产车间、质量保证体系建设等工作正在加快开展。
国内药讯
1.扬子江多索茶碱注射液通过一致性评价。7月10日,扬子江南京海陵药业宣布其4类仿制药多索茶碱注射液(10ml:0.1g,仁畅)获得国家药监局批准上市,成为继石四药之后该品种第2家通过一致性评价的产品。多索茶碱是甲基黄嘌呤的衍生物,是一种支气管扩张剂。多索茶碱注射液适用于支气管哮喘、慢性喘息性支气管炎及其他支气管痉挛引起的呼吸困难。
2.国产第三家阿卡波糖片即将获批。浙江海正药业新4类仿制药阿卡波糖片上市申请处于"在审批"状态,预计即将获批上市,成为该品种第三家通过一致性评价的产品。阿卡波糖是一种α-糖苷酶抑制剂,原研厂家为拜耳,1999年9月获批进口中国(商品名:拜唐苹),配合饮食控制用于治疗2型糖尿病。目前国内拥有阿卡波糖制剂批文的药企有原研拜耳、中美华东、绿叶制药以及北京福元医药4家。2019年阿卡波糖国内销售额达到75.68亿元。
3.捷思英达ERK1/2抑制剂Ⅰ期临床首例患者给药。7月10日,捷思英达在研ERK1/2激酶抑制剂JSI-1187美国Ⅰ期临床完成首例患者给药。该研究在携带MAPK突变的复发/难治性实体肿瘤患者中评估JSI-1187的安全性、耐受性、药代动力学、药理动力学和临床药效。这项研究包括3个部分:JSI-1187单药剂量爬坡阶段(用于实体肿瘤患者)、JSI-1187与BRAF抑制剂达拉非尼联用的剂量爬坡阶段以及对携带特定基因突变肿瘤患者的扩展研究阶段。全球范围内尚无ERK激酶抑制剂获批上市。
4.杨森第三代TKI肺癌靶向药在华申报临床。强生旗下杨森制药的lazertinib片在中国申报的临床试验申请获CDE受理。Lazertinib 是一款第三代酪氨酸激酶抑制剂(TKI),正在开发用于治疗携带EGFR基因突变的非小细胞肺癌(NSCLC)患者。在ASCO 2018年会上发表的Ⅰ/Ⅱ期临床结果表明,lazertinib能够在已经对EGFR-TKI产生抗性的NSCLC患者中达到61%的客观缓解率(ORR),同时在携带脑转移瘤的患者中达到55%的颅内ORR。
5.CEPI与三叶草生物扩大新冠疫苗合作。7月8日,CEPI(流行病防范创新联盟)宣布扩大与三叶草生物的合作,向三叶草生物“S-三聚体”疫苗项目追加投资,首笔预付款6,600万美元,用于推进临床前研究、人体Ⅰ期临床以及疫苗疗效全球临床试验的选址准备工作。同时,这项投资将用于提高三叶草生物的产能,使之快速具备年产数亿剂疫苗的生产能力。该新冠疫苗候选物基于三叶草生物独特的蛋白质三聚体化(Trimer-Tag©)专利技术平台而开发。
国际药讯
1.瑞德西韦澳大利亚获批上市。澳大利亚医疗用品管理局(TGA)临时批准吉利德的Veklury (瑞德西韦)上市,用于重症住院COVID-19成人和青少年患者。这是澳大利亚获批的首个COVID-19治疗药物。瑞德西韦目前已在美国、欧盟和日本获批上市,其仿制药已经在印度获批。瑞德西韦在发达国家的定价为每剂390美元,一个疗程(5天6剂)的治疗费用大约为3120美元。印度制药公司西普拉(Cipla)生产的瑞德西韦仿制药定价为每剂4000卢比(折合53美元)。
2.Lynparza一线维持治疗BRCA突变胰腺癌获欧盟批准。阿斯利康和默沙东联合开发的PARP抑制剂Lynparza(olaparib,奥拉帕利)获欧盟批准,用于携带生殖系BRCA突变(gBRCAm)的转移性胰腺癌患者的一线维持治疗,这些患者经过至少16周的一线化疗后病情没有进展。一项Ⅲ期临床POLO中,与安慰剂相比,Lynparza一线维持治疗将gBRCAm转移性胰腺癌患者的PFS提高近一倍(中位PFS:7.4个月vs3.8个月),将疾病进展或死亡风险显著降低47%。Lynparza是在Ⅲ期临床中一线维持治疗这类患者被证实对患者有益的唯一一个PARP抑制剂。
3.阿斯利康抗血小板疗法获FDA优先审评资格。FDA受理阿斯利康抗血小板疗法替格瑞洛(ticagrelor,Brilinta)的补充新药申请,并授予其优先审评资格,与阿司匹林联用,用于减少发生急性缺血性中风或短暂性脑缺血发作患者的后续中风。在一项Ⅲ期临床THALE中,与阿司匹林相比,替格瑞洛与阿司匹林联用显著降低导致中风和死亡的主要复合终点的风险。如果获批,该组合疗法将成为在这类高危患者中用于降低中风风险的首款FDA批准的双联抗血小板疗法。
4.Keytruda单药治疗经典霍奇金淋巴瘤获优先审评资格。默沙东宣布,FDA已受理其重磅PD-1抑制剂Keytruda递交的补充生物制品许可申请(sBLA),并授予其优先审评资格,作为单药疗法,治疗复发/难治经典霍奇金淋巴瘤成人患者。预计今年10月30日之前做出回复。在一项关键性Ⅲ期临床KEYNOTE-204中,与治疗这一患者群体的标准疗法相比,Keytruda显著改善了患者的无进展生存期。
5. 拜耳创新疗法达到Ⅲ期临床终点。拜耳在研非甾体选择性盐皮质激素受体拮抗剂finerenone在治疗患有2型糖尿病的慢性肾病(CKD)患者的Ⅲ期临床FIDELIO-DKD中达主要终点。与安慰剂相比,finerenone联合标准护理可推迟首次发生肾衰竭的时间,降低因肾病死亡的风险,并延缓肾小球滤过率的下降速度。同时,finerenone还降低关键次要终点的风险,关键次要终点是由首次发生心血管死亡、非致死性心肌梗死、非致死性中风或心力衰竭住院所需时间构成的复合终点。临床数据将在科学会议上公布。
6.NIH启动COVID-19疫苗、单抗研究网络。7月8日,美国国家卫生研究院(NIH)宣布启动临床试验网络(COVPN)用于开展预防COVID-19的Ⅲ期疫苗和单抗等疗法有效性研究。COVPN网络的疫苗部门将采用统一方案,允许开展交叉试验分析,计划在超过100个美国和国际试验场所开展试验。Moderna公司与美国国家过敏与传染病研究所(NIAID)共同开发的mRNA-1273疫苗,有望在COVPN网络开展的第一阶段Ⅲ期临床试验中开展测试,临床试验预计将于今年夏天启动。
医药热点
1.国家呼吸医学中心落定。7月9日,国家卫健委印发《关于设置国家呼吸医学中心的通知》,决定由在新冠肺炎疫情期间作出突出贡献的中日友好医院和广州医科大学附属第一医院作为主体医院,共同构成国家呼吸医学中心。这两家医院将负责医学中心的日常运行和管理,并投入一定的工作经费,确保医学中心按职责任务开展相关工作。医学中心将引领国内呼吸学科发展,共同提升我国呼吸系统疾病医疗服务水平,促进全国呼吸疾病医疗资源均衡化和均质化。
2.汛期严防急性血吸虫病。国家卫健委近日发出《关于加强2020年汛期血吸虫病防控工作的通知》,要求各地要进一步强化血吸虫病监测,加强发热病人疫水接触史询诊。如发现血吸虫病疫情,应当在24小时内进行网络直报。各级血防机构要加强病例主动搜索,及时对接触疫水人员和不明原因发热病人进行调查、诊断;对报告的疫情及时进行核实、调查和处理。各地要依法向社会公布有螺地带特别是易感环境,并设立警示标志。
3.特朗普首次公开佩戴口罩。当地时间11日下午美国总统特朗普在马里兰州一家军方医疗机构看望伤兵和一线医护人员时,戴上了口罩。美国媒体报道称,这是自打新冠肺炎疫情在美国暴发以来,特朗普首次公开佩戴口罩。根据美国约翰斯·霍普金斯大学的统计数据显示,截至美东时间10日16时30分,美国新冠肺炎确诊病例累计已超过316万,达到3163505例,死亡病例已超过13.3万,达到133847例。
股市资讯
【硕世生物】公司产品新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法)被列入世界卫生组织应急使用清单。
【四环生物】公司预计2020半年期实现扭亏为盈,盈利620万元同比增长166.14%。
【复星医药】公司向香港联合所有申请批准分拆Gland Pharma境外上市事项获联交所批准。
审评动向
1. CDE最新受理情况(07月12日)
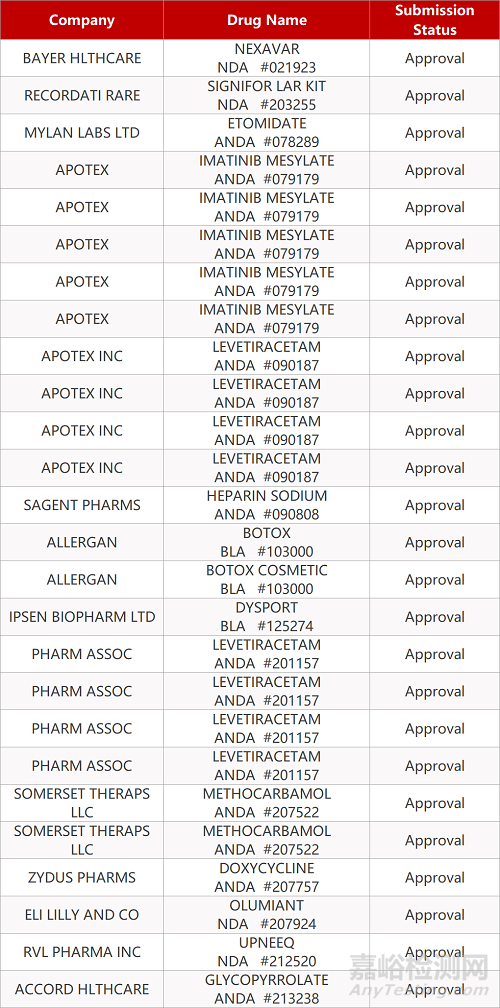
2. FDA最新获批情况(北美07月09日)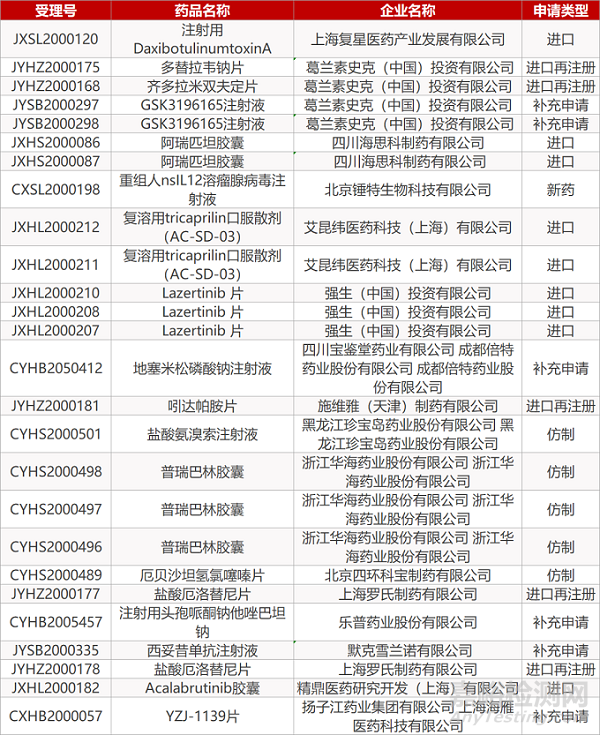
- The End -

来源:药研发