嘉峪检测网 2021-01-22 16:03
导读:更多医药技术资讯,请点击医药专栏: http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest 「 本文共:17条资讯,阅读时长约:3分钟 」 今日头条 默克/GSK终止TGF-/PD-L1双抗
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「 本文共:17条资讯,阅读时长约:3分钟 」
今日头条
默克/GSK终止TGF-β/PD-L1双抗Ⅲ期肺癌研究。默克(Merck KGaA)公布了TGF-β/PD-L1双功能免疫疗法bintrafusp alfa(M7824)肺癌Ⅲ期INTR@PID Lung 037研究的最新进展,并对INTR@PID项目进行了更新。INTR@PID Lung 037研究正在评估bintrafusp alfa与PD-1疗法Keytruda相比一线治疗PD-L1高表达的IV期非小细胞肺癌(NSCLC)患者的疗效,经独立数据监测委员会评估,该研究不太可能达到无进展生存期(PFS)共同主要终点。基于这一建议,默克决定停止INTR@PID Lung 037研究。
国内药讯
1.礼来VEGFR-2单抗申报中国上市。礼来VEGFR-2单抗ramucirumab的上市申请获CDE受理,推测申请的适应症为晚期胃癌的二线治疗。ramucirumab是全球唯一一个获批用于二线治疗晚期胃癌的靶向药物,上周刚刚公布了用于二线治疗晚期胃癌患者的亚洲Ⅲ期临床RAINBOW-Asia积极结果,ramucirumab联合紫杉醇显著延长了患者的中位无进展生存期(4.14个月vs3.15个月),并显示出与全球关键注册临床试验RAINBOW一致的中位总生存期(OS)获益(HR=0.963)。
2.正大天晴PD-1组合III期临床结果积极。正大天晴/康方生物PD-1「派安普利」联合安罗替尼一线治疗晚期肝癌(HCC)的最新临床数据在ASCO GI 2021会议上发布。截至2020年11月,派安普利联合低剂量安罗替尼一线治疗HCC 的客观缓解率为31.0%,疾病控制率为82.8%,中位无进展生存期(PFS)为8.8个月,6个月PFS率为63.2%,6个月OS率为93.2%。安全性方面,与两药物相关的3级及以上的不良事件发生率为19.4%,严重不良事件发生率为6.5%。
3.康方生物PD-1/CTLA-4双抗最新临床结果发布。康方生物“first-in-class” PD-1/CTLA-4双抗Cadonilimab(AK104)联合奥沙利铂及卡培他滨一线治疗晚期胃癌(GC)或胃食管结合部腺癌(GEJ)的Ib/II期临床最新结果在ASCO GI2021会议上发布。截至2020年11月,这一组合在可评估患者中的客观缓解率为64.1%,疾病控制率为87.2%。其中4mg/kg队列患者的中位随访时间为8.0个月,中位缓解持续时间未达到,6 个月无进展生存期率为76.5%。10mg/kg队列患者中有3 例达到部分缓解(75%)。与药物相关的3级及以上不良反应发生率为38.9%。
4.武田罕见病新药soticlestat拟纳入突破性疗法认定。武田和Ovid公司联合开发的“first-in-class”CH24H抑制剂soticlestat(TAK-935片)获CDE纳入拟突破性疗法认定公示名单,用于治疗Dravet综合征(癫痫发作伴抽搐性发作)和Lennox-Gastaut综合征(癫痫发作伴跌倒发作)。一项II期ELEKTRA研究结果显示,在12周的治疗维持期内,soticlestat治疗组患者抽搐发作(DS)和跌倒发作(LGS)频率中位数降低了27.8%,而安慰剂组患者DS和LGS频率中位数则增加了3.1%(p=0.0007)。
5.和铂医药巴托利单抗拟纳入突破性疗法认定。和铂医药巴托利单抗(HBM9161、HL161BKN)注射液获CDE拟纳入突破性疗法认定,针对适应症为用于全身型重症肌无力的治疗。HBM9161是由HanAll公司开发的一种全人源IgG单抗,和铂医药拥有其在大中华地区的权益。在一项IIa期临床中,与安慰剂组相比,HBM9161组患者重症肌无力日常生活 (MG-ADL) 量表平均改善3.8分 (p=0.029),重症肌无力复合 (MGC) 量表平均改善8.0分 (p=0.006),该新药总体安全性和耐受良好。
6.济民可信新冠中和抗体启动Ⅰ期临床。济民可信集团宣布其新冠病毒中和抗体JMB2002已在杭州树兰医院启动Ⅰ期临床。JMB2002是该集团采用Fc突变设计而开发的一款全人源特异性中和抗体,靶向病毒S蛋白的S1亚基上受体结合域(RBD)与ACE2结合界面的关键表位,已在临床前研究中显示出高效中和活病毒侵染非洲绿猴肾细胞。值得关注的是,JMB2002对不同突变病毒刺突糖蛋白均显示出良好的结合和阻断活性。
7.东阳光药两款创新药申报临床。1月20日,东阳光药两款创新药的临床试验申请获CDE受理,分别为1类新药HEC88473注射液及3.3类新药德谷胰岛素注射液。其中,德谷胰岛素注射液是一种新型长效胰岛素类似物,用于需要胰岛素治疗的糖尿病患者,2019年全球销售额超过15亿美元;2020年上半年在中国公立医疗机构终端销售额超过5000万,同比增长922.6%。目前国内市场仅有诺和诺德的原研产品(诺和达®)在售。
国际药讯
1.辉瑞/BioNTech新冠疫苗对变异病毒有效。辉瑞/BioNTech新冠疫苗BNT162b2在一项体外研究中显示出对新冠病毒突变株B.1.1.7有效。研究人员将B.1.1.7病毒株的完整刺突蛋白表达在VSV病毒表面,使用它来检测接种BNT162b2个体的血清的中和效力。结果显示,与表达不携带突变的刺突蛋白的假病毒相比,这些血清对表达B.1.1.7刺突蛋白的假病毒的中和能力没有生物学上的显著差别。BNT162b2的免疫血清仍具有针对携带B.1.1.7刺突蛋白的假病毒的中和能力。
2.阿斯利康Enhertu治疗晚期乳腺癌获欧盟批准。阿斯利康和第一三共联合开发的抗体药物偶联物Enhertu(trastuzumab deruxtecan)在欧盟(EU)获得有条件批准上市,用于单药治疗接受过两种或两种以上抗HER2方案的不能切除或转移性HER2阳性乳腺癌成年患者。在DESTINY-Breast01试验中,中位随访时间为20.5个月时,Enhertu显示出确认的ORR为61.4%,包括6.5%的完全缓解率和54.9%的部分缓解率;之前至少接受过两次治疗的HER2阳性转移性乳腺癌患者的估计中位DoR为20.8个月。
3.Sobi止血药Doptelet获欧盟扩大适用范围。欧盟委员会批准Swedish Orphan Biovitrum AB(Sobi™)公司扩大Doptelet(avatrombopag)的适应症范围,用于对其他治疗(如皮质类固醇、免疫球蛋白)无效的原发性慢性免疫性血小板减少症(ITP)成年患者的治疗。Doptelet是一种口服血小板生成素受体激动剂(TPO-RA),此前已获欧洲药物管理局(EMA)批准用于治疗计划接受手术的成人慢性肝病患者的严重血小板减少症进行侵入性手术。
4.百时美施贵宝PD-1两项补充生物制品许可申请获FDA优先审评资格。FDA受理百时美施贵宝PD-1抑制剂Opdivo(nivolumab)的补充生物制品许可申请(sBLA),联合含氟嘧啶和铂类化疗,用于治疗晚期或转移性胃癌、胃食管连接部癌(GEJC)或食管腺癌(EAC)患者。FDA同时授予其优先审评资格,预计5月25日前做出回复。如果获批,这将是一线治疗胃癌的首个基于免疫疗法的治疗选择。同时,Opdivo还获得FDA授予的另一项优先审评资格,用于作为辅助疗法,治疗接受新辅助疗法和切除手术之后的胃食管连接部癌和食管腺癌患者。
5.赛默飞世尔收购分子诊断公司Mesa Biotech。赛默飞世尔宣布以约4.5亿美元的现金和1亿的里程碑付款收购Mesa Biotech。Mesa Biotech是一家分子诊断公司,开发并销售了基于PCR的传染病快速即时检验平台,包括SARS-CoV-2(COVID-19)、A型和B型流感、呼吸道合胞病毒(RSV)和A群链球菌。此次收购,将扩展赛默飞世尔临床诊断领域业务规模,用于服务针对COVID的相关测试和开发其他传染病的即时检验。
医药热点
1.儿童新冠病例传播力更强。国际期刊柳叶刀子刊《lancet infectious disease》在线发表华中科技大学公共卫生学院团队关于新冠病毒家庭内传播的流行病学研究。该研究聚焦两万多个武汉新冠病毒家庭内的病毒传播特征等,发现在家庭内整体上婴幼儿和青少年对新冠病毒的易感性较老年人群弱,但其传播力更强。该研究建议应及时为符合条件的儿童进行新冠疫苗的接种。
2.辉瑞乳腺癌新药降价54%。1月18日,辉瑞宣布,其乳腺癌明星药爱博新(通用名哌柏西利)价格腰斩,每瓶售价从29799元跌至13667元,降价幅度达到54%。降价同时,辉瑞迅速对此前的患者援助项目做出调整,逐步停止此前针对低保和低收入患者的慈善赠药。据了解,该药降价前患者月治疗费用在3万元左右,如果有慈善赠药,月治疗费用在1.7万元左右。降价后,月治疗费用则进一步降至约1.3万元。
3.春节返乡须持7日内核酸检测阴性证明。《冬春季农村地区新冠肺炎疫情防控工作方案》日前公布。《方案》明确,返乡人员需持7天内有效新冠病毒核酸检测阴性结果返乡,返乡后实行14天居家健康监测,期间不聚集、不流动,每7天开展一次核酸检测。返乡人员是指从外地返回农村地区的人员:一是跨省份返乡人员;二是来自本省内中高风险区域所在地市的返乡人员;三是本省内的进口冷链食品从业人员、口岸直接接触进口货物从业人员、隔离场所工作人员、交通运输工具从业人员等重点人群。
4.2021年度马海德奖揭晓。马海德基金会日前公布了2021年度马海德奖项获奖名单。经马海德奖评选委员会对各地呈报的候选人线上评审,全国共有10名麻风防治工作者获得2021年度马海德奖,分别是:姚强(浙江)、李旺华(湖北)、段启志(广西)、许传勤(江西)、余海洪(安徽)、朱云霞(江苏)、胡宗厚(山东)、符方军(海南)、吴绍斌(湖南)、邓娟(贵州)。马海德基金会对获奖者进行了表彰和奖励。
股市资讯
【仙琚制药】公司的米索前列醇片通过一致性评价。
【安科生物】全资子公司安科恒益的阿莫西林颗粒收到生产注册补充申请《受理通知书》。
【生物股份】预计2020年实现归母净利润4.00-4.35亿元,同比增长80.96%-96.80%;扣非归母净利润3.85-4.20亿元,同比增长78.97%-95.24%。
审评动向
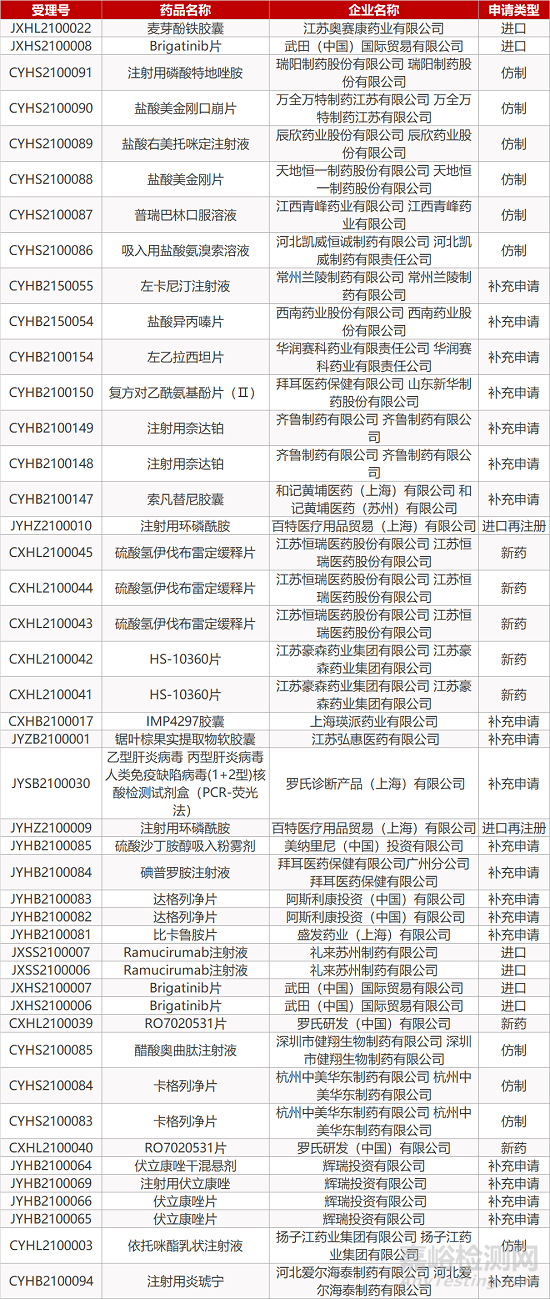
暂无
- The End -

来源:药研发