嘉峪检测网 2021-07-19 10:43
导读:医药研发每天最新资讯汇总
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
璎黎KRAS抑制剂在美获批临床。璎黎药业KRAS G12C抑制剂新药YL-15293获FDA临床试验许可,这是继PI3Kδ抑制剂林普利司(YY-20394)之后璎黎药业在美国获批临床试验的又一创新药物。KRAS基因突变存在于多种肿瘤中,其中G12C突变主要存在于肺癌、结直肠癌和胰腺癌。今年5月,安进的KRAS G12C抑制剂sotorasib获FDA加速批准上市,是首款、也是目前唯一一款获批上市的KRAS抑制剂,用于治疗经治KRAS G12C突变的非小细胞肺癌患者。
国内药讯
1.国药新冠疫苗获批国内青少年接种。国药中生北京公司新冠灭活疫苗获国务院联防联控机制有关部门批准在3-17岁人群中紧急使用。一项在河南完成的I/II期临床结果显示,3-17岁人群免疫后中和抗体阳转率为100%,中和抗体GMT和阳转率与成人组相比无显著性差异;接种后安全性良好,不良反应主要为发热和接种部位疼痛,未见严重不良反应。目前,该疫苗正在阿联酋阿布扎比开展这一年龄组的免疫桥接临床试验。
2.太阳药业「磷酸索尼德吉」将在华获批。印度太阳药业5.1类进口新药「磷酸索尼德吉」的中国上市申请审评状态变更为「在审批」,预计即将获批上市。磷酸索尼德吉是诺华研发的一种口服选择性SMO抑制剂,该药已被FDA批准用于治疗那些在手术后或放射治疗后出现病情复发,或是不适合采用手术或放射治疗的局部晚期基底细胞癌患者。太阳药业拥有该新药全球权益。
3.赛生药业CD47靶向疗法获批临床。赛生药业引进的1类新药RRx-001注射液获CDE临床试验默示许可,拟开发用于治疗广泛期小细胞肺癌(SCLC)。RRx-001是EpicentRx公司开发的一款靶向CD47-SIRPα的小分子免疫疗法,已在全球进入SCLC适应症的Ⅲ期临床。此前公布的一项Ⅱ期研究数据显示,在26例SCLC患者中,RRx-001联合化疗组的总生存期(OS)达到8.6个月,无进展生存期为7.5个月。
4.石药ADC品种获FDA临床许可。石药Claudin 18.2-ADC新药SYSA1801获FDA批准,即将在美国开展I期临床,评估SYSA1801用于治疗Claudin 18.2阳性表达晚期胰腺癌的安全性、耐受性、药代动力学特性及初步疗效。临床前研究显示,该产品对胰腺癌具有优异的体内外活性和良好的安全性,有望在临床试验中展现出良好的治疗效果。FDA已于今年授予SYSA1801用于治疗胰腺癌的孤儿药资格。
5.开拓药业和复星医药达成合作协议。开拓药业宣布与复星子公司复星医药产业就其AR拮抗剂普克鲁胺治疗新冠在印度和28个非洲国家的商业化达成合作协议,双方将共同推进普克鲁胺新冠适应症的紧急使用授权(EUA)申请、推广和销售工作。此项合作总金额高达5.6亿元人民币。开拓药业将基于产品在合作区域内的未来净销售额,分级收取不低于利润总额的50%作为销售提成。
国际药讯
1.FDA批准首款ROCK2抑制剂上市。FDA批准Kadmon制药公司新型ROCK2激酶抑制剂Rezurock(belumosudil)上市,用于治疗12岁以上、已接受过两种前期全身性治疗的慢性移植物抗宿主病(cGVHD)患者。在一项ROCKstar研究中,Rezurock达到75%的总缓解率;有62%获得缓解的患者在缓解后至少12个月不需要使用新的全身性疗法;中位缓解持续时间为1.9个月。FDA此前授予belumosudil治疗cGVHD的突破性疗法认定和孤儿药资格。
2.默克MET抑制剂获英国EAMS项目批准。英国药品和保健品管理局(MHRA)在药品早期获取计划(EAMS)项目中批准默克MET抑制剂Tepmetko(tepotinib)治疗携带METex14突变的晚期非小细胞肺癌(NSCLC)患者。在一项II期VISION研究中,经合并活检组(液体活检+组织活检)的独立评估,Tepmetko治疗的客观缓解率(ORR)达到46%。Tepmetko是全球首款获批用于治疗携带MET突变的晚期NSCLC患者的口服MET抑制剂。
3.长效C5补体抑制剂Ⅲ期临床积极。Alexion Pharmaceuticals长效C5补体抑制剂新药Ultomiris(ravulizumab)在治疗成人全身性重症肌无力(gMG)患者的Ⅲ期临床中达到主要终点。与安慰剂组相比,Ultomiris组第26周时的MG-ADL评分(日常生活能力)较基线相比获得统计学意义的改善(-3.1vs-1.4,p<0.001);该组QMG评分(量化重症肌无力总分)也显著改善;而且患者的MG-ADL和QMG评分的改善持续时间为52周。Alexion计划向FDA、欧盟(EU)等监管机构提交监管申请。
4.辉瑞/BioNTech新冠疫苗获FDA优先审评资格。FDA授予辉瑞与BioNTech联合开发的mRNA新冠疫苗优先审评资格,用于在16岁以上人群中预防COVID-19,PDUFA日期为2022年1月。值得一提的是,该疫苗上述适应症此前已获FDA授予紧急使用授权(EUA),而且FDA于今年5月将这一EUA的使用范围扩展用于在12-15岁青少年中预防COVID-19。目前两家公司正在12-15岁青少年中积累第二剂疫苗接种后6个月的数据,将用于补充上述申请。
5.益普生购进多巴胺受体拮抗剂全球权益。益普生与IRLAB公司签署了一项授权协议,益普生将获得创新多巴胺D3受体拮抗剂mesdopetam的全球开发和推广权益。mesdopetam目前正在Ⅱb期临床中评估用于治疗帕金森病患者在接受左旋多巴治疗之后出现的运动障碍。根据协议,IRLAB将获得2800万美元的前期付款,可能达3.35亿美元的开发、监管和推广里程碑付款。
6.Nimbus完成新一轮融资。Nimbus公司宣布完成一项1.05亿美元的融资。Nimbus旨在利用其基于蛋白质结构的药物发现技术平台,设计靶向蛋白质的强效和选择性小分子创新药物。此轮融资将用于推进其新型抗炎TYK2别构抑制剂的多项Ⅱ期临床,试验将在2021年与2022年进行;还将用于推进其新型HPK1抑制剂在实体瘤患者中的早期临床;以及用于加速其针对肿瘤和免疫学多个靶点的临床前项目。
7.强生召回多款防晒喷雾。强生公司当地时间14日宣布,由于在内部检测中发现部分样品中有含量较低的苯,将主动召回公司旗下几款防晒喷雾(露得清和艾维诺 ) 。目前,强生已通知分销商和零售商停止销售产品、安排退货,并调查样品被污染的原因。受影响的喷雾数量以及确切的苯含量尚未公开。强生强调消费者应停止使用受污染的防晒喷雾。
医药热点
1.WHO呼吁建立人类基因组编辑研究机构。世卫组织(WHO)日前针对人类基因组编辑研究提出新建议,呼吁建立一个全球注册机构来管理所有涉及人类基因组编辑的研究;呼吁开发一种用于识别任何可能涉及基因编辑试验的方法和机制,或建立一种揭发机制用于报告违反研究完整性的行为。WHO还希望能找到有更快速的方法来评估基因编辑治疗的有效性。
2.广州将启动12-17岁人群接种新冠疫苗。广州市卫健委官网发布,广州市即将启动12岁~17岁的未成年人群新冠疫苗接种工作。12-17岁未成年人的接种将实行团体预约,原则上由学校或街(镇)、居(村)委统一组织。截至2021年7月14日,广州市共完成接种2389万剂次,1362万人接种,其中完成全程接种1034万人。
3.甘肃卫健委与上海瑞金医院合作。甘肃省卫健委主任郭玉芬带队赴上海交通大学医学院附属瑞金医院,就瑞金医院与甘肃省合作培养卫生健康人才达成合作协议。根据协议,上海瑞金医院将发挥自身的优势专业,开展针对甘肃省卫生健康人才的合作培养工作;建立培养卫生健康人才的长效合作机制,成立合作协调机构,不定期召开协调会议,及时沟通交流,全力提升甘肃省市、县级医疗机构专业技术人员能力和服务水平。
审评动向
2. FDA新药获批情况(北美07月16日)
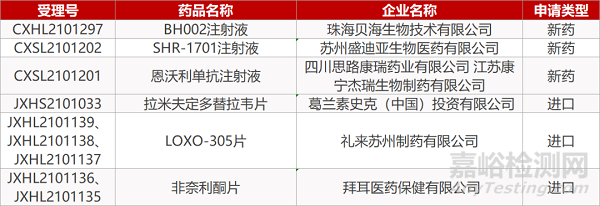
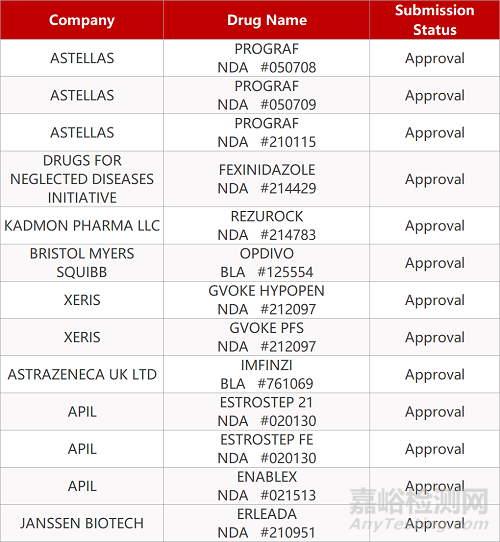

来源:药研发