嘉峪检测网 2021-07-27 11:45
导读:医药研发每天最新资讯汇总
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.度普利尤单抗将获批新适应症。赛诺菲度普利尤单抗在国内的第二个上市申请审批状态变更为"在审批",预计即将获批,联合或不联合外用皮质类固醇,用于治疗12岁及以上青少年和成人中重度特应性皮炎患者。在国内,度普利尤单抗已于去年6月获NMPA批准用于治疗外用处方药控制不佳或不建议使用外用处方药的成人中重度特应性皮炎患者,商品名为达必妥。该新药目前已通过医保谈判进入2020年国家医保。
2.广生堂乙肝创新药上Ib期临床。广生堂治疗乙肝创新药GST-HG141在Ib期临床中完成首例患者入组给药。GST-HG141是一款全新靶点的乙肝核心蛋白抑制剂,可抑制HBV(乙肝病毒)衣壳的脱壳与组装,属于该公司乙肝临床治愈“登峰计划”组合方案的重要组件。来自Ia期临床结果显示,GST-HG141片各研究剂量组在中国健康受试者中均可耐受,安全性良好,血浆浓度达到预期目标。
3.南京征祥抗流感新药报IND。南京征祥医药化学1类新药ZX-7101A片的临床试验申请获CDE受理。ZX-7101A是该公司自主研发的一款RNA聚合酶(PA)抑制剂,可有效地抑制甲型与乙型流感病毒PA中帽状-依赖型核酸内切酶(CEN)的活性。临床前的药学研究表明ZX-7101A具有良好的抗甲流和乙流的药效,且口服生物利用度良好。
4.三生国健HER2/PD-1双抗国内报IND。三生国健1类创新型生物制品注射用SSGJ-705的临床试验申请获NMPA受理。SSGJ-705是三生国健自主研发的一款重组HER2/PD-1双特异抗体注射液。该新药可将HER2靶向治疗与免疫检查点阻断治疗相结合,从而更有效地治疗HER2阳性实体瘤。SSGJ-705已于2021年6月在美获批临床,此次为国内首报临床。
5.瑞科生物赴港IPO。瑞科生物在港交所递交了IPO申请,联席保荐人为摩根士丹利、招银国际、中信证券,募集的资金将主要用于在研疫苗产品的研发。根据招股书,该公司已建立一条包括11款在研创新型疫苗的产品管线,涵盖宫颈癌、新冠肺炎、成人结核病、带状疱疹、手足口病及流感等疾病。其核心产品REC603是一款重组HPV九价疫苗,旨在提供针对HPV 6型、11型、16型、18型、31型、33型、45型、52型、58型的保护。REC603目前处于III期临床开发阶段。
国际药讯
1.欧盟CHMP支持赛诺菲新一代庞贝病疗法。欧洲药品管理局人用药品委员会(CHMP)推荐批准赛诺菲M6P靶向酶替代疗法avalglucosidase alfa上市,用于治疗糖原贮积病Ⅱ型(又名庞贝病)患者。与标准治疗α-葡萄糖苷酶相比,avalglucosidase alfa的M6P含量增加约15倍,旨在帮助改善细胞对酶的摄取并增强目标糖原清除。目前该疗法也正接受FDA的审查,预计在今年8月做出回复。
2.毛果芸香碱创新眼科配方Ⅲ期临床积极。艾伯维旗下艾尔建开发的毛果芸香碱创新眼科配方AGN-190584,在治疗老花眼的Ⅲ期临床GEMINI 1中达主要终点指标。与安慰剂相比,AGN-190584治疗组第30天时有更多患者的DCNVA(检测近视力)指标获得三行或三行以上改善;而且AGN-190584在用药15分钟后生效,效果可长达6个小时。AGN-190584的新药申请目前正在接受FDA审评,预计在今年年底做出回复。
3.Denali酶替代疗法早期临床积极。Denali Therapeutics基于ETV技术开发的能够穿越血脑屏障的酶替代疗法DNL310,在治疗黏多糖贮积症II型(MPS II,又名亨特综合征)患者的Ⅰ/Ⅱ期临床中获积极结果。每周一次DNL310治疗的所有患者脑脊液(CSF)中的硫酸乙酰肝素(HS)水平降低到正常水平;而且CGI量表评估(CGI-C)结果显示,患者的认知能力,行为和运动能力都出现临床改善。Denali计划明年上半年启动关键性Ⅱ/Ⅲ期临床试验。
4.罗氏与FDA就AD抗体Gantenerumab展开谈判。罗氏日前透露正在与FDA就其阿尔茨海默病(AD)候选药物Gantenerumab进行谈判。在临床试验DIAN-TU-001(NCT01760005)中,与礼来Solanezumab相比,Gantenerumab显著减少遗传、早发性AD患者淀粉样蛋白斑块,降低了脑脊液(CSF)总tau和磷酸化tau181(p-tau181)水平;但没有显示出对改善AD患者认知有益的证据。目前探索性开放标签扩展研究仍继续监测该药物随着时间的推移对患者症状的影响。Gantenerumab的Ⅲ期试验预计将在明年下半年完成。
5.Anocca完成4700万美元B轮融资。Anocca公司宣布完成4700万美元的B轮融资,用于支持公司的工业化(industrialized)细胞生物学平台,并推进其TCR-T细胞免疫疗法管线到Ⅰ/Ⅱa期临床试验。Anocca细胞生物学平台由许多专有的细胞生物学和分子遗传学技术组成,能够对T细胞进行高精度分析,并利用T细胞的免疫力,开发具有高度靶向性的疗法。
6.渤健2021半年报营收55亿元。渤健公布2021半年业绩,上半年营业收入54.69亿美元,同比下滑24.21%,其中产品收入44.48亿美元,同比下滑-21.97%;净利润14.30亿美元,同比下降52.31%。值得一提的是,Biogen阿尔茨海默病新药Aduhelm(aducanumab)于今年6月获得FDA批准。上市销售不到半个月的时间,为该公司贡献了160万美元的收入。Biogen还计划开展Aduhelm验证性IV期临床、长期随访安全性及耐受性研究以及真实世界观察性研究。
医药热点
1.医保覆盖“互联网+”医疗服务收费项目。四川省医保局发布《关于四川省第二批“互联网+”医疗服务价格项目试行价格和医保支付政策专家论证结果的公示》。根据公示,本次新增4项目互联网+医疗服务价格项目。分别为远程心电监测、远程起搏器监测、家庭自动腹膜透析远程监测和远程多参数监测。其中除远程起搏器监测医保基金不予支付外,其他三项根据支付标准纳入医保乙类支付。
2.我国分级诊疗取得阶段性成效。国家卫健委日前在新闻发布会上介绍我国分级诊疗制度与体系建设、综合医院中西医协同发展有关情况。截至2020年年底,我国重点人群的家庭医生签约率从2015年的28.33%增加到75.46%,全国县域内就诊率达94%,比2015年同期增长10个百分点;患者下转人次年均增长率达38.4%;日间手术试点病种达120种,“五大中心”建设累计超过1.4万个;各种模式的医联体超过1.5万个。
3.生育三孩费用纳入生育保险待遇支付范围。国家医保局日前发布《关于做好支持三孩政策生育保险工作的通知》。通知提出,积极支持三孩生育政策落地实施,确保参保女职工生育三孩的费用纳入生育保险待遇支付范围,各地医保部门要按规定及时、足额给付生育医疗费用和生育津贴待遇,切实保障参保人员生育保障权益。同步做好城乡居民生育医疗费用待遇保障和新生儿参保工作。
审评动向
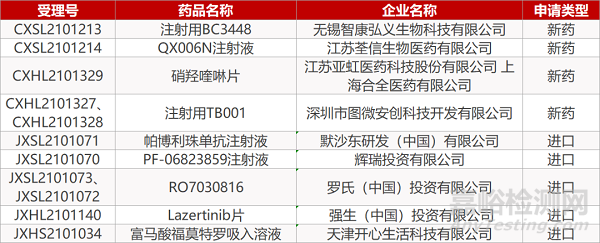
无锡智康弘义生物的注射用BC3448、江苏荃信生物的QX006N注射液、江苏亚虹医药、上海合全的硝羟喹啉片、深圳市图微安创科技的注射用TB001(2个规格)、默沙东的帕博利珠单抗注射液、辉瑞的PF-06823859注射液、罗氏的RO7030816(2个规格)、强生的Lazertinib片。
来源:药研发