嘉峪检测网 2021-11-29 21:31
导读:本文主要介绍了重庆永仁心医疗器械有限公司研发的创新医疗器械“植入式左心室辅助系统”的临床前研发实验。
本文主要介绍了重庆永仁心医疗器械有限公司研发的创新医疗器械“植入式左心室辅助系统”的临床前研发实验。
一、植入式左心室辅助系统的产品结构及组成
该产品由体内部件、体外部件、手术工具组成,其中体内部件包括血液泵组件(含泵缆)、入血管、出血管,体外部件包括控制器、控制器连接元件、纯水密封构成组件、纯水密封流路清洗组件、 AC/DC适配器、电池、充电器、紧急备用电池、备用控制器、外部监控器、外部监控器底座、外部监控器连接线缆、操作钥匙,手术工具包括隧道刀、穿孔器、手术扳手、解剖器。
二、植入式左心室辅助系统的产品适用范围
该产品由体内部件、体外部件、手术工具组成,其中体内部件包括血液泵组件(含泵缆)、入血管、出血管,体外部件包括控制器、控制器连接元件、纯水密封构成组件、纯水密封流路清洗组件、 AC/DC适配器、电池、充电器、紧急备用电池、备用控制器、外部监控器、外部监控器底座、外部监控器连接线缆、操作钥匙,手术工具包括隧道刀、穿孔器、手术扳手、解剖器。
三、植入式左心室辅助系统的型号/规格
EVAHEART Ⅰ
四、植入式左心室辅助系统的工作原理
该产品通过入血管将血液由左心室引入血液泵,由血液泵叶轮转动产生的离心力将血液从血液泵内排出,经出血管流至升主动脉, 从而支持患者血液循环,详见图1。
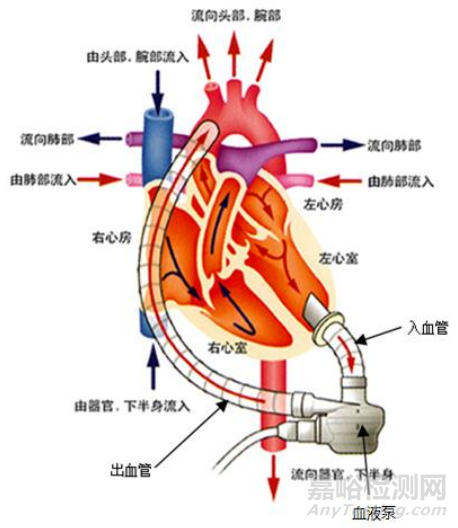
图1 工作原理示意图
五、植入式左心室辅助系统的产品性能研究
该产品性能指标包括血液泵、出入血管、控制器、纯水密封构 成组件、手术工具、软件功能、物理性能、化学性能、无菌、环境试验、电气安全、尺寸重量、材质、连接性能、极端条件响应、耐 久性等要求。 重庆永仁心提交了该产品与日本已上市产品实质等同性分析报告、 流体动力学仿真计算报告、流场可视化分析报告、MPC涂层研究报 告、耐久性研究报告等资料,并提交了产品技术要求与产品检测报 告,检测结果与产品技术要求相符。
六、植入式左心室辅助系统的生物相容性研究
该产品体内部件所含血液泵、出入血管与血液持久接触,泵缆 与组织持久接触,体外部件所含纯水密封构成组件与血液持久接触, 手术工具与血液短期接触。 重庆永仁心按照GB/T 16886系列标准要求开展了生物相容性评价, 包括细胞毒性、皮内反应、皮肤致敏、急性全身毒性、亚慢性毒性、 遗传毒性、植入、血液相容性,证实该产品生物相容性风险可接受。
七、植入式左心室辅助系统的灭菌研究
该产品体内部件全体及体外部件所含控制器连接元件、纯水密 封构成组件、纯水密封流路清洗组件采用环氧乙烷灭菌,手术工具 均采用湿热灭菌,其中穿孔器为一次性使用,解剖器、隧道刀、手 术扳手为重复使用。 重庆永仁心提交了灭菌确认报告,证实所用灭菌方法可实现有效灭菌,且不会影响产品使用性能。
八、植入式左心室辅助系统的产品有效期和包装研究
重庆永仁心提交了产品有效期研究资料,其中血液泵组件、控制器 连接元件、纯水密封构成组件、纯水密封流路清洗组件、隧道刀、 手术扳手、解剖器的无菌货架有效期为2年,入血管、出血管、穿 孔器的无菌货架有效期为37个月。 重庆永仁心提交了产品包装验证报告,证实包装完整性符合设计要 求。
九、植入式左心室辅助系统的动物实验研究
重庆永仁心采用牛模型开展了三次动物实验,分别验证产品的机械 稳定性与血液相容性、抗血栓性能、耐久性,包括血液泵运转性能 与轴密封性能、血液指标、血栓形成情况、内皮化情况、长期稳定 性等评价,实验结果表明产品能够达到预期设计要求。
十、植入式左心室辅助系统的软件研究
该产品软件安全性级别为C级,控制器软件发布版本为1.4,完 整版本为1.4.0;备用控制器软件发布版本为2.0,完整版本为2.0.2; 外部监控器软件发布版本为2.3,完整版本为2.3.2。重庆永仁心按照《医 疗器械软件注册技术审查指导原则》要求,提交了相应级别的软件 描述文档和软件版本命名规则真实性声明,证实该产品软件设计开发过程规范可控,剩余风险均可接受。 重庆永仁心根据《医疗器械网络安全注册技术审查指导原则》要求, 提交了网络安全描述文档,证实该产品现有网络安全风险可控,已 建立网络安全应急响应计划。
十一、植入式左心室辅助系统的产品符合的相关标准
该产品符合以下安全标准要求: GB 9706.1-2007 医用电气设备第1部分:安全通用要求; GB 9706.15-2008 医用电气设备第1-1部分:安全通用要求并列 标准:医用电气系统安全要求; YY 0505-2012 医用电气设备第1-2部分:安全通用要求并列标 准:电磁兼容要求和试验; YY 0709-2009 医用电气设备第1-8部分:安全通用要求并列标 准:通用要求医用电气设备和医用电气系统中报警系统的测试和指 南; GB 16174.1-2015 手术植入物有源植入式医疗器械第1部分:安 全、标记和制造商所提供信息的通用要求。 重庆永仁心提交了相应检测报告,证实该产品符合上述安全标准要 求。

来源:嘉峪检测网
关键词: 创新医疗器械 植入式左心室辅助系统