不仅能缝合伤口,还能感知炎症并输送治疗药物!
伤口闭合是防止异物进入和支持伤口愈合的关键。由于机械损伤或炎症导致的伤口闭合失败可导致组织有效附着失败,并表现为延迟愈合甚至死亡(这取决于伤口的部位)。因此,一个能够识别炎症以及提供治疗方法的平台,包括化学、生物和细胞疗法,可以改变我们有效感知潜在失败的能力,并最大限度地提高治疗效果。
基于此,麻省理工学院的Giovanni Traverso教授团队报告了一种去细胞化的肠组织(De-gut)缝合线的发展,该缝合线能够感知炎症并提供广泛的治疗方法,包括小分子,单克隆抗体和基于细胞的治疗方法。作者在啮齿动物和猪身上展示了其机械和生物功能,并期望它可以改变我们对伤口和患者的护理方式。该工作以“A multifunctional decellularized gut suture platform”为题发表在Matter,并被Nature亮点报道。
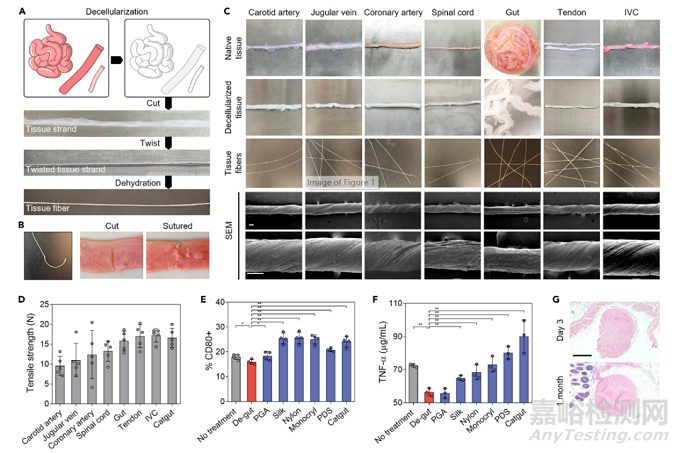
为了制造组织来源的缝合纤维,作者首先使用洗涤剂溶液将组织去细胞化,产生白色去细胞化基质(图1A)。然后纵向打开去细胞化组织,切成几条预先确定宽度的长组织链。随后通过扭转和组织链脱水制备纤维形式的缝合线(图1A-C)。为了测试去细胞化组织缝合线的缝合能力,作者将一根手术针附着在纤维末端,缝合在切开的肠组织上,制备的缝合线能够实现良好的贴合,防止内部内容物泄漏。与市售的组织源羊肠缝合纤维(16.6 G 2.4 N)相比,作者制备的缝合线具有强大的抗拉强度(图1D),因此进一步开发的重点是去细胞化肠组织(De-gut)支架。通过利用去细胞化基质制造缝线,基于保存原生组织中的ECM成分,可能增强缝线的组织再生能力。通过小鼠皮下植入缝合线,初步评价其体内相容性和组织反应。对取出的纤维与邻近组织进行组织学分析发现,植入3天、1个月后,植入的组织纤维没有明显的炎症和异物反应,这表明植入的缝合纤维周围几乎没有纤维化组织的形成和免疫细胞的聚集。这些数据证明了低免疫模量的De-gut缝合线的体外和体内相容性(图1G)。
图1 去细胞化基质缝合纤维的制备与表征
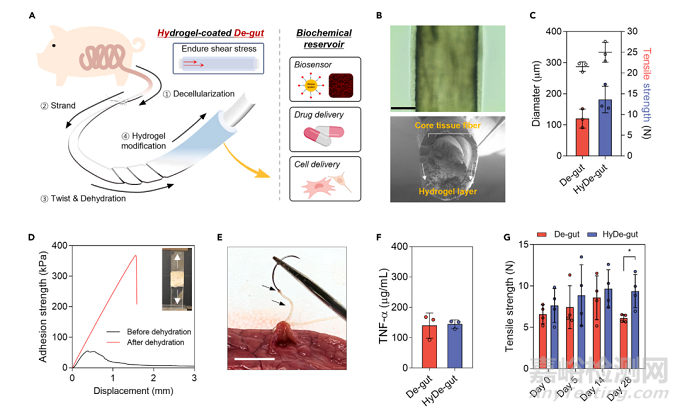
为了支持基于De-gut缝合线的治疗平台的开发,作者在De-gut缝合线的表面进一步设计了一层薄薄的水凝胶层。这些带有水凝胶涂层的增强型HyDe-gut缝合线可以支持治疗和诊断成分的药物的输送,以帮助最大限度地提高伤口护理和监测的能力(图2A)。显微镜图像显示,De-gut缝合线表面成功地修饰了一层薄而均匀的水凝胶层。添加水凝胶层可使HyDe-gut缝线的最终直径增加20-25 mm。为了评估改性水凝胶层在De-gut表面的粘附力,在两个肠道组织基质之间形成水凝胶层后进行实验室剪切测试。经水凝胶改性后的最大粘接强度为~55 kPa,脱水后黏附力显著提高至~370 kPa(图2D)。然而,基于最终产品中水凝胶层稳定而紧密的组织粘附,甚至以水合形式存在,在缝合过程中,水凝胶层没有从De-gut缝合线上脱离(图2E)。重要的是,尽管De-gut缝合线表面覆盖了一层薄薄的水凝胶层,但通过培养巨噬细胞分泌TNF-a来评估,De-gut缝合线的免疫原性在De-gut缝合线孵育组之间是相似的(图2F)。这种水凝胶涂层可以携带各种组分,比如药物、传感器甚至治疗细胞,还可以增加强度。当用于缝合大鼠伤口时,水凝胶涂层缝合线在四周后比未涂层缝合线牢固得多。
图2 水凝胶修饰脱肠缝合线表面作为多功能治疗平台
作者在水凝胶中加入了可以感知炎症的微米大小的颗粒:当炎症酶存在时,这些颗粒会降解并释放出一种可以在尿液中检测到的染料。作者还在水凝胶中嵌入了携带药物和细胞的微粒。作者说,这些配方可以让智能缝合线提供化学和细胞治疗。
【小结】
作者提出了一种由去细胞化基质和水凝胶组成的多功能生物相容性缝合治疗平台。De-gut纤维作为核心缝合材料,以最小的组织反应增强组织再生,水凝胶层为将各种功能集成到缝合平台提供了空间。随着纳米和微加工技术的最新进展,其他生物功能形式也可以很容易地在HyDe-gut缝合平台中结合,最终将增强伤口愈合和疾病治疗。
报道链接:https://www.nature.com/articles/d41586-023-01591-z
原文链接:https://doi.org/10.1016/j.matt.2023.04.015

来源:BioMed科技
关键词:
水凝胶
缝合线