摘 要 / Abstract
真实世界研究是基于真实环境而非理想环境开展的科学研究。新型冠状病毒流行期间,由于受毒株的高变异性、公共卫生政策的动态性等因素的影响,随机对照临床试验难以准确及时地评估新冠病毒疫苗效果,真实世界研究受到广泛重视。本文通过对2020年以来新冠病毒疫苗真实世界研究的系统梳理,总结不同研究类型及其设计与统计分析,比较了各种研究的优势与劣势,概括了新冠病毒疫苗真实世界研究面临的挑战和可能的解决途径,以期为开展高质量疫苗真实世界研究提供参考。
Real world studies are scientific research conducted in real world settings rather than ideal conditions. During the COVID-19 pandemic, due to factors such as the high variability of viral strains and the dynamic nature of public health policies, randomized controlled clinical trials struggled to assess the effectiveness of COVID-19 vaccines accurately and timely.Consequently, real world studies have gained widespread attention in this context. This article provides a systematic review of real world studies on COVID-19 vaccines conducted since 2020, summarizing various study types, their designs, and statistical considerations. It compares the strengths and weaknesses of different study approaches, outlines the challenges faced by real world studies on COVID-19 vaccines, and suggests potential solutions. The aim is to provide insights for conducting highquality real world vaccine studies.
关 键 词 / Key words
真实世界研究;新冠病毒疫苗;疫苗保护效果;检测阴性设计;队列研究;模仿目标试验
real world study; COVID-19 vaccine; vaccine effectiveness; test-negative design; cohort study; target trial emulation
1、背 景
疫苗临床研究与药物临床研究相比,在安全性和有效性临床评价方面有所不同。(1)安全性评价:疫苗临床研究的目标人群通常为暴露风险下的健康人群,因此对于安全性方面的考虑会更多,所需样本量更大,以充分评估疫苗接种相关的罕见不良事件。(2)有效性评价:通常需要同时考虑免疫原性和疫苗保护效力(vaccine efficacy),并以保护效力作为评价疫苗有效性的直接证据。
随机对照临床试验(randomized controlled clinical trial,RCT)普遍被认为是评价药物有效性的“金标准”[1-4],无论是采用较为严格的入选或排除标准,还是基于随机化分配治疗干预,都能够很好地减少各种偏倚(如混杂因素、信息偏倚、选择偏倚等)和其他因素对有效性评估的影响,使得研究结论更为可靠。在疫苗的临床研究中,这种观念同样被广泛接受[5]。
然而,疫苗的RCT亦有其局限之处:(1) RCT严格的入选或排除标准使得临床试验人群不能充分代表目标人群,其研究结果对于真实世界的疫苗保护效果(vaccine effectiveness,VE)的外推性较差;(2)虽然疫苗RCT的样本量较大,但对于在真实世界环境下发现罕见不良事件仍显不足;(3)随访时间较短,所得到的有效性结论可能会受限于流行的病毒株和当前的公共卫生政策;(4)存在伦理问题,安慰剂组的受试人群仍然可能会受到传染性疾病的影响;(5)如果进行头对头比较,RCT会花费高昂的时间和经济成本[2-3]。
2019年以来新型冠状病毒的大规模流行使上述问题更为突出[6]。新冠疫情期间,新冠病毒毒株变异所导致的流行特征变化、公共卫生政策及其变动、多种疫苗获批上市等重要因素对疫苗保护效果产生的影响,仅靠RCT难以及时获得不同疫苗在真实世界环境下的预估效果,从而影响公共卫生政策制定或修订的准确性和及时性,进而影响对新冠疫情的防控效果。鉴于此,新冠病毒疫苗的真实世界研究(real world study,RWS)受到广泛重视,并及时为公共卫生政策决策提供了依据。本文系统梳理近3年来不同新冠病毒疫苗的RWS,介绍不同研究类型及其设计与统计分析,对比各种研究设计的优势与劣势,以期为开展高质量疫苗RWS提供参考。
2、已发表新冠病毒疫苗RWS相关文献分析
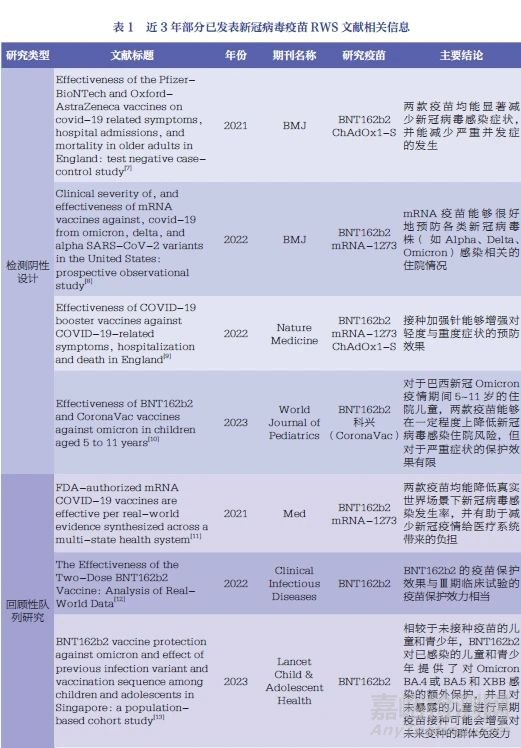
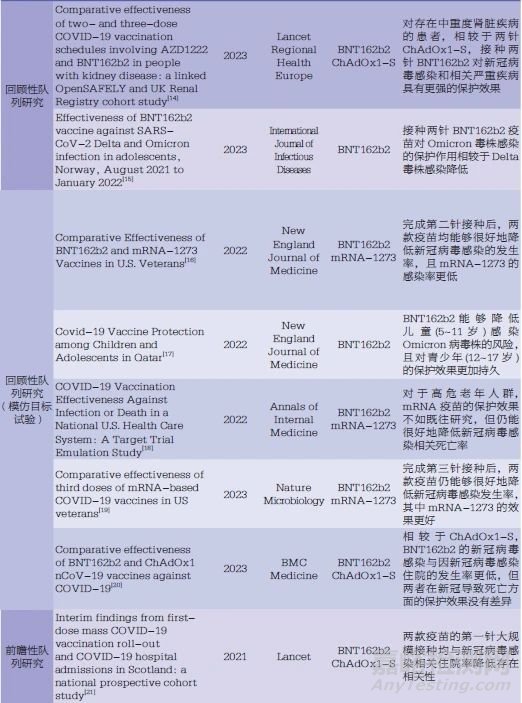
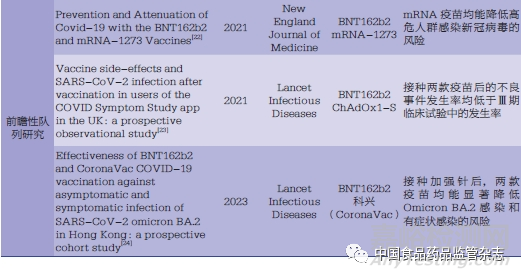
新冠病毒疫苗RWS均为观察性研究,主要包括病例-对照研究(case-control study)、回顾性队列研究(retrospective cohort study)和前瞻性队列研究(prospective cohort study)。其中,病例-对照研究又以检测阴性设计(testnegative design)为主。此外,近年来兴起基于模仿目标试验(target trial emulation)的思路设计队列研究的研究方案,以达到模仿目标RCT,产生更加稳健的真实世界证据的目的。表1简要汇总了近3年部分已发表新冠病毒疫苗RWS文献的相关信息,笔者在后文针对各类研究类型的研究设计、优缺点以及分析策略进行了讨论说明。
3、研究类型
(一)病例-对照研究及检测阴性设计
1. 研究设计
病例-对照研究属于回顾性研究,数据来源通常为现有医疗记录和历史数据,因此能够以较少的时间和经济成本得以开展。与此同时,由于采用的是既往已有数据,其质量往往较前瞻性研究所获取的数据差。病例-对照研究通常在目标人群中先选择病例组,然后采用匹配方法按一定比例选择对照组,以尽可能缩小病例组与对照组在重要变量上的差异[25]。
检测阴性设计属于病例-对照研究,2005年首次被用于评估流感疫苗保护效果[26],并逐渐受到公共卫生领域的关注[27]。检测阴性设计与一般的病例-对照研究设计不同之处在于,其病例组与对照组都来自于目标疾病的疑似病例(如表现出新冠病毒感染症状后前来医院就诊的人群),并对该人群进行检测,根据检测结果分配病例组与对照组,再回溯两组人群的疫苗暴露历史,最终得到疫苗的保护效果。
检测阴性设计的主要优势是可以减少目标人群异质性可能带来的偏倚。例如,有研究者通过检测阴性设计,对2021年4月至2022年1月的出现新冠病毒感染类似症状的住院患者进行检测,根据检测结果阳性或阴性确定病例组或对照组,进而分析新冠病毒疫苗对于Alpha、Delta和Omicron病毒株的保护效果[8]。另有研究者采用类似的设置,对2022年2月~6月期间巴西的因严重急性呼吸道综合征住院的儿童进行分析,基于PCR或抗原的检测结果划分为病例组或对照组,发现在Omicron病毒株流行时期,即使完全接种了BNT162b2和科兴的两款疫苗,儿童的疫苗保护效果以及对危重症的保护效果均有所降低[10]。上述两项研究将研究对象限定为出现新冠病毒感染类似症状的住院患者,他们的健康寻求行为、接触史和症状严重性等特征类似,因此可以降低产生偏倚的风险。
然而,检测阴性设计所得到的疫苗保护效果容易受到检测方法特异度的影响[27-28]。若检测方法的特异度不足,假阳性病例分布在病例组的比例则会增加,进而导致疫苗保护效果被低估[29]。因此,在疫苗保护效果的评估中,检测阴性设计通常会采用高特异度的检测手段。同时也应注意,灵敏度不足亦会导致疫苗保护效果的估计产生偏倚[30]。
2. 统计分析
病例-对照研究,包括检测阴性设计,多基于比值比(odds ratio,OR)评估疫苗保护效果。通常会通过Logistic回归模型对OR进行估计,模型中会纳入较为重要的协变量。求得OR后,可根据下式计算疫苗保护效果(VE)(%):
VE (%) = (1-OR) x100%
(二)回顾性与前瞻性队列研究
1. 研究设计
根据数据来源,队列研究可分为回顾性队列研究、前瞻性队列研究和回顾前瞻性队列研究,后文主要针对前两种类型进行讨论。队列研究根据从暴露到结局的顺序产生的纵向数据进行因果推断,故较病例-对照研究从结局到暴露的推断更为可靠。
队列研究设计首先根据暴露情况确定暴露组或队列(如已接种某种疫苗的人群)和非暴露组或队列(如未接种该疫苗的人群),并对这两组人群进行长期随访观察,直到发生感兴趣的结局事件或研究结束。然后,通过比较两组或队列人群的结局事件发生情况,评估暴露(接种疫苗)是否与结局(感染)存在关系。
回顾性队列研究主要具有两个优点:(1)相较于病例-对照研究,能够以相似的经济与时间成本得到更强的因果关系;(2)相较于前瞻性队列研究,能够更好地研究特定情况下的暴露,因为可以在大量的历史数据中找到足够多的暴露人群,进而快速形成研究队列[31]。
回顾性队列研究的局限在于既往数据内容与质量不可控,如研究人群的特征无法反映真实世界的人群分布特征、关键的混杂因素存在遗漏情况等,从而影响研究结论的准确性、稳健性与外推性[11,32]。有研究者采用回顾性队列研究比较了两款获得美国食品药品监督管理局(FDA)批准上市的mRNA疫苗。该研究采用倾向性评分方法,分析得到这两款疫苗预防新冠病毒感染的保护效果分别为86.1%(95%置信区间:82.4%~89.1%)和93.3%(95%置信区间:85.7%~97.4%)。然而,该研究的人口学特征与自然人群有较大差异,如研究人群的90%以上为白色人种,以及其中一款疫苗研究人群的50%年龄超过65岁等,因此该研究结论尚不足以外推至自然人群[11]。此外,在一项2023年5月的研究中,有研究者基于Open SAFELY平台对英国国家医疗服务体系中患有慢性肾脏病的患者进行分析,以探究不同接种策略的疫苗保护效果,如两针均为Ch Ad Ox1-S或BNT162b2,但在接种加强针时选择另一种疫苗。尽管研究结果表明Ch Ad Ox1-S的疫苗保护效果(包括对危重症患者的疫苗保护效果)不如BNT162b2,但研究者认为,分析数据中接种Ch Ad Ox1-S人群的特征(如年龄或疾病特征)可能难以代表真实世界中患有慢性肾脏病的人群,因此仍需要谨慎解释两种疫苗保护效果的差异[14]。
前瞻性队列研究可以根据研究目的与实际情况确定数据收集方法、数据库融合方式、研究变量和数据管理计划等[22,33-34],因此能够产生更高质量的观察性研究证据。然而,高昂的经济与时间成本、失访、罕见结局的采集等也是研究者在设计阶段需要着重考虑的问题。例如,随着新冠病毒毒株的更替,可能较难出现Alpha病毒株的感染情况[35],如果盲目对其开展前瞻性队列研究,则很可能无法得到感兴趣的结局事件。此外,如果随访时间不足,研究结束时研究人群可能还未发生感兴趣的结局事件(如住院或死亡),也会影响对于疫苗针对这类事件保护效果的评估[22,34]。
2. 统计分析
队列研究主要基于相对危险度(relative risk,RR)评估暴露与结局的关系,由于研究人群的随访时间不一定完全一致,观察期较长的人有更大概率发生事件。为避免由此产生偏倚,在疫苗RWS中,研究者更多会采用发生率比(incidence rate ratio,IRR)评估疫苗保护效果。
研究者一般采用Poisson回归模型估计IRR,因为该模型在考虑发生率的基础上,还会将每个人的观察时间作为一个“偏移量”(offset),并将其包含在模型中进行调整,这时估计得到的是结局事件的发病速率,而不只是发病率。如果模型出现过度离散(overdispersion)的情况,即观测到的数据的方差大于均值,则需要采用负二项回归估计IRR。此外,Cox比例风险模型也能在考虑每个人的观察时间的基础上,通过估计风险比(hazard ratio,HR)评估暴露对于结局事件的影响。
对于IRR,VE(%)可通过下式计算:
VE (%)=(1-IRR) x100%
而对于HR,可以通过类似的公式计算得到相应的VE(%):
VE (%)=(1-HR) x100%
(三)模仿目标试验
1. 研究设计
2016年有研究者提出模仿目标试验采用RCT的视角设计观察性研究,即基于大样本RWD,模仿良好的目标RCT设计,继而产生RWD的子集,进行因果推断后得出研究结论[16,36]。该研究具体分为两步,即制定目标RCT的研究方案和产生模仿数据及分析结果。
在制定目标RCT的研究方案方面,根据研究所需回答的临床问题,按照RCT规范制定研究方案,即所谓的“目标试验”,其核心要素包括但不限于:入排标准、治疗策略、随机治疗分配、随访期限、随访时间点及时间窗、终点事件及其评价、统计分析计划等。
在产生模仿数据及分析结果方面,根据RCT研究方案,在大样本观察性数据中抽取符合研究方案的数据构成分析数据子集,形成模仿的RCT数据,并基于该子集进行分析,产生因果推断的研究结果。
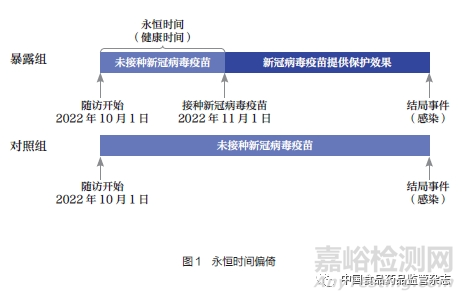
在应用模仿目标试验时,需要特别注意永恒时间偏倚(immortal-time bias)[36]。此类偏倚主要是由随访开始时间与暴露时间不统一导致。在RCT中,受试者通常会在随机入组当天就接受研究药物,因此不会受到此类偏倚的影响。然而在观察性研究中,如果对研究人群采用统一的随访开始时间,可能存在部分研究对象的暴露时间晚于随访开始时间,这段时间内研究对象不会发生结局事件(若发生则不会被纳入分析),因此被称为永恒时间。若将永恒时间纳入分析,很可能会使研究结论产生偏倚。例如,某研究采用观察性数据分析新冠病毒疫苗的保护效果,并将随访开始时间统一设置在2022年10月1日。对于被分配至暴露组的研究对象,如果在接种疫苗前已发生新冠病毒感染,则不会被纳入分析。某研究对象被纳入分析,并在2022年11月1日接种第一针新冠病毒疫苗,被分配至暴露组;但是2022年10月1日至2022年11月1日期间疫苗并不会对其提供保护效果。如果仅通过结局事件(感染)与随访开始的发生时间间隔判断疫苗的保护效果,将会导致错误地认为这1个月的“健康时间”属于疫苗提供的保护效果,最终导致疫苗保护效果被高估(图1)。此外,由于观察性研究无法进行随机化,需要基于较强且无法验证的假设模仿随机化过程[37],因此在模仿目标RCT时需要更加谨慎。
2. 应用实例
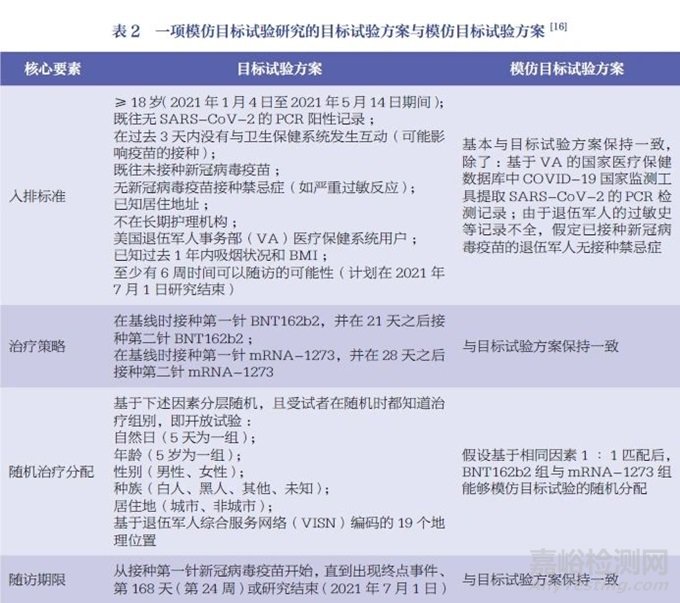
模仿目标试验作为一种新方法,在新冠病毒疫苗RWS中得到了初步应用。2022年有研究者在《新英格兰医学杂志》上发表了模仿目标试验的研究成果:研究者首先假想了目标试验方案,然后基于该方案设计模仿目标试验方案(表2),通过美国退伍军人事务部的国家医疗保健数据库(national health care databases of the department of veterans affair)中BNT162b2和m RNA-1273相关记录,对两款疫苗进行头对头比较,最后得到接种m RNA-1273后的感染风险比BNT162b2更低的结论[16]。此后,又有研究者于2023年基于上述同样的研究思路,对完成上述两款疫苗第三针加强针接种后的数据进行模仿目标试验研究,也得到了相似结论[19]。此外,有研究者对接种了BNT162b2或m RNA-1273后存在多种高危合并疾病的老年人进行评估[18];还有研究者对接种了BNT162b2的儿童(5~11岁)和青少年(12~17岁)进行评估[17],都较好地估计了在模仿目标试验框架下的疫苗保护效果,为评估新冠病毒疫苗在不同场景下的预防感染效果提供了新的证据。
4、挑战与展望
新冠病毒疫苗RWS在回答真实世界环境下的新冠病毒疫苗保护效果方面起到了积极作用,为公共卫生政策决策和监管决策提供了重要依据,但同时也面临着观察性研究在因果推断方面的挑战。
由于观察性研究具有一定的局限性,其研究结论的证据强度不及RCT。病例-对照研究(包括检测阴性设计)是一个从结果到原因的回溯过程,且需要根据研究结局的定义选择研究人群,因此仅能探索关联关系,而不足以做出因果推断。同时,虽然队列研究比较适用于因果推断,但回顾性队列研究通常受限于数据质量,如果缺少某些关键变量,其研究结论的可靠性也会受到挑战。前瞻性队列研究证据强度最高,但也会受到失访等因素的影响,尤其是对大样本的研究人群进行长时间随访。因此,在设计RWS的研究方案时,务必更加谨慎,应尽可能规避观察性研究的局限,以得到更高质量的研究结论。
即使是同类型研究,采用的评价指标、方法、纳入模型的变量也不完全一致,因此研究者难以对不同研究的疫苗保护效果直接进行比较。例如,即便是针对同一类型的疫苗,有研究者基于HR评估疫苗保护效果[22],也有研究者基于IRR和HR进行评估[21]。如何看待不同真实世界场景下疫苗保护效果的差异,也是未来研究中需要正视的问题。另外,鉴于新冠病毒的高变异性,对于既往主流的新冠病毒感染临床评价分析方法需要重新考虑,而这是否会影响目前已有的疫苗保护效果的结论,还需要进一步探索。
无论是监管部门还是学术界,都开始关注RWS与RCT的差异[38-39],包括模仿目标试验方法。该方法可能会受到各类研究假设的影响,尤其是随机分配的相关假设,因此需要辩证看待其结论。此外,对于疫苗RWS,如何构建真实世界环境下合理且完备的估计目标尚需深入研究。
引用本文
陈瑞,吴莹,陈平雁*.新冠病毒疫苗真实世界研究现状及统计学考虑[J].中国食品药品监管,2023(10):32-41.
来源:中国食品药品监管杂志
关键词:
新冠病毒疫苗