嘉峪检测网 2024-08-14 09:10
导读:在上市许可的申请批准前,CDE会与申请人沟通进行生产工艺信息表、质量标准、药品说明书的校对核准,本文分享一些校核时常见的问题或审评关注点,供各位同仁参考。
在上市许可的申请批准前,CDE会与申请人沟通进行生产工艺信息表、质量标准、药品说明书的校对核准,本文分享一些校核时常见的问题或审评关注点,供各位同仁参考。
三证校核建议由生产、质量检验及注册等部门的专业人员进行校核确认。校核时采用修订模式(需批注说明修订原因和理由),完成校核后,建议先与审评员沟通确认,再电子提交修订版本及净版文件。
1、生产工艺信息表
1.格式
(1)最终版本的“流程图”应以图片格式呈现。
(2)字体格式需与中心公布的生产工艺信息表保持一致。一般情况下,标题采用黑体,中文正文采用宋体,西文正文采用Times New Roman。
2.药品上市许可持有人、生产企业、生产地址
确保申请表、药品生产许可证、CPP证书(进口产品)中相关信息(药品上市许可持有人、地址、生产企业、生产地址)一致,并注意确认上述证书均应在有效期内。
关注审评期间企业名称或地址名称等变更情况。生产工艺信息表中的生产地址需具体到厂房/车间、生产线,并需与最新版药品生产许可证、CPP证书(进口产品)等保持一致。如申请表不一致,需告知审评员并提交公文修订申请表中相关内容。
进口产品需关注字母格式错误。
示例如下:
例1:上市许可持有人由广东xxxx有限公司变更为海南xxxx有限公司。
例2:某产品生产地址Straβe,应为StraΒe。
3.批量
需关注数据填写准确性,工艺验证批量应与申报资料保持一致。
4.原辅包、生产企业、执行标准、登记号等
建议在CDE原辅包登记平台查询确认,关注登记号或执行标准数字误写。示例如下:
例1:Y2021xxxx124应为Y2021xxxx142。
例2:“中硼硅玻璃管制注射剂瓶的国家标准YBB00292005-2015”应为“中硼硅玻璃模制注射剂瓶的国家标准YBB00062005-2-2015”。
5.生产工艺流程图
步骤及工艺参数等应与“附件2生产工艺”保持一致;关注洁净区级别标识,应与实际生产一致。示例如下:
例:实际生产区为D级,错误核定为C级。
6.生产工艺
工艺描述应与申报资料、工艺验证及批生产记录等保持一致,需关注易错细节。示例如下:
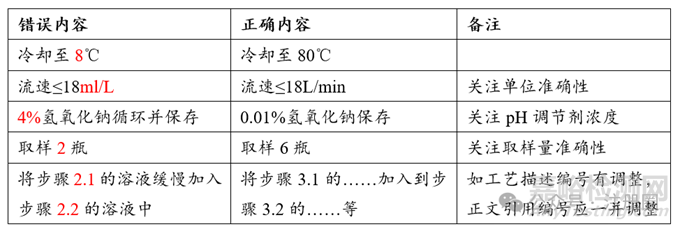
7.主要生产设备
关注设备型号、设备体积、生产商等参数的准确性。示例如下:
例1:“灭菌柜容积20m3”,应为“灭菌柜容积2.0m3”。
例2:设备生产商“广州XX公司”,应为“湖南XX公司”。
8.原辅料内控标准
参照质量标准核定关注点修订该部分内容。
如果原料药内控标准中的方法与制剂方法相同时,需关注限度等差异,避免直接粘贴后出现错误。示例如下:
例:制剂中杂质A≤0.5%,原料药中杂质A≤0.3%。
9.制剂的放行标准
如果放行标准与注册标准一致,只需在该部分写明“放行标准与注册标准一致”,无需进行列表对比。如放行标准与注册标准存在差异,建议进行列表对比,并注意随核定过程中的修订要求进行相应调整。
(1)注意生产工艺信息表中不同部分的相同信息应保持一致,例如某参数调整时,需关注其他出现该参数的部分应一并调整。
(2)如核定的质量标准有调整,“附件7:放行标准”对比表格中的注册标准应一并调整。
2、质量标准
1. 有关物质、含量测定
(1)色谱柱
关注色谱柱信息(类型、柱长、内径等)中常见错误,应与实际验证一致。示例如下:
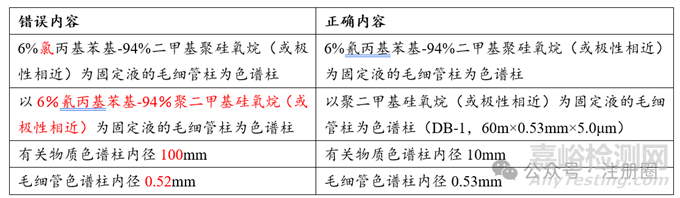
(2)稀释剂或稀释操作
关注稀释溶剂比例或多次稀释操作过程中描述错误。示例如下:
例1:“稀释剂甲醇-水(80:20)”,应为“稀释剂甲醇-水(1:1)”。
例2:“乙醚溶解3次,每次6ml”,应为“乙醚6ml分3次溶解,每次2ml”。
(3)流动相、溶液浓度、进样体积、检测波长等
建议关注数字、小数点、重复数字、数据单位等,示例如下:
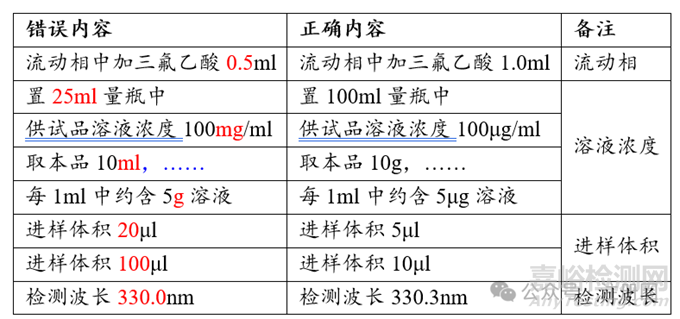
(4)对映异构体
关注对照品溶液或系统适用性溶液配制时采用的对照品是消旋体还是其中一个单体。示例如下:
例:“加流动相溶解并定量稀释制成每1ml约含左氧氟沙星X的溶液”,应该为“加流动相溶解并定量稀释制成每1ml约含氧氟沙星X的溶液”。
(5)系统适用性要求
关注出峰顺序描述,应与典型色谱图及实际检验时出峰顺序保持一致。示例如下:
例:“出峰顺序依次为……、API、杂质C与杂质E”,应该为“出峰顺序依次为……、API、杂质E与杂质C”。
(6)限度
对于以浓度标示的限度,建议关注单位或浓度的小数点,应根据处方浓度仔细计算、核实。示例如下:
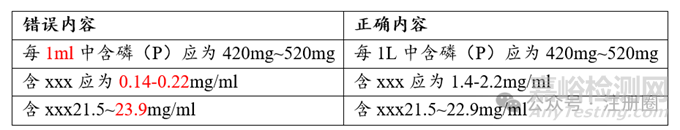
(7)含量限度
关注含量限度的表示方式(按平均装量计、按平均含量计、按干燥品计、按无水物计等),应与计算公式相匹配,并关注分子量折算等。示例如下:

2. 无菌、微生物限度
如涉及,建议关注限度上标、单位、稀释液、冲洗液种类、单次冲洗量与总冲洗量等信息的准确性,需与实际验证方法一致。示例如下:
例1:冲洗液种类“0.1%蛋白胨水溶液”,应为“0.9%无菌氯化钠溶液”。
例2:“103cfu、102cfu”,应为“103cfu和102cfu”。
例3:cuf/ml,应为cfu/g
3. 细菌内毒素
关注限度中的单位。示例如下:
例如:“每1g磷酸氢二钠中含内毒素的量应……”,应为“每1mg磷酸氢二钠中含内毒素的量应……”。
4. 规格
关注规格中分子式,特别是盐与游离碱的转换。示例如下:
例1:“2.0g(按C15H16N7O5S3计)”,应该为“2.0g(按C15H17N7O5S3计)”。
例2:“1mL:5μg”,应为“1ml:5μg”。
5. 复核单位
确认省所名称有无变更,应填写最新信息。
部分一致性评价品种委托检验省所非申请人所在地省所,需关注确认。
示例如下:
例1:“重庆市食品药品检验检测研究院”,应为“四川省药品检验研究院(四川省医药器械检测中心)”。
例2:上市许可持有人为江西省公司,复核省所为山西省食品药品检验所。
6. 附件中的主成分与已知杂质信息
关注主成分与已知杂质化学结构式、分子式的准确性。示例如下:
例:R构型应为S构型,C5H6O2应为C5H6N2。
7. 错别字
关注正文中相似读音错别字导致的错误。示例如下:
例1:“条件pH值”,应为“调节pH值”。
例2:“生产黄色到红色或紫红色的溶液”,应为“生成黄色到红色或紫红色的溶液”。
3、说明书(药学部分)
【成份】、【性状】、【规格】、【贮藏】、【包装】、【有效期】、【上市许可持有人】、【生产企业】等需与质量标准或生产工艺信息表中相同信息保持一致。示例如下:
例:“氯化丁基涂层橡胶塞”,应该为“氯化丁基覆膜橡胶塞”。
4、其它
1. 删除文件中超链接等,避免打印错误。
2. 对于摄氏度(℃)、比旋度(°)等特殊符号,采用全角输入法规范格式,应显示完全。
3. 所提交文件均应为“.docx”格式。
目前审评中心采用office 2016,低于该版本可能造成打印错误或乱码。建议电子提交最终版本文件前,申请人自行打印纸质版,确认有无打印错误。
4. 确保说明书、质量标准、生产工艺信息表、批件中共同信息一致。

来源:注册圈
关键词: 药物生产