嘉峪检测网 2025-02-13 18:35
导读:本文介绍了如何确定医疗器械的基本性能。
为什么您应该关注医疗器械的基本性能?
基本性能是指具有如下特征的器械规格:
如果在预期使用过程中有一项或多项性能未能达到,就会导致患者受伤的风险。
如果您没有定义器械的基本性能,您将无法完全声称符合基本的风险管理ISO 14971的要求。
基本性能可能是一个棘手的概念,事实上,定义不清的基本性能是我们经常在FDA缺陷信中看到的。如果你在早期恰当地定义了你的器械的基本性能,你可以避免以后潜在的问题。
器械基本性能定义
所有医用电气设备的基本性能的识别都源于IEC 60601-1中3.27的定义:

*基本性能指的是临床功能的性能,除了与基本安全性相关的性能,其损失或退化超出了制造商规定的限值,导致不可接受的风险。
这意味着什么呢?设备不能自动工作是否会产生不可接受的风险?什么是基本安全?有什么区别?可以对IEC 60601系列及其与ISO 14971的联系方面去进行高层次的概述来找到答案。
IEC 60601和产品专用系列标准概述
IEC 60601系列为各种电子医疗设备提供基本的安全和基本的性能要求。母标准《IEC 60601-1》规定了产品性能和安全测试期间必须满足的一般要求(如适用)。
附属系列,IEC 60601-1-x文件,阐明了额外的要求,解决没有完全涵盖在IEC 60601-1中的设备特定的特点。这些文档解决了关键问题,例如:EMC测试;警报系统;使用环境——家庭护理和紧急医疗服务;和可用性测试。应该指出的是,虽然不是每个设备都有报警系统,但是每个电子医疗设备都需要进行EMC测试,以确定设备可以在预期的电磁环境中安全有效地工作。FDA最近发布了了一份关于医疗设备电磁兼容性的指南,制造商应参考该文件了解更多信息。
产品特定标准,指的是IEC 60601-2-x和ISO/IEC 80601-2-x系列,是补充母标准IEC 60601-1的设备专用标准。特定标准必须与母标准和附属标准结合使用。
定义基本性能与风险管理的关联
因为定义基本性能与风险管理紧密相关,ISO 14971及其包含的概念至关重要。医疗器械的基本性能由危害分析决定,危害分析是整个风险管理过程的一部分。潜在危险是指那些可能影响临床功能的性能,使该功能的损失超出制造商可接受的限度的危险;基本性能的失效会给患者带来不可接受的风险。应注意,与设备基本安全相关的危险不包括在该定义中;它与制造商确定的性能指标密切相关。
基本安全被定义为“当医用电气设备在正常条件和单一故障条件下使用时,不存在由物理危害直接导致的不可接受的风险”(IEC 60601-1,3.10)。
如何确定设备的基本性能
确定设备的基本性能是应用ISO 14971适用风险管理要求的关键部分。
确定基本性能所需的步骤:
1、确定设备临床功能的性能。
2、规定全功能性能相对于已确定性能的损失或退化的性能极限。
3、评估已确定性能的损失、中断、偏离、降级或超额交付(如危害)的风险。
如果某个性能特征失效没有造成损害的可能性,则该功能不被视为基本性能。如果存在造成伤害的可能性,请参考ISO 14971的附录C和IEC 60601-1的附录A,以获得关于确定潜在危险导致伤害的可能性的指导。只有在一系列事件或其他情况导致危险情况后,危险才会造成伤害。以安装在大容量输液泵上的报警系统为例,它可以降低输液不足或过量的风险。警报系统可以是关于其他潜在危险状态的极好的信息来源。当检测到过量输注时,警报系统通过通知系统发出警报信号,警告临床医生他们的患者需要立即关注并避免潜在的伤害。但是如果报警系统本身发生故障会怎么样呢?输液泵可能会检测到过量输液,但不会发出报警信号,可能会对患者造成严重伤害或死亡!
风险可接受性可以通过估计伤害的概率和伤害的严重性来评估。任何因危险情况而失效并导致伤害的设备功能都可以被视为该设备的基本性能。
IEC 60601和ISO/IEC 80601系列中的器件特定标准也是确定基本性能的良好资源。
除了已经提到的文件之外,还有其他指南文件来帮助制造商了解基本性能和设备特性的概念。
* FDA EMC指南: Electromagnetic Compatibility (EMC) of Medical Devices
* AAMI CR500:2019, Basic Introduction to the IEC 60601 Series
* ISO TR 24971, Medical devices—Guidance on the application of ISO 14971
确定设备基本性能的产品示例 (病人监护仪)
病人监护仪是一种独立设备,集成了测量患者生理参数(如心率、血压和血氧饱和度)的附加组件。典型的病人监护仪将该信息传输到医院的中央监视系统上显示,并且具有警报系统以通知临床医生患者状况的变化。
如前所述,制造商的第一步是首先列出监护仪临床性能功能的所有方面,以便通过风险分析将其作为潜在的危害源进行评估。它们可能是什么?数据显示是一个例子。警报系统是另一个例子。
接下来,对于这些功能中的每一项,您必须确定超过或低于指定性能水平的操作是否会对患者或操作员造成伤害。
使用上面的例子,不能在监护仪上正确地传输或显示数据可能导致病人的重要生理变化被忽视。如果警报系统出现故障,重要的听觉和视觉警报可能不会被触发,这也可能导致患者受伤。
如上所述,如果性能的变化不会导致伤害,则该功能不被视为基本性能。如果变更确实导致损害,不发生损害的操作范围构成基本性能。为了将风险保持在可接受的水平,制造商有义务实施风险控制措施,以减少功能丧失时对患者或操作者的风险。例如,如果断电会导致设备上的报警系统发生故障,从而对患者造成伤害,则制造商可以安装备用电池,以降低断电期间设备功能中断的风险。
幸运的是,在这种情况下,有一个特定的标准可以提供基本性能的附加信息: ANSI/AAMI MP80601-2-49,医用电气设备-第2-49部分:多功能病人监护仪的基本安全和基本性能的特殊要求。
请注意,本文不包括集成到监控单元中的独立单元。ANSI/AAMI MP80601-2-49第201.4.3条增加了IEC 60601-1第4.3条的要求。2-49中的条款在表201.4.3.101(如下)中明确规定了病人监护仪的基本性能要求。

您将看到表中的每一项都有一个相应的条款编号,该编号提供了关于该要求的具体细节。监护仪专用标准(ANSI/AAMI MP80601-2-49)中包含的要求补充了母标准(IEC 60601-1)中的要求,因此在基本性能的确定和测试中使用这两个标准是至关重要的。请记住,一旦定义了基本性能,还需要进行EMC测试。
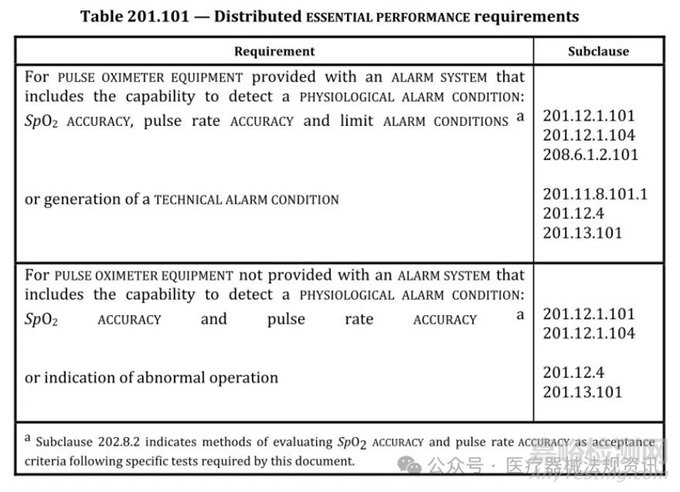
当然,如果没有测量组件,患者监护仪将无法实际监测患者。例如,如果制造商希望增加一个测量脉搏血氧饱和度(SpO2)的附加元件,则需要进行同样的测试来确定基本性能。他们必须确定临床功能,规定性能限制,并评估潜在的危险。在这种情况下,还有一个提供基本性能要求的特殊标准,ISO 80601-2-61,医疗电气设备-第2-61部分:脉搏血氧计设备基本安全和基本性能的特殊要求。该标准还有一个补充IEC 60601-1第4.3条的条款。201.4.3.101条款提供了一个类似于ANSI/AAMI MP80601-2-49中的表格。该部分还增加了一条声明,要求满足文件中列出的所有性能方面的验收标准。这对制造商来说是一条关键信息,因为它让他们知道基本性能的最低可接受水平。这些信息列在哪里?检查2-61子条款201.4.102中的表201.101(如下):
一旦基本性能测试完成,并且采取了适当的风险控制措施以确保基本性能得以维持,制造商就应该对设备的安全性有合理的保证。

来源:医疗器械法规资讯
关键词: 医疗器械