嘉峪检测网 2025-06-05 22:36
导读:建立液相色谱-质谱联用法测定中成药中21种非甾体类抗炎药的含量。样品粉碎研磨后,采用80%甲醇溶液进行超声提取,用C18色谱柱(100 mm×2.1 mm,2.7 μm)分离,以含0.05%甲酸的2 mmol/L乙酸铵溶液、乙腈为流动相,梯度洗脱。在电喷雾离子模式下,采用多反应监测模式进行检测,以外标法进行定量。21种非甾体抗炎药在各自的浓度范围内与色谱峰面积具有良好的线性关系,相关系数
摘 要: 建立液相色谱-质谱联用法测定中成药中21种非甾体类抗炎药的含量。样品粉碎研磨后,采用80%甲醇溶液进行超声提取,用C18色谱柱(100 mm×2.1 mm,2.7 μm)分离,以含0.05%甲酸的2 mmol/L乙酸铵溶液、乙腈为流动相,梯度洗脱。在电喷雾离子模式下,采用多反应监测模式进行检测,以外标法进行定量。21种非甾体抗炎药在各自的浓度范围内与色谱峰面积具有良好的线性关系,相关系数均大于0.990,检出限为0.005~0.16 μg/g。样品加标回收率为87.4%~123.3%,测定结果的相对标准偏差为3.0%~8.0%(n=5)。该方法可用于止痛类中成药中多组分非甾体抗炎药非法添加的测定。
关键词: 液相色谱-质谱联用法; 非法添加; 非甾体类抗炎药; 中成药
非甾体类抗炎药是一类不含有甾体结构的抗炎药,它能够减轻炎症、缓解疼痛并改善关节功能,其常见有布洛芬、吲哚美辛、阿司匹林等药。非甾体类抗炎药药理作用机制主要是通过抑制环氧化酶,减少炎性介质前列腺素的合成,从而产生解热、镇痛、抗炎的作用[1],是世界范围内使用率最高的药物品种之一[2‒3]。若使用不当或者长期过量使用会出现胃肠道损害、肝脏损害等不良反应,对患者的身体健康构成潜在威胁[4‒5]。
近年来,随着中成药的发展以及人们认知的提高,中成药愈发受到广大医生和患者的青睐。然而,与之相伴的是,非法添加问题也日益受到人们的广泛关注,且这种非法添加现象在食品和药品领域均有存在[6‒7]。2023年12月27日市场监管总局办公厅发布了《食品中非法添加非甾体抗炎药物有毒有害的专家认定意见》,认为非法添加非甾体抗炎药具有一定危害。中成药或者含中药的保健食品,因基质复杂、成分较多,所以非法添加的风险较高。基于此,要检测这类基质中的非法添加,就需要灵敏度较高的分析方法,而液相色谱-质谱联用(LC-MS)法恰好符合这一要求,成为较好的选择。潘炜等[8]采用LC-MS法测定了中成药制剂中23种非甾体类抗炎药,检出了吡罗昔康、萘普生等化合物。傅小红等[9]采用LC-MS法对退热贴中13种解热镇痛类化学药物进行了测定。
非甾体类抗炎药种类较多,应用范围较广,一方面用于常见疼痛的短期治疗(如痛经、感冒头痛、牙痛),另一方面用于一些风湿类疾病的长期治疗[10]。之前大部分研究均针对抗风湿类药物[11‒15]的筛查,以糖皮质激素类药物为主,非甾体抗炎药仅占一部分,对于其他止痛类中成药的筛查较少。为有效防控非法添加风险,实现更全面精准检测,笔者将该类筛查较少的化合物(帕瑞昔布、艾瑞昔布、伊索昔康、吲哚洛芬、吡咯布洛芬、卡洛芬)纳入检测范围,建立了一种可对中成药中21种非甾体类抗炎药进行定性、定量检测的方法,适用于止痛类中成药中非甾体类抗炎药的相关检测工作。
1 实验部分
1.1 主要仪器与试剂
液相质谱联用仪:ACQUTTY UPLC H-Class TQ-XS型,美国沃特世公司。电子分析天平:XS205DU型,感量分别为0.01、0.1 mg,瑞士梅特勒-托利多仪器集团。超声波清洗仪:P 300H型,德国艾尔玛公司。超纯水机:Milli-Q IQ 6000型,美国密理博公司。甲醇:色谱纯,美国西格玛奥德里奇公司。乙腈:质谱纯,德国默克公司。甲酸、乙酸铵:均为质谱纯, 赛默飞世尔科技(中国)有限公司。二氟尼柳、美洛昔康、贝诺酯、奥沙普秦、尼美舒利、依托度酸、萘丁美酮、对乙酰氨基酚、氨基比林、安替比林、非那西丁、异丙安替比林、酮洛芬、甲芬那酸、普拉洛芬、艾瑞昔布、帕瑞昔布标准品:纯度(质量分数)均大于99%,中国食品药品检定研究院。伊索昔康、吲哚洛芬、吡咯布洛芬、卡洛芬标准品:纯度(质量分数)均大于98%,上海安谱璀世标准技术服务有限公司。止痛类中成药样品:市场流通样品,适应症包括感冒引起的头痛、月经痛、牙痛、关节痛等。其中胶囊剂13批、颗粒剂9批、片剂17批、丸剂1批。
1.2 仪器工作条件
1.2.1 色谱条件色谱柱:Poroshell 120 SB-C18柱[100 mm×2.1 mm,2.7 μm,安捷伦科技(中国)有限公司];流动相:A相为含0.05%甲酸的2 mmol/L乙酸铵溶液,B相为乙腈,流量为0.3 mL/min;柱温:35 ℃;进样体积:2 μL;梯度洗脱程序见表1。
表1 梯度洗脱程序Tab. 1 Gradient elution program
| 时间/min | 质量分数% | |
| 含0.05%甲酸的2 mmol/L | 乙腈 | |
| 0~2 | 95 | 5 |
| 2~14 | 95~5 | 5~95 |
| 14~16 | 5~95 | 95~5 |
| 16~18 | 95 | 5 |
1.2.2 质谱条件离子源:电喷雾离子源(ESI);检测方式:多反应监测(MRM)模式;扫描方式:正离子模式和负离子模式;毛细管电压:2.0 kV;脱溶剂气温度:400 ℃;脱溶剂气流量:1 000 L/h;离子源温度:150 ℃;进样体积:2 μL,其余质谱参数见表2。
表2 21种化合物质谱参数
Tab. 2 Mass spectrometry parameters of the 21 compounds
| 化合物名称 | 保留时间/min | 质荷比 | 维孔电压/V | 碰撞电压/V | 离子模式 | |
| 母离子 | 子离子 | |||||
| 二氯尼柳 | 9.84 | 249 | 204.9¹,157.1 | 25 | 18,32 | - |
| 美洛昔康 | 9.96 | 352 | 115.0¹,141.0 | 25 | 22,20 | + |
| 贝诺酯 | 9 | 314.1 | 121.1¹,272.1 | 25 | 15,8 | + |
| 奥沙普桑 | 10.43 | 294.1 | 103.1¹,276.1 | 25 | 28,17 | + |
| 尼美舒利 | 10.25 | 307 | 229.1¹,198.1 | 25 | 15,25 | - |
| 依托度酸 | 10.61 | 286 | 242.0¹,212.0 | 30 | 16,23 | - |
| 萘丁美酮 | 10.77 | 229.1 | 171.0¹,128.1 | 25 | 40,15 | + |
| 对乙酰氨基酚 | 2.53 | 152.1 | 152.0¹,110.0 | 30 | 5,15 | + |
| 氨基比林 | 4.51 | 232.1 | 113.0¹,111.1 | 30 | 13,16 | + |
| 安替比林 | 6.27 | 189.1 | 104.0¹,77.1 | 30 | 23,30 | + |
| 非那西丁 | 7.27 | 180.1 | 110.2¹,138.0 | 30 | 20,30 | + |
| 异丙安替比林 | 8.83 | 231.1 | 189.2¹,201.1 | 30 | 19,23 | + |
| 酮洛芬 | 9.58 | 255.1 | 105.0¹,209.0 | 30 | 22,8 | + |
| 甲芬那酸 | 11.57 | 242.1 | 209.0¹,224.0 | 30 | 25,3 | + |
| 普拉洛芬 | 8.31 | 256 | 241.0¹,210.1 | 25 | 30,30 | + |
| 艾瑞昔布 | 10.01 | 370.1 | 278.0¹,236.0 | 25 | 20,30 | + |
| 帕瑞昔布 | 10.21 | 371.1 | 234.1¹,192.1 | 30 | 20,20 | + |
| 伊索昔康 | 9.98 | 336.3 | 99.0¹,209.9 | 20 | + | |
| 吲哚洛芬 | 8.88 | 282 | 218.0¹,236.0 | 20 | 30,25 | + |
| 吡咯布洛芬 | 10.3 | 252.1 | 210.0¹,178.0 | 20 | 15,25 | + |
| 卡洛芬 | 10.52 | 274.2 | 228.0¹,193.0 | 30 | 20,30 | + |
注:1)为定量离子
1.3 实验步骤
1.3.1 标准品溶液配制
21种非甾体类抗炎药标准储备液:精密称取约10.0 mg的21种非甾体类抗炎药标准品,分别置于200 mL容量瓶中,加入5 mL水使美洛昔康溶解,再用甲醇稀释至标线,其余标准品均用甲醇溶解并稀释至标线,摇匀,制得各化合物的质量浓度均为50 μg/mL的标准储备液,于-20 ℃保存。
精密量取10 mL卡洛芬标准储备液,置于100 mL容量瓶中,用甲醇稀释至标线,摇匀,制得质量浓度为5 000 ng/mL的标准溶液A。精密量取1 mL二氟尼柳、美洛昔康、贝诺酯、奥沙普秦、尼美舒利、依托度酸、萘丁美酮、对乙酰氨基酚、氨基比林、安替比林、异丙安替比林、酮洛芬、甲芬那酸、普拉洛芬、艾瑞昔布、帕瑞昔布、伊索昔康、吲哚洛芬、吡咯布洛芬标准储备液,置于同一50 mL的容量瓶中,再用甲醇稀释至标线,摇匀,制得质量浓度均为1 000 ng/mL的混合标准溶液B。精密量取1 mL非那西丁标准储备液,置于100 mL容量瓶中,用甲醇稀释至标线,制得500 ng/mL非那西丁标准中间备液,再精密量取20 mL,置于50 mL容量瓶中,用甲醇稀释至标线,摇匀,制得质量浓度为200 ng/mL的标准溶液C。
准确量取标准溶液A 2 mL、混合标准溶液B 1 mL、标准溶液C 1 mL于同一20 mL容量瓶中,用甲醇或空白基质溶液稀释至标线,摇匀,得21种非甾体类抗炎药混合标准溶液。精密量取上述混合标准溶液1、1、2、4、6 mL,分别置于25、10、10、10、10 mL容量瓶中,用甲醇或空白基质稀释至标线,摇匀,得系列混合标准工作溶液。其中卡洛芬质量浓度分别为20、50、100、200、300、500 ng/mL;非那西丁质量浓度分别为0.4、1、2、4、6、10 ng/mL;其余19种化合物质量浓度均分别为2、5、10、20、30、50 ng/mL。
1.3.2 样品溶液的制备
将止痛类成药片、胶囊、颗粒等制剂粉碎,精密称取1.0 g,置于25 mL容量瓶中,加入20 mL 80%甲醇溶液,摇匀,超声30 min,冷却至室温后,再用80%甲醇溶液定容至标线,静置10 min,精密量取1 mL上清液至10 mL容量瓶中,加入80%甲醇溶液定容至标线,过滤,即得。
1.3.3 空白基质溶液的制备
取样品一份,精密称取1.0 g,置于25 mL容量瓶中,加入20 mL 80%甲醇溶液,摇匀,超声30 min,冷却至室温后,再加入80%甲醇溶液定容至标线,静置10 min,精密量取10 mL上清液至100 mL容量瓶中,加入80%甲醇溶液定容至标线,制得空白基质溶液。
1.3.4 样品测定
在1.2仪器工作条件下,对系列混合标准工作溶液和样品溶液进行测定,得到目标化合物总离子流色谱峰面积,分别以21种化合物的质量浓度为横坐标,对应的色谱峰面积为纵坐标,绘制标准工作曲线,以保留时间和相对丰度比同时定性,采用外标法进行定量。
2 结果与讨论
2.1 提取溶剂选择
非甾体类化合物的结构特征为苯环取代的羧酸结构,均可在甲醇和水中溶解;而大部分中成药的提取工艺采用水提醇沉工艺,因此选择80%甲醇溶液作为提取溶剂,并与无水甲醇作为提取溶剂进行对比,试验发现使用80%甲醇溶液所得的样品溶液中各色谱峰峰形良好且信号稳定。
2.2 质谱条件优化
根据21种非甾体类抗炎药的结构特点,二氟尼柳、依托度酸及尼美舒利选择了电喷雾源负离子模式(ESI-),其余18个化合物采用电喷雾源正离子模式(ESI+),均进行多反应监测方式进行试验。每种化合物均采用标准溶液对质谱参数进行确认,优化锥孔电压及碰撞能量等相关参数,优化后的质谱参数见表2。
2.3 液相色谱条件优化
非甾体类物质一般用反相色谱柱进行分离,常用的色谱柱为C18色谱柱。对比了Agilent proshell SB-C18、Waters BEH C18、Waters HSS T3 C18 3种色谱柱,大部分化合物在液相-质谱可以获得较好的采集,在T3和BEH色谱柱上,部分化合物如吡罗昔康、奥沙普秦峰形较差,因此选用Agilent proshell SB-C18色谱柱。在流动相的选择中,考虑到非甾体化合物的特殊性质,一般需要加入离子对试剂抑制,因此对比了水-乙腈、0.05%甲酸溶液-乙腈、2 mmol/L乙酸铵溶液-乙腈以及含0.05%甲酸的2 mmol/L乙酸铵-乙腈作为流动相对测定结果的影响。试验结果表明,0.05%甲酸的2 mmol/L乙酸铵溶液-乙腈作为流动相,化合物的色谱峰峰形更好,灵敏度更高。
2.4 线性关系、检出限与定量限
在1.2仪器工作条件下,对系列混合标准工作溶液进行测定,以各化合物的质量浓度(x)为横坐标,对应的色谱峰面积为纵坐标,绘制标准工作曲线。通过空白基质标准溶液与甲醇标准溶液评价基质效应(EM),当 EM<0表示基质溶液对目标化合物具有抑制效应,当EM>0表示基质溶液对目标化合物具有增强效应。当 0 ≤ |EM| ≤ 20时,基质溶液对待测物干扰程度较低; 20%< |EM| <50%时基质溶液对待测物干扰程度中等; |EM| ≥ 50%时基质效应干扰强烈。方法检出限(LOD)和定量限(LOQ)均采用信噪比法(S/N)进行计算,LOD满足S/N>3,LOQ满足S/N>10。21种化合物的质量浓度线性范围、相关系数、基质效应、检出限及定量限见表3。
表3 21种化合物质量浓度线性范围、线性方程、相关系数、基质效应、检出限及定量限
Tab. 3 21 compound mass concentration linear range, linear equation, correlation coefficient, matrix effect, detection limit and quantification limit
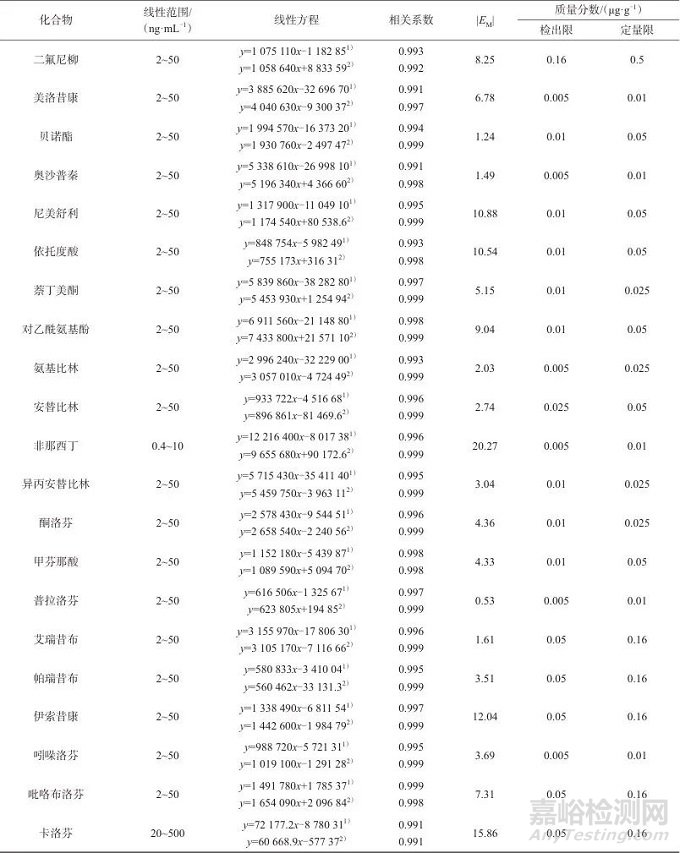
注:1)代表甲醇标准曲线,2)代表基质标准曲线。
由表3可知,20种化合物基质效应干扰较低,非那西丁基质效应较明显,因此使用基质标准工作曲线进行计算。21种非甾体类抗炎药在各自的质量浓度范围内与色谱峰面积具有良好的线性关系,相关系数均大于0.990,检出限为0.005~0.16 μg/g,定量限为0.01~0.5 μg/g。
2.5 样品加标回收试验
采用不含21种化合物的中成药为基质,以2个浓度水平添加标准溶液:(1)低浓度水平:卡洛芬质量浓度为50 ng/mL、非那西丁质量浓度为1 ng/mL,其余19种化合物质量浓度均为5 ng/mL;(2)高浓度水平:卡洛芬质量浓度为200 ng/mL、非那西丁质量浓度为4 ng/mL,其余19种化合物的质量浓度均为20 ng/mL。按照1.4方法进行处理,在1.2仪器工作条件下测定,每个水平平行5份,并计算回收率,试验结果见表4。由表4可知,各组分加标样品的回收率为87.4%~123.3%,测定结果的相对标准偏差为3.0%~8.0%,表明该方法满足测定要求。
表4 加标回收试验结果
Tab. 4 tResults of spiked recycling test
| 名称 | 质量浓度/(ng·mL⁻¹) | 平均回收率% | RSD% | ||
| 加标量 | 测定值 | 平均值 | |||
| 二氟尼柳 | 5 | 5.005, 5.329, 4.832, 5.287, 5.082 | 5.107 | 102.1 | 4 |
| 20 | 20.221, 19.538, 22.998, 20.882, 20.501 | 20.828 | 104.1 | 6.3 | |
| 美洛昔康 | 5 | 5.491, 5.201, 4.779, 4.852, 4.612 | 4.987 | 99.7 | 7.1 |
| 20 | 18.745, 19.799, 22.322, 19.532, 19.382 | 19.956 | 99.8 | 6.9 | |
| 贝诺酯 | 5 | 5.308, 5.330, 4.826, 4.963, 4.679 | 5.021 | 100.4 | 5.8 |
| 20 | 18.453, 18.094, 20.996, 18.538, 17.498 | 18.716 | 93.6 | 7.2 | |
| 奥沙普泰 | 5 | 5.139, 5.292, 4.535, 4.690, 4.505 | 4.832 | 96.6 | 7.5 |
| 20 | 18.775, 19.044, 21.805, 18.579, 18.490 | 19.339 | 96.7 | 7.2 | |
| 尼美舒利 | 5 | 5.676, 5.261, 4.802, 5.187, 4.811 | 5.147 | 102.9 | 7 |
| 20 | 18.084, 18.522, 21.475, 20.100, 18.286 | 19.293 | 96.5 | 7.5 | |
| 依托度酸 | 5 | 5.068, 5.023, 4.635, 5.238, 4.488 | 4.89 | 97.8 | 6.4 |
| 20 | 18.981, 19.213, 22.464, 20.084, 19.461 | 20.041 | 100.2 | 7.1 | |
| 萘丁美酮 | 5 | 4.793, 5.112, 4.467, 4.965, 4.712 | 4.81 | 96.2 | 5.1 |
| 20 | 19.548, 18.987, 22.028, 19.104, 18.575 | 19.648 | 98.2 | 7 | |
| 对乙酰氨基酚 | 5 | 5.005, 5.325, 5.075, 4.798, 4.799 | 5 | 100 | 4.4 |
| 20 | 17.180, 17.109, 19.480, 17.293, 16.361 | 17.485 | 87.4 | 6.7 | |
| 氨基比林 | 5 | 4.925, 5.579, 4.905, 5.080, 4.800 | 5.058 | 101.2 | 6.1 |
| 20 | 18.059, 17.687, 20.375, 18.467, 18.274 | 18.572 | 92.9 | 5.6 | |
| 安替比林 | 5 | 4.932, 5.226, 4.472, 4.749, 4.321 | 4.74 | 94.8 | 7.6 |
| 20 | 18.237, 19.249, 22.011, 19.248, 18.270 | 19.403 | 97 | 7.9 | |
| 非那西丁 | 1 | 0.998, 0.989, 0.948, 0.953, 0.915 | 0.961 | 96.1 | 3.5 |
| 4 | 3.616, 3.499, 4.204, 3.594, 3.776 | 3.738 | 93.4 | 7.5 | |
| 异丙安替比林 | 5 | 4.929, 5.318, 4.919, 4.823, 4.454 | 4.889 | 97.8 | 6.3 |
| 20 | 18.317, 18.410, 21.479, 18.684, 17.860 | 18.95 | 94.8 | 7.6 | |
| 酮洛芬 | 5 | 6.313, 6.320, 6.292, 6.078, 5.812 | 6.163 | 123.3 | 3.6 |
| 20 | 17.535, 17.835, 20.776, 18.185, 17.778 | 18.422 | 92.1 | 7.3 | |
| 甲芬那酸 | 5 | 5.321, 5.372, 4.741, 4.764, 4.760 | 4.992 | 99.8 | 6.5 |
| 20 | 17.385, 17.908, 20.477, 17.510, 17.829 | 18.222 | 91.1 | 7 | |
| 普拉洛芬 | 5 | 5.058, 5.256, 4.928, 4.910, 4.807 | 4.992 | 99.8 | 3.5 |
| 20 | 19.333, 19.049, 22.635, 19.641, 18.700 | 19.872 | 99.4 | 8 | |
| 艾瑞昔布 | 5 | 5.002, 5.052, 4.830, 4.881, 4.452 | 4.843 | 96.8 | 4.9 |
| 20 | 19.221, 19.497, 20.853, 19.605, 18.167 | 19.469 | 97.3 | 4.9 | |
| 帕瑞昔布 | 5 | 5.240, 5.871, 5.529, 5.057, 5.225 | 5.384 | 107.7 | 6.9 |
| 20 | 18.932, 16.919, 19.101, 19.322, 16.776 | 18.21 | 91.1 | 6 | |
| 伊索昔康 | 5 | 5.372, 5.008, 4.694, 4.844, 4.873 | 4.958 | 99.2 | 5.2 |
| 20 | 17.849, 18.385, 20.607, 19.541, 18.403 | 18.957 | 94.8 | 5.9 | |
| 吲哚洛芬 | 5 | 5.575, 5.544, 5.518, 4.632, 5.049 | 5.264 | 105.3 | 7.9 |
| 20 | 18.126, 18.891, 20.860, 18.351, 18.371 | 18.92 | 94.6 | 5.9 | |
| 吡咯布洛芬 | 5 | 4.590, 4.864, 4.711, 4.925, 4.655 | 4.749 | 95 | 3 |
| 20 | 18.885, 18.597, 21.401, 19.738, 19.343 | 19.593 | 98 | 5.6 | |
| 卡洛芬 | 50 | 46.477, 51.027, 49.920, 52.502, 57.462 | 51.478 | 103 | 7.8 |
| 200 | 183.429, 200.102, 194.001, 202.655, 207.812 | 197.6 | 98.8 | 4.7 | |
3 结语
建立了一种止痛类中成药中21种非甾体类抗炎药的检测方法,特别聚焦于此前非法添加风险筛查关注度较低的帕瑞昔布、艾瑞昔布、伊索昔康、吲哚洛芬、吡咯布洛芬、卡洛芬等非甾体化合物。该方法适用于中成药中 21 种非甾体药物非法添加的筛查工作,为药品日常监管提供了可靠的检测手段,有助于提升监管效能,保障公众用药安全。
参考文献
1 王利敏. 非甾体抗炎药不良反应发生表现及预防[J]. 中国伤残医学, 2016, 24(7):181.
WANG Limin. Occurrence and prevention of adverse reactions to non-steroidal anti-inflammatory drugs[J]. Chinese Journalof Trauma and DisabilityMedicine, 2016, 24(7): 181.
2 陈金,马建霞,于晓峰,等.老年人非甾体抗炎药相关性上消化道出血的临床特点[J].中国临床药学杂志, 2020, 29(3): 177.
CHEN Jin,MA Jianxia,YU Xiaofeng,et al. Clinical characteristics of NSAIDs-related upper gastrointestinal bleeding in the elderly[J]. Chinese Journal of Clinical pharmacy, 2020, 29(3): 177.
3 GARCA-RAYADO G,NAVARRO Met al.NSAID induced gastrointestinal damage and designing GI-sparing NSAIDs[J].Ex pert Rev Clin Pharmacol,2018,11(10): 1 031.
4 王丽,于文雯,郭瑞惠,等. 433例非甾体抗炎药物不良反应报告分析[J].中国医药指南, 2024, 22(9): 121.
WANG Li, YU Wenwen, GUO Ruihui, et al. Analysis of 433 reports of adverse reactions to NSAIDs[J]. Guide of China Medicine, 2024,22(9): 121.
5 陈金,姚健凤.非甾体类抗炎药致老年人胃肠道不良反应研究进展[J].中华老年病研究电子杂志,2017,4(4): 22.
CHEN Jin,YAO Jianfeng. Research progress of gastrointestinal adverse reactions caused by non-steroidal anti-inflammatory drugs in the elderly[J]. Chinese Journal of Geriatrics Research,2017,4(4): 22.
6 胡青,孙健,冯睿,等. 超高效液相色谱-三重四极杆质谱法 测定食品中34种非法添加减肥类化合物[J]. 色谱,2017,35(6): 594.
HU Qing,SUN Jian,FENG Rui,et al. Determination of 34 illegally adulterated weight loss compounds in foods by ultra high performance liquid chromatography-triple quadrupole mass spectrometry[J]. Chinese Journal of Chromatography, 2017,35(6): 594.
7 胡青,孙健,于泓,等. 超高效液相色谱-三重四极杆质谱法 测定保健食品中28种降糖类非法添加化合物[J]. 食品安全质量检测学报, 2018, 9(1): 93.
HU Qing,SUN Jian,YU Hong,et al. Determination of 28 anti-diabetic compounds in health foods by ultra performance liquid chromatography-triple quadrupole mass spectrometry[J]. Journal of Food Safety and Quality, 2018, 9(1): 93.
8 潘炜,顾鑫荣,刘志璋,等. LC-MS/MS法测定中成药制剂中23个非甾体抗炎药[J]. 药物分析杂志,2012,32(2): 261.
PAN Wei,GU Xinrong,LIU Zhizhang, et al. LC-MS/MS determination of 23 nonsteroidal anti-inflammatorydrugs in traditional Chinese medicine preparation[J]. Chinese Journal of Pharmaceutical Analysis, 2012, 32(2): 261.
9 傅小红,陈思,姜伟,等. 高效液相色谱-质谱法同时测定退热贴中13种解热镇痛类化学药物[J]. 化学分析计量, 2024, 33(6): 34.
FU Xiaohong, CHEN Si, JIANG Wei, et al. Simultaneous determination of 13 antipyretic and analgesic chemical drugs in antipyretic patches by high-performance liquid chromatography-mass spectrometry[J]. Chemical Analysis and Meterage, 2024, 33(6): 34.
10 AKRAM M,DANIYAL M,SULTANA S,et al. Traditional and modern management strategies for rheumatoid arthritis[J]. Clin Chim Acta,2021, 512: 142.
11 汪元符.抗炎抗风湿功效中成药中非法添加非甾体抗炎药及激素类成分的检测[J].中国执业药师, 2015, 12(11): 19.
WANG Yuanfu. Detection of non-steroidal anti-inflammatory drug and glucocorticoid added illegally in anti-inflammatory and antirheumatic traditional chinese medicine[J]. China Licensed Pharmacist, 2015, 12(11): 19.
12 张亚锋,李卓,董靖,等.高效液相色谱法测定消肿止痛类中成药中16种非法添加糖皮质激素及消炎镇痛类化学成分[J].中南药学, 2019, 17(10): 1 676.
ZHANG Yafeng,LI Zhuo,DONG Jing,et al. HPLC determination of 16 glucocorticoids and anti-inflammatory analgesics illegally added in Chinese traditional patent medicines[J]. Central South Pharmacy, 2019, 17(10): 1 676.
13 言慧洁,刘伟,夏青松,等. UPLC-MS/MS法同时检测抗风湿中药制剂中非法添加的12种非甾体抗炎药[J]. 中国药房, 2017,28(7): 3 871.
YAN Huijie,LIU Wei,XIA Qingsong,et al. Simultaneous detection of 12 non-steroidal anti-inflammatory drugs illegally added in traditional Chinese medicinepreparations for rheumatism by UPLC-MS/MS[J]. China Pharmacy, 2017, 28(7): 3 871.
14 左甜甜,张琳琳,金红宇,等. UPLC-MS/MS检测益心酮片中37个非法添加解热镇痛类化合物[J].药物分析杂志, 2021, 41(10): 1 739.
ZUO Tiantian, ZHANG Linlin, JIN Hongyu, et al. Detection of 37 compoundsillegally added in Yixintong tablets by ultra-high performance liquid chromatography-tandem mass spectrometry [J]. Journal of Pharmaceutical Analysis, 2021, 41(10): 1 739.
15 羊银,刘莹,张瑞华,等. 高效液相色谱-串联质谱法测定保健食品中28种非法添加抗风湿类药物[J]. 职业与健康, 2024(12): 1 612.
YANG Yin, LIU Ying, ZHANG Ruihua, et al. Determination of 28 kinds of illegally added anti-rheumatic drugs in health food by high performance liquid chromatography tandem mass spectrometry method[J]. Occup and Health, 2024(12): 1 612.

来源:化学分析计量
关键词: 液相色谱-质谱联用法 中成药 非甾体类抗炎药