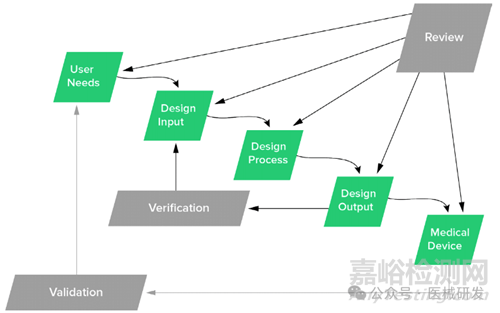
医疗器械研发的流程图里,“用户需求”永远在最前面。(当然,这里只针对已立项的项目,正式立项前其实也是个项目,也是有用户需求的)
多年研发经历,我认为——用户需求这一步,看似简单,其实是整个研发里最容易出问题的地方。
FDA的设计控制指南文件里就明确强调过:设计输入是整个研发的起点,是后面所有工作的地基。
既然提到basis,那就简单比喻一下:如果需求没定准,就像是盖楼时地基打歪了,后面再怎么加钢筋、贴大理石,最后楼还是可能要推倒重来。
以下根据个人经验结合FDA的设计控制指南和六西格玛管理,总结3点经验,分享给大家:Ps:看似官话,却是真话。
1. 把“模糊的感受”翻译成“可验证的指标”
医生常说“要柔顺”“要顺滑”,这些话听上去都对,但如果照单全收,研发根本无从下手。
所以第一步就是翻译。
比如,“柔顺”可以转成最小弯曲半径,或者某个角度下的推送力≤3N。
FDA也提醒过:需求必须清晰、完整,而且能被验证,不能只停留在模糊的形容词上。
2. 用六西格玛思路:从“声音”到“特性”
在六西格玛里,有个很实用的概念叫 CTQ(关键质量特性)。
医疗器械研发完全可以借鉴这个思路。
医生说:“手术要快” → CTQ 就是“操作时间 ≤ X分钟”。
患者说:“恢复要快” → CTQ 就是“术后并发症率 ≤ X%”。
分享常用的流程:
用户之声(VOC) → CTQ → 设计输入。
Ps:这里的用户是指广泛的用户,并非单一指医生主任。
这样,团队既能理解临床的语言,又能落到工程师能执行的指标上。
3. 多角度听,别只听“大咖”
这个坑相信大家可能也踩过。
早年做调研时,我们只找了某主任聊需求,结果产品上线后发现:
主任觉得很好用,但地市医院的年轻医生完全用不顺。另外,即使同是大咖,不同大咖之间的意见也可能也会是相左的。为什么?因为他们关注的细节不一样。
同时,FDA也强调,需求应尽可能覆盖所有用户群体和使用场景。
因此,对于调研,建议:
要有主任,也要有年轻医生
要有一线护士(很多的产品或设备第一步其实是护士操作)
甚至还有患者随访的声音分享一个护士的反馈——说产品的“保护套太难撕开”——让我们发现了一个大问题。
想想看,手术台上护士多浪费几分钟,就完全可能给患者增加风险。
小细节,有时候才是真需求。
研发现场
很多时候,用户需求并不是会议室里聊出来的,而是手术室里蹲出来的,因此,珍惜跟台(包括动物实验)学习的机会,特别是对于新人。
当然,这是临床端暴露出来的,往前的产品开发过程中,需求往往也是在一线中暴露出来的,特别是生产工艺的优化,SOP的编写,只有亲自经历了,才可能会有更好的改进或体会。
分享一次跟台,有听护士到小声说道:“这个包装袋撕起来有点费劲。”
这一句话,似乎没什么大不了,但我认为比厚厚的测试报告更有价值。
我认为:需求不仅是性能参数,还有使用体验。如果连打开包装都不顺手,那就是需求没做好。
Ps:根据GB/T 42061 中 投诉 定义,这本质上就应是1个投诉,那么就应该有投诉处置。
来源:医械研发
关键词:
医疗器械
用户需求