嘉峪检测网 2019-11-21 09:34
导读:医药研发每天最新资讯汇总
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「本文共:17条资讯,阅读时长约:3分钟 」
今日头条
首个国产贝伐珠单抗生物类似药即将获批。齐鲁制药的贝伐珠单抗生物类似药审评状态变更为“在审批”, 这意味着首个国产贝伐珠单抗生物类似药即将获批上市。贝伐珠单抗(安维汀)是一种人源化抗VEGF单克隆抗体,是罗氏旗下的全球首个可广泛用于多种肿瘤的抗血管生成药物,该药于2004年首次获FDA批准上市,目前获批包括结直肠癌、非小细胞肺癌、胶质母细胞瘤、肾细胞癌、宫颈癌、卵巢癌、输卵管癌、腹膜癌等多个实体瘤适应症。贝伐珠单抗2018年全球销售额约为68.49亿瑞士法郎,2017年中国销售额约为15亿元。国内目前仅有原研产品获批上市。
国内药讯
1.恩华药业利培酮分散片首家通过一致性评价。恩华药业利培酮分散片获国家药监局核发的《药品补充申请批件》,成为该品种首家通过一致性评价的药品。利培酮分散片用于治疗急性、慢性精神分裂症和其它各种精神病性状态的明显的阳性症状(如幻觉、幻想、思维紊乱等)、明显的阴性症状(如反应迟钝、情绪淡漠及社交淡漠等);用于减轻与精神分裂症有关的情感症状(如抑郁、负罪感、焦虑);以及用于治疗双相情感障碍的躁狂发作。
2.诺华尼洛替尼第三项适应症在华获批。诺华旗下产品达希纳®(尼洛替尼)新适应症获国家药监局批准,可用于治疗2岁以上儿童慢性髓性白血病。这是继2009年尼洛替尼获批用于治疗既往治疗(包括伊马替尼)耐药或不耐受的费城染色体阳性的慢性髓性白血病(Ph+CML)慢性期或加速期成人患者和2016年获批用于治疗新诊断的费城染色体阳性的慢性髓性白血病(Ph+CML)慢性期成人患者后,在中国获批的又一适应症。据悉,达希纳®是国内二代酪氨酸激酶抑制剂(TKI)药物中唯一用于治疗儿童慢性髓性白血病的药物。
3.诺诚健华奥布替尼提交上市申请。诺诚健华BTK抑制剂奥布替尼(ICP-022)用于治疗复发/难治慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者的新药上市申请获国家药监局受理。据了解,奥布替尼由诺诚健华自主研发,用于治疗多种B细胞恶性肿瘤及自身免疫性疾病,目前正在中美两地开展广泛的临床研究,适应症包括套细胞淋巴瘤(MCL)、边缘区淋巴瘤(MZL)、中枢神经系统淋巴瘤(CNSL)等。此前百济神州的泽布替尼胶囊已获FDA批准上市,国内预计明年获批上市。诺诚健华很有可能是第二家国产BTK抑制剂申报上市。
4.众生药业1类创新药ZSP0678临床新进展。众生药业旗下众生睿创的1类创新药ZSP0678片启动在健康受试者中的I期临床,并完成首例受试者入组和给药。ZSP0678是众生睿创研发的具有明确作用机制和全球自主知识产权的用于治疗非酒精性脂肪性肝炎(NASH)的1类创新药物,也是众生睿创第二个获NMPA批准开展临床的用于治疗NASH的 1类创新药。目前全球尚无获批治疗NASH的上市药物,全球在研处于III期临床的NASH新药有Intercept公司的奥贝胆酸、Genfit公司的GFT-505、艾尔建的CVC和Madrigal公司的MGL-3196。
5.阿斯利康Selumetinib胶囊在华递交临床申请。阿斯利康在研MEK 1/2抑制剂Selumetinib胶囊在国内递交临床申请并获国家药监局受理。这款新药刚刚向FDA递交了新药申请,用于治疗3岁及以上丛状神经纤维瘤相关的无法通过手术治疗的1型神经纤维瘤病(NF1)患者,FDA同时也授予其优先审评资格,FDA给出的PDUFA日期为2020年Q2,如果该药获批,将成为FDA批准的首个用于治疗NF1的口服MEK1/2抑制剂。一项II期临床SPRINT研究显示,selumetinib单药治疗可使NF1患者客观缓解率达到66%。
6.石药2019年前3季度财报发布。石药集团发布2019年前3季度业绩报告。报告显示石药前3季度录得收入167.61亿元,同比增加27.5%;研发投入15.02亿元,较去年同期的9.16亿元同比增长64%。约占成药业务收入的11.2%;销售收入133.87亿元,同比增加35.1%。其中创新药产品(包括恩必普、多美素、津优力、克艾力、艾利能、诺利宁、欧来宁及玄宁)销售收入为95.25亿元,同比增加51.9%;普药产品的销售收入为38.62亿元,同比增加6.0%。
国际药讯
1.辉瑞Humira生物类似药获FDA批准。辉瑞的生物仿制药Abrilada获FDA批准上市,用于Humira获批的各种炎症性疾病。Abrilada是艾伯维阿达木单抗(Humira)的生物类似药,由于专利时间问题,Abrilada将等到2023年11月才能上市销售。一项临床结果显示,治疗26周后,Abrilada治疗组中有68.7%的类风湿关节炎患者达到了ACR20(美国风湿病学会改善20%标准),Humira对照组比例为72.7%,治疗差异为-3.98%,符合±14%的预定范围内。
2.口服前列腺癌新药达到Ⅲ期主要终点。Myovant Sciences公司在研GnRH受体拮抗剂relugolix,在治疗晚期前列腺癌患者的Ⅲ期研究HERO中获积极结果。治疗48周内,96.7%接受relugolix治疗的患者的睾丸激素被持续抑制至去势水平(≤50 ng/dL),达主要终点。治疗组中患者在快速抑制睾丸激素,降低前列腺特异性抗原(PSA)水平等方面,显著优于活性对照组中接受醋酸亮丙瑞林治疗的患者,达关键性次要终点。Myovant Sciences计划于2020年第二季度向FDA递交relugolix的新药申请(NDA)。
3.CRISPR基因编辑疗法临床试验数据积极。CRISPR Therapeutics公司与Vertex 公司宣布CRISPR/Cas9基因编辑疗法CTX001,在正在进行的Ⅰ/Ⅱ期临床试验中取得积极中期数据。1例每年平均需要输血16.5次的输血依赖性β地中海贫血症患者接受CTX001输注后9个月,患者不再依赖输血,总血红蛋白水平为11.9 g/dL,其中胎儿血红蛋白水平为10.1 g/dL。而且血液循环中99.8%的血红细胞表达胎儿血红蛋白。另1例每年平均经历7次血管闭塞性危象(VOC)的严重镰状细胞贫血症患者接受CTX001输注后4个月,患者没有再经历VOC,总血红蛋白水平为11.3 g/dL,也达到停止依赖输血的效果。
4.Orphazyme创新疗法arimoclomol获突破性疗法认定。Orphazyme公司在研药物arimoclomol获FDA授予突破性疗法认定,用于治疗C型尼曼匹克病。Orphazyme公司计划于2020年上半年向FDA递交新药申请。Arimoclomol是一种可穿透血脑屏障的口服小分子热休克应激反应诱导剂。它通过刺激细胞自身的热休克反应在应激细胞中发挥作用,增加HSP70(防止蛋白聚积形成的热休克蛋白)的产生,进而减少脂质的聚积。FDA已授予其孤儿药资格、罕见儿科疾病认定以及快速通道资格。目前,arimoclomol正被开发用于4种罕见病的治疗,包括肌萎缩侧索硬化症、散发性包涵体肌炎、C型尼曼匹克病和戈谢病。
5.赛诺菲三特异性抗体抗癌效果显著。赛诺菲开发的三特异性抗体临床前研究结果积极。该款三特异性抗体不仅能够与多发性骨髓瘤(MM)细胞表面的CD38抗原结合,还能够与T细胞表面的CD3和CD28抗原结合。激活CD28受体能够刺激Bcl-xL蛋白的表达,Bcl-xL可以帮助阻断T细胞凋亡,从而延长T细胞的活性。在体外试验中,与已获批的CD38单克隆抗体daratumumab相比,三特异性抗体裂解的癌细胞比例提高了3-4倍;在多发性骨髓瘤小鼠模型中,这款三特异性抗体也能剂量依赖性缩小移植到小鼠体内肿瘤的大小。
6.2019全球制药公司TOP10发布。国外生物技术网站GEN发布《2019年全球制药公司TOP10》榜单,该榜单根据截至2019年11月13日的市值进行排名。数据显示,2019年TOP10制药公司的总市值是1.792万亿美元,较2018年榜单总市值1.845万亿美元下降2.9%。今年的榜单包括了2018年上榜的全部10家药企,其中5家市值上涨,5家下跌。市值涨幅最大的阿斯利康(+21.3%),其次是默沙东(+11.4%)、葛兰素史克(+9.0%)、赛诺菲(+1.1%)、诺华(+0.3%)。市值跌幅最大的是辉瑞(-18.9%),其次是强生(-10.7%)、礼来(-8.6%)、艾伯维(-4.4%)、罗氏(-1.6%)。
医药热点
1.2019年度何梁何利奖揭晓。何梁何利基金2019年度科学与技术奖评选结果揭晓。35位科技工作者获“科学与技术进步奖”;20位科技工作者获“科学与技术创新奖”。其中,11位获奖科技工作者来自生命科学和医学健康领域。浙大胡海岚、昆明理工大学季维智、上海生科院杨辉分获生命科学奖;上海交大范先群、中科院耿美玉、上海市东方医院刘中民、首都医科大王松灵、黑龙江中医药大学附一院吴效科、中国医学科学院庾石山分获“医学药学奖”;上海生科院刘真获“青年创新奖”;上海微创医疗器械常兆华获“产业创新奖”。
2.诺华上海研发中心或裁员150人。据FierceBiotech网站报道,诺华(中国)生物医学研究中心(CNIBR)战略调整,该中心约有150名工作于早期药物发现领域的研究人员将面临失业。诺华生物医学研究所所长Jay Bradner日前在采访中对CNIBR药物发现工作表示肯定并指出,“我们需要更好地在全球范围内为早期药物开发提供资源,结合中国药物开发和商业化格局的重大变化,诺华已经决定上海中心从药物发现转向早期药物开发。”到2023年,上海研发中心将增加340个开发和商业化的工作岗位,诺华还计划在中国提交50种新药申请。
3.江苏7项举措保“试点扩围”落地。江苏省医保局等9部门联合印发《江苏省推进落实国家组织药品集中采购和使用试点扩大区域范围工作实施方案》,明确今年12月31日前全面执行国家组织药品集中采购和使用“试点扩围”结果;同时提出7项举措,确保政策落地。7项举措为:带量采购,以量换价;招采合一,保证使用;质量优先,保障供应;保证回款,降低交易成本;探索集中采购药品医保支付标准与采购价协同;通过机制转化,促进医疗机构改革;调动医疗机构积极性,确保用量。
4.浙江医疗机构借力区块链推进电子票据改革。11月18日,记者从“浙江省借力区块链技术推进医疗电子票据改革成效新闻发布会”上获悉,截至今年10月底,浙江已有480家医疗机构实行了医疗电子票据改革,累计开票突破1亿张,金额达到417亿元。目前,浙江已成为电子票据改革推进速度最快、开票数量最多、开票金额最大、区块链技术应用最早的省份。医疗收费电子票据即城乡居民在就医过程中取得的“发票”。每年,医疗票据的开具量占财政开具票据(约8亿张)的75%。
【乐普医疗】缬沙坦胶囊首家通过药品一致性评价。
审评动向
1. CDE最新受理情况(11月20日)
2. FDA最新获批情况(北美11月19日)
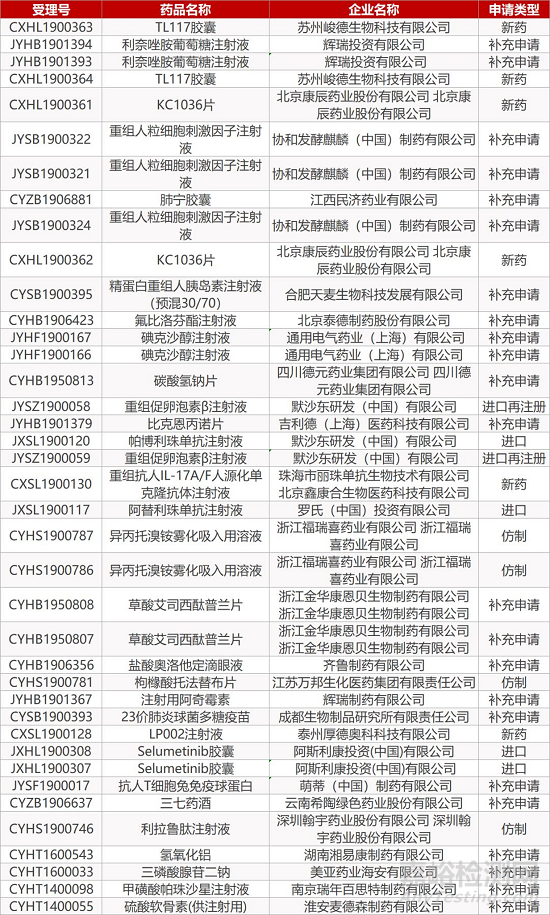
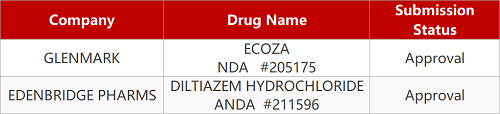

来源:药研发