嘉峪检测网 2022-09-21 11:01
导读:医药研发每天最新资讯汇总
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
苏州瑞博siRNA疗法获批降血脂临床。苏州瑞博1类化药“RBD7022注射液”获国家药监局临床许可,拟定适应症为“以低密度脂蛋白胆固醇(LDL-C)升高为特征的原发性(家族性和非家族性)高胆固醇血症或混合型高脂血症”。RBD7022是一款GalNAc缀合的siRNA药物,可与肝细胞表面的ASGPR特异性结合,并通过抑制PCSK9表达,从而实现降低血液中LDL-C水平的目标。RBD7022也是国产首款针对ASGPR和PCSK9的siRNA疗法获批临床。
国内药讯
1.君实PD-1单抗第6项适应症获批。君实生物PD-1抑制剂特瑞普利单抗获国家药监局批准第六项适应症,联合标准一线化疗用于未经治疗、驱动基因(EGFR/ALK)阴性的晚期非小细胞肺癌。公布在ASCO2022年会上的一项Ⅲ期临床CHOICE-01(NCT03856411)结果显示,与化疗相比,联合治疗可显著延长患者的中位无进展生存期(PFS),降低51%的疾病进展风险,总生存期(OS)亦可得到显著延长(未成熟vs17.1个月),并可降低31%的死亡风险。
2.泰它西普治疗红斑狼疮Ⅲ期临床积极。荣昌生物全球首款BLyS/APRIL双靶点融合蛋白泰它西普(RC18, 泰爱®)治疗系统性红斑狼疮(SLE) 的国内Ⅲ期确证性研究达到预设的临床终点。与安慰剂相比,RC18联合标准治疗显著提高患者第52周SRI-4应答率(82.6%vs38.1%)。泰它西普也显示出良好的安全性。目前RC18用于治疗SLE的国际Ⅲ期临床正在推进当中,并于今年上半年在美国完成首例受试者入组给药。
3.德琪PD-L1/4-1BB双抗获胰腺癌孤儿药资格。德琪医药新型PD-L1/4-1BB双特异性抗体ATG-101获FDA孤儿药资格,用于治疗胰腺癌。ATG-101可阻断免疫抑制性的PD-L1/PD-1结合,同时条件性激活4-1BB共刺激信号,从而激活抗肿瘤免疫效应细胞,在增强药效的同时,提高安全性。该新药目前正在澳大利亚、中国和美国三地同步临床开发,适应症包括晚期实体瘤和非霍奇金淋巴瘤。
4.上海凌达FGFR抑制剂获批临床。凌达生物1类创新药物“RG002片”获国家药监局临床试验默示许可。RG002是一款高选择性的强效不可逆pan-FGFR抑制剂,已在多种FGFR信号通路异常的临床前肿瘤模型中具有显著的抑瘤效果,本次获批的临床适应症为包括但不限于伴有FGF/FGFR基因改变的晚期胆管癌、肝细胞癌、尿路上皮癌等恶性肿瘤。全球范围内,已有三款FGFR抑制剂获批上市,分别为强生的厄达替尼(Balversa)、Incyte公司佩米替尼(Pemazyre)和BridgeBio/Helsinn的英菲格拉替尼(Truseltiq)。
5.大冢PDE4抑制剂在华获批临床。大冢制药Difamilast软膏获国家药监局临床试验默示许可,拟用于治疗儿童及成人特应性皮炎。Difamilast是一款非甾体类外用磷酸二酯酶-4(PDE4)抑制剂,通过阻抑细胞因子和化学介质的产生来发挥其抗炎作用。该药物已于2021年9月获日本厚生劳动省批准上市,作为2岁及以上儿童和成人特应性皮炎的局部疗法。
6.应世引进FIC实体瘤ADC报IND。国家药监局受理了应世生物从Oncomatryx公司引进的抗体偶联药物 (ADC)"OMTX705注射用浓溶液"的临床试验申请(受理号:JXSL2200167)。OMTX705具有新颖的双重作用机制,靶向癌症相关的成纤维细胞和内皮细胞,与抑制微管蛋白聚合和破坏微管稳定性的780 Da细胞毒剂偶联。该新药目前正准备在美国和西班牙针对转移性实体瘤开展I期临床,评估单药或与免疫疗法联合使用的潜力。
国际药讯
1.罗氏VEGF-A/ANG-2眼科双抗获欧盟批准上市。罗氏眼科双抗Faricimab(Vabysmo) 获欧盟批准上市,用于治疗新生血管或湿性年龄相关性黄斑变性(nAMD)和糖尿病黄斑水肿(DME)。Faricimab是首个针对眼科疾病开发的VEGF-A/ANG-2双特异性抗体,已在今年1月获FDA批准上市,用于上市适应症。该新药较anti-VEGF疗法相比,实现减少眼部注射给药频率,每4个月注射1次,改善患者的远期视力结局。
2.辉瑞20价肺炎球菌疫苗Ⅲ期临床积极。辉瑞20价肺炎球菌疫苗(20vPnC)在欧盟婴幼儿中开展的关键性Ⅲ期临床结果积极。婴幼儿在出生后2、4和11~12个月接种20vPnC。结果显示,与活性对照(Prevenar 13)相比,3剂20vPnC接种后一个月,受试者的IgG的平均几何浓度(GMC)在19个血清型中达到非劣效性标准。所有20个血清型表现出强有力的功能性抗体反应。辉瑞计划向欧盟递交上市申请。
3.HER2双抑制疗法获优先审评资格。Seagen公司HER2抑制剂Tukysa(tucatinib)的补充新药申请获FDA授予优先审评资格,与HER2单抗trastuzumab联合治疗HER2阳性、转移性、不可切除结直肠癌(mCRC)经治患者。在一项Ⅱ期MOUNTAINEER临床中,联合治疗达到38.1%的确定客观缓解(95% CI:27.7-49.3),中位DoR为12.4个月(95% CI:8.5-20.5),中位PFS为8.2个月(95% CI:4.2-10.3),中位OS为24.1个月(95% CI:20.3-36.7)。如果获批,它将是FDA批准的首个靶向HER2结直肠癌疗法。
4.GABAA靶向药治疗抑郁症临床积极。Sage公司与渤健开发的新一代GABAA变构调节剂zuranolone(SAGE-217/BIIB125),在用于治疗成人抑郁症(MDD)的SHORELINE试验最新结果积极。数据显示,在那些初始14天对zuranolone(30mg和50mg)产生应答的MDD患者中,必须进行第一次重复疗程的中位间隔时间分别为135与249天。接受zuranolone治疗的患者不需长期每天服药,该新药有潜力成为MDD的发作性治疗药物。
5.NeuroBo引进两款糖尿病领域新药。NeuroBo公司与Dong-A公司就后者两款临床早期、拟用于糖尿病领域新药(DA-1241和DA-1726)达成附条件合作协议。DA-1241是一款新型GPR119激动剂,拟用于降低血糖和血脂水平;DA-1726是一款新型OXM类似物,对GLP-1R和GCGR具有双重激动作用,可起到减少食物摄入并增加能量消耗的作用。根据协议,NeuroBo将获得DA-1241和DA-1726在除某些亚太地区以外的全球开发、监管和商业化权益。
医药热点
1.湖北要求卫生院药师不得少于3人。湖北省卫健委印发《关于贯彻落实〈进一步加强用药安全管理提升合理用药水平〉的通知》,要求发挥药师用药安全的“守门人”作用,乡镇卫生院、社区卫生服务中心药师数不得少于3人;完善药学人员岗位设置,努力使药师薪酬水平不低于医院医师薪酬平均水平;改善药师工作条件,支持药师参加业务培训和继续教育提高专业技能。
2.基石药业前高管王三虎加入贝达药业。据贝达药业官网近日披露,原基石药业的政府及监管事务高级副总裁王三虎先生近日已加盟贝达,担任公司副总裁。根据公开资料,王三虎曾长达11年任职于国家药监局,历任发展规划处处长,办公厅副主任应急管理司司长助理及食品安全监管司副巡视员职位。在进入国家药监局前,王三虎曾担任北京市丰台区卫生局副局长等职位,在公共卫生领域有超过10年的丰富经验。
3.云南对多孩家庭发一次性生育补贴。云南省日前印发《关于优化生育政策促进人口长期均衡发展的实施方案》明确,2023年1月1日至2025年12月31日,将对新出生并户口登记在云南的二孩、三孩分别发放2000元、5000元的一次性生育补贴,并按年度发放800元育儿补助;对新出生并户口登记在云南的婴幼儿购买意外伤害险给予每人每年50元参保补贴。这是三孩生育政策实施以来,全国首个以省为单位发放育儿补贴的政策。
评审动态
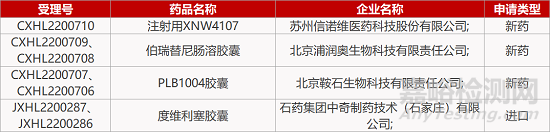
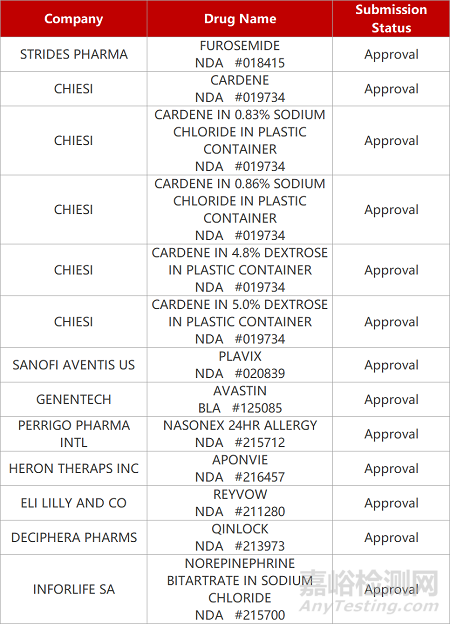

来源:药研发