今日头条
天港医诺中美双报单抗获批IND。天港医诺自主研发的新型免疫检查点单抗药物TGI-5注射液获国家药监局批准开展Ⅰ期临床,拟评估用于不可切除、局部晚期或转移性实体瘤的安全性与有效性。TGI-5能同时恢复NK细胞和T细胞的抗癌免疫功能,已在临床前研究中显示出对肝癌、结直肠癌、黑色素瘤的抗肿瘤活性。去年年底,该新药已在美国获批临床许可。
国内药讯
1.恒瑞2款抗癌药拟纳入突破性品种。恒瑞医药新型PARP抑制剂氟唑帕利胶囊和VEGFR2抑制剂甲磺酸阿帕替尼片获CDE拟纳入突破性治疗品种,适应症为:氟唑帕利单药或联合阿帕替尼治疗gBRCA突变的HER2阴性乳腺癌。此前,氟唑帕利已获批用于治疗gBRCA1/2突变的铂敏感复发性卵巢癌,以及铂类敏感复发性卵巢癌维持治疗。氟唑帕利单药或联合阿帕替尼的多个适应症开发目前正处在Ⅲ期临床阶段。
2.罗氏乳癌抑制剂拟纳入突破性品种。罗氏PI3Kα抑制剂GDC-0077(inavolisib)获CDE拟纳入突破性治疗品种,联合哌柏西利和内分泌疗法治疗PIK3CA突变、HR+/HER2-、局部晚期或转移性乳腺癌成人患者。在Ⅲ期临床(INAVO120)中,与哌柏西利+氟维司群方案相比,inavolisib组合疗法显著提高了无进展生存期(15.0个月vs7.3个月),并将疾病进展或死亡风险降低57%。目前,国内尚无同靶点抑制剂获批上市。
3.石药司美格鲁肽获批IND。石药集团开发的司美格鲁肽注射液获国家药监局临床许可,拟开发用于在减少热量饮食和增加体力活动的基础上对成人超重或肥胖患者的体重管理。此前,该新药已获批准开展成人2型糖尿病患者的血糖控制的新药研究。司美格鲁肽是一种GLP-1类似物,原研产品由诺和诺德开发,已在中国获批用于治疗2型糖尿病。
4.广州赛隽干细胞获批新IND。广州赛隽生物自主研发的CG-BM1异体人骨髓间充质干细胞注射液获国家药监局批准开展用于缺血性脑卒中的新药研究。间充质干细胞(MSC)对多种活性淋巴细胞有免疫调节作用。此前,该产品已有两项IND获批,适应症分别为感染引起的中重度成人急性呼吸窘迫综合征(ARDS)和慢加急性肝衰竭(ACLF)。
5.葆元医药被收购。Nuvation Bio公司与葆元医药达成最终协议,以全股票交易方式收购葆元医药,预计将于2024年第二季度完成收购交易。葆元医药的前股东将持有Nuvation Bio约33%的股份,而Nuvation Bio的现有股东将持有Nuvation Bio约67%的股份。葆元的主要资产他雷替尼是新一代ROS1抑制剂,正在两项Ⅱ期研究中评估治疗ROS1阳性非小细胞肺癌(NSCLC)的潜力,该新药已获得FDA和NMPA授予的突破性疗法认定。
国际药讯
1.口服降脂疗法获批扩展适应症。FDA批准Esperion公司降胆固醇口服疗法Nexletol(bempedoic acid)和口服复方疗法Nexlizet(bempedoic acid/ezetimibe)扩展适应症,作为单药或者与他汀类药物联合使用,用于在一级预防和二级预防群体中降低心血管疾病风险和进一步降低低密度脂蛋白胆固醇(LDL-C);以及单药或联合他汀类药物治疗原发性高脂血症。Bempedoic acid是一款“first-in-class”的ATP柠檬酸裂解酶(ACL)抑制剂,已于2020年获批上市。
2.AZ自免病抑制剂获批新适应症。阿斯利康长效C5补体抑制剂Ultomiris(ravulizumab)获FDA批准新适应症,用于治疗抗水通道蛋白4(AQP4)抗体阳性(Ab+)视神经脊髓炎谱系疾病(NMOSD)成年患者。在III期CHAMPION-NMOSD研究中,中位治疗为73周时,Ultomiris较安慰剂降低了98.6%(p<0.0001)的疾病复发风险。此前,该新药已被FDA批准治疗阵发性睡眠性血红蛋白尿和重症肌无力等多种自身免疫性疾病。
3.俄罗斯药企K药类似药启动Ⅲ期临床。俄罗斯药企R-Pharm生物类似药RPH-75在Clinicaltrials.gov网站上注册了一项Ⅲ期临床,计划入组266例晚期黑色素瘤患者,评估RPH-75与Keytruda对比的治疗效果、药代动力学、安全性和免疫原性。该项试验实际开始日期为2023年9月27日,预计2026年1月完成。值得一提的是,安进生物类似药ABP 234也于近期注册与Keytruda头对头治疗晚期或转移性非鳞状非小细胞肺癌患者的Ⅲ期临床。
4.再生元双抗上市遭拒。再生元CD3/CD20双抗Odronextamab用于治疗复发性或转移性滤泡淋巴瘤(FL)和弥漫大B细胞淋巴瘤(DLBCL)的上市申请收到FDA发出的完全回复函(CRL)。FDA要求确证性临床的入组完成时间必须在递交上市申请前确定。在II期试验中,随访为17.1个月时,该新药在DLBCL患者中ORR和CR分别为53%和37%;在FL患者中,odronextamab的ORR和CR分别为82%和75%。
5.诺和诺德购入一款ASO新药。诺和诺德将以约10.25亿欧元的总交易金额收购Cardior Pharmaceuticals,并获得该公司拟开发用于治疗心力衰竭的反义寡核苷酸疗法(ASO)CDR132L。CDR132L旨在通过选择性降低微RNA分子miR-132的表达水平,中止并部分逆转细胞病理,从而可能促进心脏功能的长期改善。该新药正在Ⅱ期临床HF-REVERT中评估用于治疗射血分数降低型心力衰竭(HFrEF)的潜力。
6.Engrail公司完成B轮融资。Engrail公司宣布完成超额认购的1.57亿美元B轮融资,用于推进其主打项目新型靶向GABAA的正向别构调节剂(PAM)ENX-102开展Ⅱ期临床(ENCalm),评估用于单药治疗广泛性焦虑障碍(GAD)患者的潜力。此轮融资还将继续推动多个临床前研发管线进入临床开发,包括拟开发用于治疗抑郁/快感缺失的ENX-104项目,以及治疗创伤后应激障碍/情绪障碍的ENX-105项目。
医药热点
1. 吴小剑任中大附六院院长。3月25日,山大学附属第六医院召开校管干部会议,宣布学校干部任命决定:任命吴小剑同志为中山大学附属第六医院院长。吴小剑表示,将带领中山六院团队坚守“大专科、强综合”发展模式,秉承“三创三服”文化核心理念,扎实推进研究型医院高质量发展。吴小剑同时担任广东省胃肠病学研究所(中山大学胃肠病学研究所)所长、胃肠肛门外科学部主任,擅长困难的局部晚期和复发性结直肠癌、复杂炎性肠病手术治疗。
2.北京大学国际医院成立特色老年医学中心。3月26日,首都医科大学宣武医院国家老年疾病临床医学研究中心北京大学国际医院分中心正式挂牌,双方共同推动北京大学国际医院特色老年医学中心建设。未来,北京大学国际医院将主动肩负起健康老龄化的使命和任务,加快提高医疗健康供给质量和服务水平,奋力开创医疗健康高质量发展新局面,为积极应对人口老龄化、满足人民群众对美好生活的向往贡献力量,以实际行动展现国家医疗卫生事业生力军的担当作为,助力健康中国战略建设。
3.德国大麻合法化引发巨大争议。德国联邦参议院上周通过大麻合法化法案。根据该法案,从4月1日起,德国18岁以上的成年人可以合法持有最多25克供个人使用的大麻,并可带进允许的公共场所。同时,成年人可在家中最多存放50克大麻、种植最多3株大麻植物。非商业的大麻种植俱乐部将于7月1日合法开放,最多可为500名会员种植大麻并向其分发,每人每月最多50克。德国政府希望采取大麻合法化来遏制大麻黑市交易。然而,多个联邦州对该法案提出猛烈批评。
评审动态
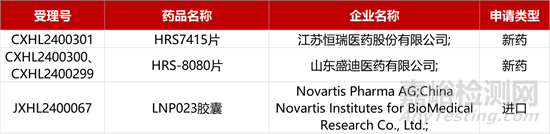
1. CDE新药受理情况(03月25日)
2. FDA新药获批情况(北美03月22日)

来源:药研发
关键词:
药物研发
医药研发
药品研发