嘉峪检测网 2024-11-13 16:53
导读:本文将汇总分析目前已存在尚未被监控机构采纳的皮肤药动学研究方法。
局部皮肤外用制剂的药物从基质中释放,渗透或扩散进皮肤,一定给药时间后在局部发挥抗菌,消炎、镇痛等作用,几乎没有系统循环,体内药代动力学的生物等效性评价方法存在局限性,目前监管机构多数接受以临床为终点的BE评价方法[1],但该方法区分药物制剂之间差异的灵敏度低,评价指标模糊,变异度高,实验所需样本量大,周期长,费用高,不利于局部皮肤外用制剂仿制药的发展;本文将汇总分析目前已存在尚未被监控机构采纳的皮肤药动学研究方法,包括皮肤贴片法、微透析法和共聚焦拉曼光谱法,为后续开发灵敏度高、准确性和重现性好的局部皮肤外用制剂生物等效性评价方法的开发提供思路。
一、皮肤贴片法
皮肤贴片法是用粘性胶带在一定时间内粘取给药部分皮肤的角质层如下图1所示,采用适宜的分析方法测定药物浓度,已得到角质层中完整的药时曲线,通过AUC和Cmax评判等效性;
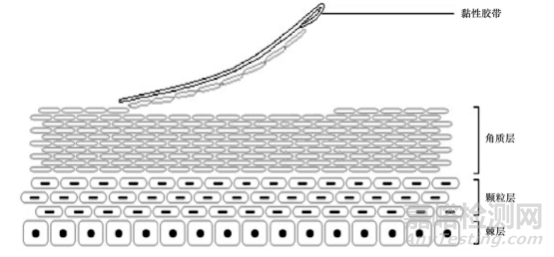
图1 胶带剥离角质层示意图
1998年FDA曾发布局部经皮给药制剂BE指南中包含皮肤贴片法,但不同实验室维A酸凝胶皮肤贴片生物等效性评价产生了截然相反的结果,2002年FDA撤销了指南;皮肤贴片法重现差主要是因为粘去角质层总量无法评判,可进行优化的方法有:1)根据Fick’s第一扩散定律采用经皮水分散失值(TEWL)反映角质层去除程度;2)吸收相结束时,采用彻底的冲洗程序去除未吸收的药物,根据TEWL值的变化确定采集胶带条数,而非FDA之前规定的固定数量的胶带[2];
二、微透析法
微透析法是将探针放置在皮肤中通过微透析泵灌注无菌缓冲液,模拟血管通透性作用,以透析原理实现灌流液与细胞外小分子物质交换,进而可以体内取样,该技术关键问题是如何对取出样品准确校正,即探针回收率测定;回收率准确性影响因素包括体内药物吸收、代谢及蛋白结合的因素,体外灌流速度、灌流组成、半透膜性质、探针位置等;微透析法比较适用于水溶性、小分子物质的采样,新研发的开放式微灌注是探针设计具有开放的交换区域,可以直接采样间质流体,无药物分子大小,蛋白结合和亲脂性限制,如下图2所示,但需要主动推泵,避免灌注液在组织中损失和水肿风险[3]。目前该方法存在缺乏准确易操作的探针回收率校正方法,操作技术要求高,成本高,会对组织造成一定的损伤[4]等问题;
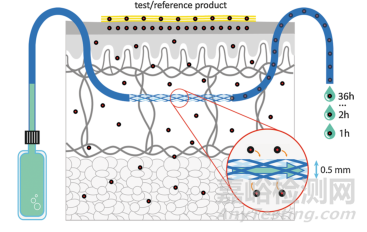
图2 开放式微灌注示意图
三、共聚焦拉曼光谱法
共聚焦拉曼光谱法是一种非侵入性分析内源性皮肤成分的方法,已广泛应用于角质层厚度、角质层水分和经皮促渗剂效果的测定,其原理是激光束通过显微镜聚焦到皮肤上,散射光通过窄阻带过滤波器引导,由同一显微镜聚焦,之后将光聚焦到一根光纤上得到光谱图,其设备组成如下图3所示。共聚焦拉曼光谱法是一种无创、快速、实时监测皮肤药动学研究方法,但只能提供相对药浓度,不能提供绝对药物浓度。
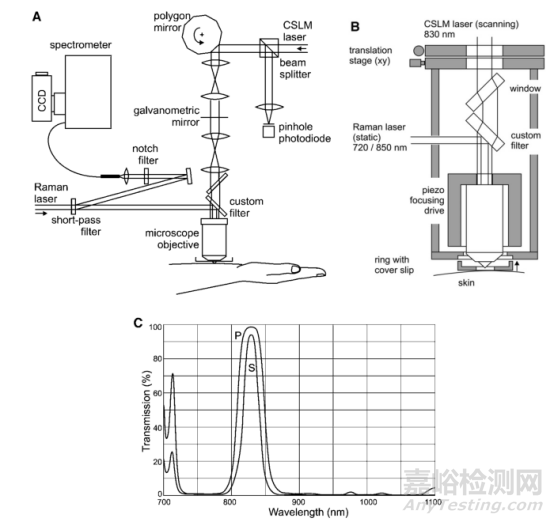
图3 共聚焦拉曼光谱法设备组成情况示意图
四、讨论
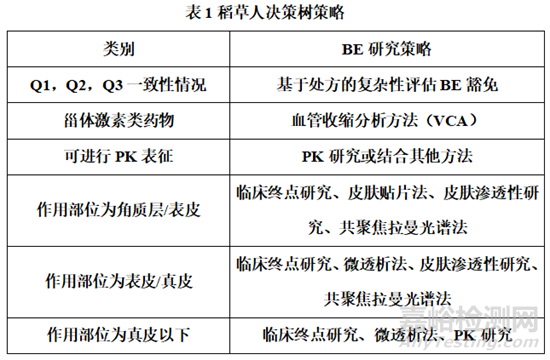
局部皮肤外用制剂的作用靶点在皮肤,体内PK研究往往更多的是反映药物的不良反应,而不是靶点位置药效的药物浓度,采用体内PK研究进行仿制药的BE评价通常是不合适的,需要综合考虑参比制剂处方的复杂性、药物作用机制以及作用靶点等多个方面针对性的进行临床研究设计。为加快局部皮肤外用制剂仿制药的开发,2015年时来自学术界、工业界以及药物监管部门的研究人员鉴于目前局部皮肤外用制剂BE评估方法的局限性,提出了“稻草人决策树(strawman decision tree)”策略[5],从制剂的Q1、Q2、Q3开始考虑,设计BE研究策略,详见下表1。对于目前尚未有BE指南的品种可参考借鉴,结合各方法的优缺点选择多个方法从不同方面进行仿制药和参比制剂的BE评估,从研究成本和仿制药开发方面,各监管机构支持鼓励开发优化皮肤药动学研究方法。
[参考文献]
[1] 陈振. 美国FDA《仿制药开发的个药指导原则》中局部外用药的生物等效性评价方法介绍. [J] . 中国医药工业杂志2022,53(2)
[2] 刘晓琳,丁亮,管宴萍等. 皮肤药动学在经皮给药制剂生物等效性评价中的研究进展. [J]. 中国新药杂志2020,29(23)
[3] BODENLENZ M, TIFFNER KI, RAML R, et al. Open flow microperfusion as a dermal pharmacokinetic approach to evaluate topical bioequivalence. [J]. Clin Pharmacokinet, 2017, 56(1) :91-98
[4] 徐红燕,汤湛,王俏. 微透析在皮肤给药研究中的应用. [J]. 中国新药与临床杂志,2013,32(4)
[5] YACOBI A, SHAH V P, BASHAW E D, et al. Current challenges in bioequivalence,quality, and novel assessment technologies for topical products. [J]. Pharm Res, 2014, 31(4):837 – 846

来源:药研