嘉峪检测网 2024-12-07 14:41
导读:本文介绍皮肤与神经细胞间的作用机制与相关靶标,有助于解决多种皮肤美容问题。
摘 要 / Abstract
人体皮肤与神经系统密切关联,神经纤维与皮肤细胞通过多种神经介质相互交流,从而调节皮肤的各项功能。近年来,美容行业愈发关注神经信号分子与皮肤细胞之间互动的作用机制并致力于寻找神经美容功效成分,以解决各种皮肤问题、改善肌肤健康。本文旨在阐明神经美容科学的理论基础,针对即时祛皱、抗衰老、防脱发、调节色素沉着、舒缓镇静功效阐述各种神经介质对皮肤细胞的影响,梳理神经系统靶标,并介绍了气味分子通过嗅觉受体对皮肤的作用。最后对神经美容学的发展趋势做出展望,期待研发更有效的功能性化妆品,改善皮肤外观与健康。
Human skin is closely related to the nervous system. Nerve fibers and skin cells communicate with each other through a variety of neuromediators to regulate various functions of the skin. In recent years, the beauty industry has increasingly focused on the mechanism of interaction between nerve signaling molecules and skin cells and been committed to finding neurocosmetic ingredients to solve various skin problems and improve skin health. The purpose of this paper is to clarify the theoretical basis of neuroaesthetic science elucidate the effects of various neuromediators on skin cells in terms of instant wrinkle removal, anti-aging, anti-hair loss, regulation of pigmentation, soothing and sedative effects, sort out the nervous system targets, and introduce the effects of odor molecules on skin through olfaction receptors. Finally, the development trend of neuroaesthetics is prospected, and more effective functional cosmetics are expected to improve skin appearance and health.
关 键 词 / Key words
神经美容;神经介质;皮肤细胞;功效;靶标
neurocosmetics; neurotransmitters; skin cells; efficacy; targets
前 言
皮肤由表皮层和真皮层构成,皮肤表面覆盖着毛囊皮脂腺分泌的脂质,真皮层下方为皮下脂肪,主要由脂肪细胞构成。表皮层主要由角质形成细胞组成,表皮的基底层散布着黑色素细胞;朗格汉斯细胞和T 驻留记忆细胞(T resident memory cell,Trm)也存在于表皮。真皮层含有更多样化的细胞类型, 包括成纤维细胞、树突状细胞(dendriticcell,DC)、巨噬细胞、Trm、肥大细胞和Foxp3 T调节细胞[1]。
皮肤的神经支配非常密集,神经末梢可到达表皮上层,但不进入角质层。神经纤维与皮肤细胞之间存在密切接触。神经介质是皮肤与神经系统之间信息交流的介质,可分为小分子神经递质与神经肽,例如神经生长因子(nerve growth factor,NGF)、神经肽P 物质(neuropeptide substance P,SP)、降钙素基因相关肽(calcitonin gene -related peptide,CGRP)、黑色素细胞刺激素(melanocyte stimulating hormone,MSH)、促肾上腺皮质激素(adrenocorticotropic hormone,ACTH)以及脑啡肽、内啡肽、乙酰胆碱等。这些介质不仅能由神经细胞合成, 也可通过皮肤和免疫系统的细胞产生。皮肤细胞和免疫细胞表达这些神经介质的特异性受体,并产生降解介质的酶。神经介质可由物理、化学乃至情绪刺激诱导释放,与受体结合并介导皮肤功能调节,而皮肤细胞也能调节神经元的活动与生长。皮肤、神经与免疫系统共同构成神经免疫皮肤系统(neuro -immuno -cutaneous system,NICS)[2]。不仅如此,皮肤亦具有内分泌功能,可作为多种激素的靶器官并表达各种内分泌受体,而许多激素也在皮肤中合成,例如等效下丘脑 -垂体 -肾上腺(hypothalamic -pituitary -adrenal,HPA)轴调节皮肤应激的适应性反应。由此,皮肤通过与中枢神经、免疫系统及内分泌之间的信息交流维持内部稳态,产生出神经 -免疫 -皮肤 -内分泌网络的概念[3]。
许多皮肤问题,例如光老化、色素异常、敏感刺痛等均与神经介质作用有关,因此,针对神经系统解决皮肤美容问题具有重要的现实意义。一些神经信号分子介导皮肤与神经细胞之间的相互作用,深度影响皮肤的稳态平衡。神经美容护肤品应用于皮肤,对皮肤神经系统发挥各种活性,或调节皮肤信号分子[4]。本文介绍皮肤与神经细胞间的作用机制与相关靶标,有助于解决多种皮肤美容问题。
1、神经系统与即时祛皱
胆碱能神经传递的过程包括乙酰胆碱合成、储存、释放、受体结合,伴随之后的胆碱酯酶降解与循环再利用。阻断胆碱能神经传递的任一环节,都可达到即时祛皱功效,详见图1。胆碱首先通过载体系统从细胞外液转运到胆碱能神经元的细胞质中,在乙酰辅酶A 作用下形成乙酰胆碱,然后进入突触囊泡储存。当动作电位沿神经纤维传导到神经末梢时,突触前膜中的电压门控钙离子通道打开,胞内钙浓度增加,促使突触囊泡与突触前膜融合,释放乙酰胆碱。乙酰胆碱与肌肉纤维上突触后膜离子型烟碱受体(nicotinic acetylcholine receptors,nAChRs)结合,驱动Na+、Ca2+ 电流,导致肌肉收缩[5]。乙酰胆碱酯酶(acetylcholinesterase,AchE)迅速将乙酰胆碱分解为胆碱和乙酸盐,高亲和力运输系统将胆碱回收至神经元[6]。
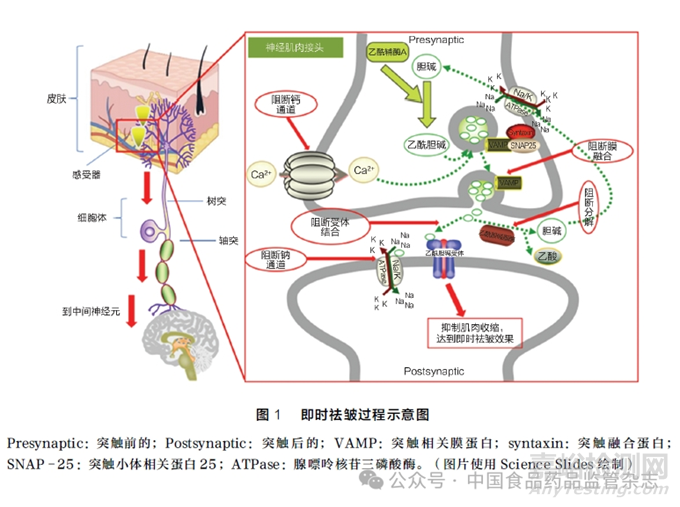
1. 1 电压门控钠离子通道
当乙酰胆碱释放到突触间隙并与突触后膜烟碱受体结合,突触后膜钠离子通道打开,使膜去极化从而传递动作电位。阻断钠离子通道则抑制动作电位形成,抑制肌肉收缩,使得肌肉呈松弛状态。
1. 2 电压门控钙离子通道
当动作电位传导至神经末梢,钙离子通道被激活导致细胞内钙离子内流,促进突触囊泡与细胞膜融合,使乙酰胆碱释放。阻断钙离子通道则抑制囊泡内乙酰胆碱的释放。
1. 3 烟碱型乙酰胆碱受体
乙酰胆碱扩散到突触间隙与突触后膜上的烟碱受体结合,导致一系列信号传递后启动肌肉收缩。抑制乙酰胆碱与nAChRs 结合,则突触后膜无法去极化,抑制肌肉收缩。
1. 4 SNARE 蛋白复合体
可溶性 N -乙基马来酰亚胺敏感因子附着蛋白受体(SNARE) 复合体, 包含突触相关膜蛋白(VAMP)、突触融合蛋白(syntaxin)和突触小体相关蛋白25(SNAP -25)。SNARE 复合蛋白是囊泡膜与突触前膜结合的必要成分,抑制蛋白功能会影响囊泡复合体形成,囊泡膜与突触末梢膜无法融合,乙酰胆碱便难以释放[7]。最终导致动作电位传递障碍,使肌肉去神经支配。
1. 5 乙酰胆碱酯酶
乙酰胆碱酯酶将乙酰胆碱分解为胆碱和乙酸盐,高亲和力运输系统再将胆碱收回神经元内重新利用。抑制乙酰胆碱酯酶活性使得过量乙酰胆碱积累在突触间隙不能被分解并回收,肌肉纤维无法及时去兴奋,最终导致肌肉收缩频率降低,实现肌肉放松。
2、神经系统与抗老化
皮肤神经支配与皮肤主要功能密切相关。皮肤感觉神经起源于背根神经节的细胞体,并形成不同亚型神经末梢,遍布整个真皮层和表皮。感觉神经支配由自由神经末梢和与微粒结构相关的末梢组成,自由神经末梢实时传递外界刺激,包括Aδ 纤维和C 纤维。中等髓鞘的Aδ 纤维遍布真皮,游离无髓鞘C 纤维末端能到达表皮颗粒层[8]。
面部皮肤老化与表皮中神经支配减少相关联[9]。随着年龄增长,面部皮肤表皮神经纤维密度下降,背根神经节神经元数量减少,支配皮肤的有髓鞘和无髓鞘纤维丧失。随年龄增长而产生的神经支配减少与神经营养因子(neurotrophic factors,NTF)合成减少以及神经营养因子受体(neurotrophin receptor,NTR)水平下降有关,这类受体在调节神经细胞生长分化方面起着重要作用,详见图2。内在皮肤老化表现出真皮 -表皮交界处的扁平化,黑色素细胞和朗格汉斯细胞密度降低;真皮层中的细胞外基质丢失与胶原降解,金属蛋白酶水平升高,成纤维细胞和血管网络丧失[10];细胞中丝裂原活化蛋白激酶活性下降,应激相关激酶如p38 和c -jun N 末端激酶(c -jun N -terminal kinase,JNK)活性增加。光老化皮肤中黑色素细胞在基底层分布不均匀,黑色素细胞数量显著增加以及黑色素合成过度活跃导致色素沉着,且光老化皮肤的真皮层中胶原蛋白和弹性纤维表现出退行性变化。神经系统与皮肤相互作用中,多种机制参与了抗老化过程。
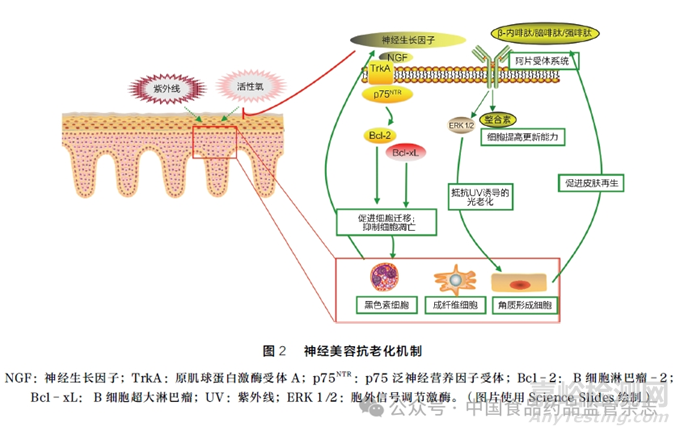
2. 1 神经生长因子保护皮肤细胞抵御凋亡
NGF 是神经营养因子家族成员,该家族还包括脑源性神经营养因子、神经营养因子 -3、神经营养因子 -4 等。NGF 是促进神经元生长发育和功能完整性的重要神经营养因子之一,肥大细胞、脂肪细胞、成纤维细胞、上皮细胞、角质形成细胞和淋巴细胞等多种细胞均可产生NGF 作用于神经细胞。NGF 通过激活两类受体起作用,即原肌球蛋白激酶受体A(tropomyosin receptor kinase A,TrkA)和p75 泛神经营养因子受体(p75 neurotrophin receptor,p75NTR)。NGF 与TrkA 结合,脑源性神经营养因子与原肌球蛋白激酶受体B(tropomyosin receptor kinase B,TrkB)结合,神经营养因子 -3与(tropomyosin receptor kinase C, TrkC) 结合。另一种NGF 低亲和力受体p75NTR 是一种75kD 跨膜糖蛋白,在没有共表达TrkA 情况下激活该受体可以发出细胞死亡信号,导致胞内神经酰胺增加,转录因子核因子 κB(nuclear factor kappa -B,NF - κB)活化,诱导细胞凋亡[11]。
NGF 可促进成纤维细胞迁移速率增加,该作用通过激活TrkA 途径介导[12]。TrkA 是NGF 的高亲和力受体,不仅调节神经元功能,还参与调节其他细胞的迁移和增殖,p75NTR 增强TrkA 对NGF 的亲和力。自分泌NGF 还可以使角质形成细胞免于凋亡。在正常表皮中,基底层的分裂细胞正在经历细胞周期的特定阶段,对细胞凋亡最敏感,TrkA 受体仅在基底角质形成细胞中表达,而增殖的角质形成细胞释放NGF,因此NGF 通过与高亲和力受体作用来抵御凋亡[13]。NGF mRNA 和蛋白质表达在紫外线(ultraviolet,UV)辐射下显著下调,诱导角质形成细胞凋亡,且紫外线照射下调正常角质形成细胞中的TrkA mRNA,但不下调p75NTR。而高水平的内源性NGF 和TrkA 可防止紫外线诱导的角质形成细胞凋亡,抑制人角质形成细胞中的半胱天冬酶活化,从而保护细胞免受UV 损伤。
抗凋亡蛋白Bcl -2 是细胞凋亡调节B 细胞淋巴瘤(B -cell lymphoma,Bcl) -2 蛋白家族成员,可保护多种细胞免于凋亡。NGF 通过Bcl -2 保护细胞,可增强人角质形成细胞中Bcl -2 蛋白水平,而抗NGF 抗体在没有外源性NGF 的情况下显著下调Bcl -2。Bcl -2 蛋白可抑制紫外线诱导的细胞凋亡。紫外线B(ultraviolet radiation B,UVB)下调角质形成细胞中Bcl -2 表达,但过表达NGF 的细胞通过调节Bcl -2 来抵抗细胞凋亡。在正常情况下,NGF在基底层角质形成细胞中维持Bcl -2 水平恒定,Bcl -2 及其同源家族抗凋亡蛋白Bcl -xL 可阻断半胱氨酸天冬氨酸蛋白酶激活[14 -15]。NGF 还能够保护黑色素细胞避免UV 损伤。UV 照射诱导角质形成细胞产生NGF,而NGF 通过上调表皮黑色素细胞中的Bcl -2 蛋白来保护细胞[16]。
TrkA 是一种典型的酪氨酸激酶受体,NGF 通过与TrkA 结合发挥各种作用,能够影响神经元的生长发育与功能,并且有利于皮肤细胞的存活。通过TrkA 可激活多种信号分子,主要涉及丝裂原活化蛋白激酶(mitogen -activated protein kinase,MAPK)、胞外信号调节激酶( extracellular -signal -regulated kinase,ERK)、磷脂酰肌醇3 激酶(phosphoinositide 3 -kinase,PI3K)、蛋白激酶B(protein kinase B,PKB/Akt)途径以及磷脂酶C(phospholipase C,PLC) -γ,从而调节下游通路[11]。
2. 2 阿片受体系统参与对抗皮肤老化
阿片受体系统与皮肤衰老及再生密切关联。阿片受体及其配体是皮肤神经内分泌系统的一部分,主要调节对伤害感受和炎症的反应,在皮肤稳态、再生与伤口愈合中发挥重要作用[17]。内源性阿片系统由μ -阿片受体(mu opioid receptor,MOPr)、δ -阿片受体(delta opioid receptor,DOPr)和κ -阿片受体(kappa opioid receptor,KOPr)以及肽类配体组成,包括内啡肽、脑啡肽、强啡肽和内吗啡肽。阿黑皮质素原( pro - opiomelanocortin,POMC)是一种含有267 个氨基酸残基的蛋白质,裂解产生β -内啡肽、ACTH 以及MSH。POMC及其裂解产物主要在下丘脑和垂体前叶产生,同时皮肤细胞也可产生。皮肤POMC 系统以自分泌方式响应外部或内部应激,显示了阿片受体系统对皮肤的影响,为研究抗衰老产品提供思路[4]。
2. 2. 1 μ -阿片受体系统
内啡肽对MOPr 具有高亲和力,β -内啡肽可抑制通过神经细胞从疼痛源(伤害感受器)到脊髓的传递信号。当内啡肽与阿片受体结合时,大脑产生欣快感。MOPr 在真皮和表皮无髓鞘周围神经纤维上表达,β -内啡肽参与皮肤细胞与周围神经末梢的交流[18]。
MOPr 系统影响角质形成细胞分化、迁移以及细胞因子的产生, 与伤口愈合与皮肤再生过程有关。β -内啡肽结合皮肤细胞表达的MOPr 可加速皮肤再生与伤口愈合。细胞角蛋白(cytokeratin,CK)16 主要在伤口愈合和过度增殖性皮肤病期间的再生上皮细胞中表达。转化生长因子β(transforming growth factor β,TGF -β)II 型受体是一种跨膜丝氨酸/苏氨酸激酶,参与皮肤再生过程。β -内啡肽可上调CK16 和TGF -β II 型受体的表达[17]。慢性伤口边缘β -内啡肽水平较高,使MOPr表达显著降低,长时间暴露于β -内啡肽会促使阿片受体细胞内化。而在正常伤口再生过程中,配体和MOPr 的膜表达水平保持平衡,促进大量CK16 和TGF -β 型II 受体表达[19]。用MOPr 激动剂芬太尼处理大鼠伤口可刺激磷酸血小板衍生生长因子受体(platelet -derived growth factor receptor,PDGFR)-β 以促进再生与伤口闭合[17]。在UVB 照射下,表皮角质形成细胞合成β -内啡肽。有研究发现β -内啡肽通过抑制NF - κB 信号通路来减少UVB照射产生的炎症反应,并逆转UVB 造成的异常表皮增殖分化,从而修复皮肤屏障。该影响是通过阻断Akt/mTOR 信号通路介导的[20]。调节MOPr 表达与活化可促进神经细胞与皮肤细胞间交流平衡,促进再生并改善皮肤外观,靶向针对皮肤衰老问题[4]。
2. 2. 2 δ -阿片受体系统
皮肤细胞与周围神经纤维均表达 δ -阿片受体,DOPr 及其内源性配体脑啡肽调节皮肤细胞增殖分化。皮肤老化可分为内在老化与外在老化,内在老化与个人年龄增长相关,外在老化与光照(主要是UV 照射)、受伤、化学刺激等因素相关。发生内在老化的皮肤表皮层变薄,即表皮细胞收缩与体积减小,屏障功能下降。DOPr 系统促进基底角质形成细胞增殖,DOPr 缺失会导致正常表皮变薄、分化标志物CK10 水平升高,伴随伤口愈合延迟、表皮中CK6 和真皮中胶原IV 过表达[21]。伤口处DOPr 活化可促进角质形成细胞正确迁移并有效闭合伤口,促进再上皮化进程,表明DOPr 系统在控制皮肤稳态过程中具有重要作用[22 -23]。角质形成细胞过表达DOPr 会使得迁移活性增强,这种效应是通过蛋白激酶C 信号通路介导的[24]。DOPr 还可以防止由于UV 照射而导致的外在皮肤老化。UV 照射刺激角质形成细胞释放脑啡肽,介导胞外信号调节激酶(ERK) 1/ 2 信号级联反应,参与对光老化的保护机制[17, 25]。
皮肤老化与表皮干细胞标志物β1 整合素水平降低有关,整合素是一种参与细胞黏附和识别的膜受体,包括组织修复和免疫反应[17]。研究显示表达高水平β1 整合素的细胞具有很高的自我更新能力,而衰老的表皮细胞自我更新能力明显降低[26]。皮肤β1 整合素水平随人体年龄增加而下降,激活DOPr 能够增加β1 整合素在角质形成细胞中的表达[24]。DOPr 激活介导丝裂原活化蛋白激酶信号,特别是与细胞分化、增殖和凋亡相关的ERK 1/ 2。DOPr 介导的ERK 1/ 2 信号传导由PLC 作为媒介,将DOPr 与整合素偶联,进一步导致受体酪氨酸激酶(receptor tyrosine kinases, RTKs) 活化,RTKs 最终激活ERK 1/ 2[27]。
2. 2. 3 脑啡肽酶
压力应激会加速皮肤老化与稳态失衡。脑啡肽可缓解压力影响,但会被脑啡肽酶迅速降解[28 -29]。抑制脑啡肽酶活性可维持脑啡肽浓度,缓解皮肤压力并对抗皱纹等[4]。此外,重复的紫外线A(ultraviolet radiation A,UVA)照射会刺激角质形成细胞分泌白介素(interleukin,IL) -1α 等炎症因子,渗透到真皮层上调成纤维细胞脑啡肽酶表达,且成纤维细胞的直接UVA 暴露也会导致脑啡肽酶表达增加,切割弹性纤维,导致弹性纤维网络破坏,皮肤弹性丧失、产生皱纹与松弛[30]。抑制脑啡肽酶活性可保护真皮层弹性网络,维持皮肤弹性,对抗皮肤松弛老化。
2. 3 神经保护实现对抗皮肤老化
神经元细胞衰老的过程被称为神经退行性变,该过程主要由具有神经毒性的 β -淀粉样蛋白(amyloidβ-protein,Aβ )形成神经末梢表面老年斑块的作用介导,而Aβ 由可溶性淀粉样前体蛋白(soluble amyloid precursor protein, sAPP) 裂解产生[31]。淀粉样前体蛋白(amyloid precursor protein,APP)裂解分为两种途径,淀粉样蛋白切割途径由β 分泌酶作用产生神经毒性Aβ ,非淀粉样蛋白生成途径在α 分泌酶促下产生具有神经保护性的神经营养因子sAPPα 肽[32]。在正常神经元中这两种裂解途径处于动态平衡,但神经元老化与氧化应激导致Aβ 逐渐增多,加剧神经元衰老。神经元衰老会影响神经纤维与成纤维细胞之间的信息交流,降低成纤维细胞的活力,从而抑制真皮胶原蛋白和弹性蛋白含量,导致皮肤老化。增加sAPPα 肽水平可保护神经元免受神经退行性变,建立神经与成纤维细胞间的正常交流,从而激活胶原与弹性蛋白合成[4]。
2. 4 降低皮质醇对抗皮肤老化
皮质醇主要源于肾上腺皮质, 通过响应下丘脑 -垂体 -肾上腺(HPA)轴激活产生,并与糖皮质激素受体结合起作用[33]。下丘脑神经元会分泌促肾上腺皮质激素释放激素(corticotropin releasing hormone, CRH), 皮肤细胞也可产生CRH、ACTH 及各种受体,组成功能齐全的外周HPA 轴。压力应激促使CRH 释放诱导皮肤细胞产生皮质醇,破坏皮肤稳态、降低屏障功能以及诱发炎症等[34]。UV 照射或情绪压力等应激上调11β -羟基类固醇脱氢酶1 型(11β -hydroxysteroid dehydrogenase type 1,11β -HSD1)的表达,11β -HSD1 将无活性可的松转化为生物活性皮质醇,导致角质形成细胞生长抑制、基质金属蛋白酶活化、NF - κB 激活等,使皮肤伤口愈合延迟、胶原蛋白含量下降、促炎细胞因子释放以及活性氧(reactive oxygen species,ROS)水平升高并引起氧化应激[35]。阻断11β -HSD1 活性可帮助皮肤平衡皮质醇水平,提高真皮胶原蛋白合成、增强屏障功能,恢复稳态并抵抗皮肤衰老[4,36]。降低皮质醇对抗皮肤老化过程详见图3。
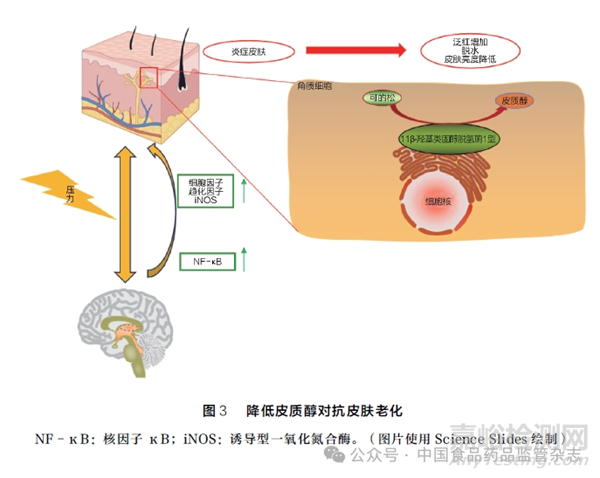
2. 5 皮肤褪黑素能系统具有抗氧化益处
人体皮肤和中枢神经系统拥有共同的胚胎起源,因此共享多种神经介质。皮肤中也存在一个褪黑素能系统,具有抗氧化防御功能,可维持皮肤稳态平衡[ 37]。在毛囊角质形成细胞和真皮成纤维细胞等表皮部位可检测到褪黑素受体1(melatonin receptor 1,MT1)的基因。此外皮肤细胞中存在核受体类维A 酸受体相关孤儿受体 -α(retinoid acid receptor -related orphan receptor -α,RORα)[40]。褪黑激素是有效的活性氧清除剂,可抵御UV 等因素引起的氧化应激,上调皮肤中过氧化氢酶、超氧化物歧化酶等抗氧化酶活性,保护角质形成细胞DNA 免受损伤,并防止线粒体膜电位降低和膜脂质过氧化等[38 -39]。褪黑素及其受体表达水平随年龄增长而下降,从而削弱皮肤抗氧化能力,打乱皮肤细胞的昼夜节律并增加氧化应激积累[41]。在皮肤局部应用褪黑激素或其衍生物可激活褪黑素受体表达,清除自由基, 抗细胞凋亡并保持线粒体功能,具有抗衰老功效[4]。皮肤褪黑素能系统被认为是对UV 照射的有效防御,可减少皮肤粗糙与皱纹等现象,改善皮肤老化外观[40]。
3、神经系统与防脱发
脱发是一个严重的美容问题,神经肽及其受体都对脱发有着不容忽视的作用,例如神经肽P 物质或p75NTR 水平升高都会促使毛囊凋亡。调节神经肽P 物质或神经营养因子受体的活性可作为防脱发策略,详见图4。
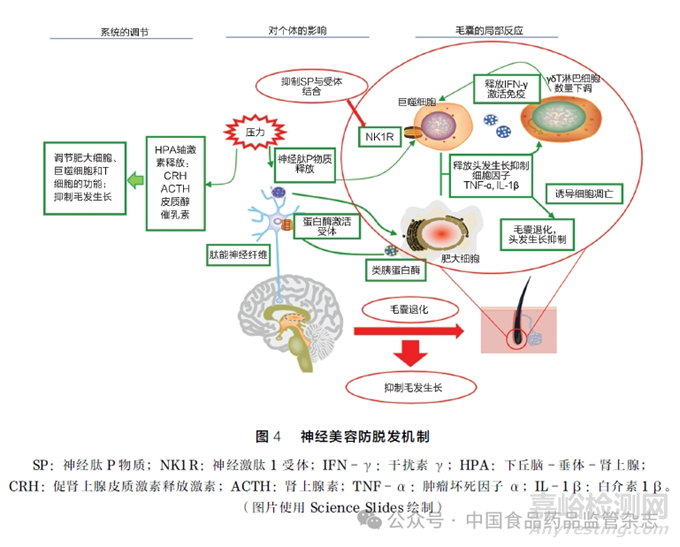
3. 1 抑制神经肽P 物质作用减少毛囊凋亡
毛囊(hair follicle,HF)是皮肤上的一种微型器官。通过控制毛发周期的休止期、生长期、退行期三个阶段能够调节毛囊干细胞生长发育过程[42]。在神经内分泌 -免疫相互作用中,压力应激会改变免疫反应,而免疫细胞及免疫调节因子都显著影响毛囊活性与毛发生长周期。压力应激会抑制毛发生长并导致毛囊退化[43]。许多患者在遭遇重大压力后出现斑秃症状,而斑秃是一种自身免疫性疾病,与毛囊周围神经纤维中丰富的SP 表达有关[44]。中枢应激反应可激活HPA 轴, 沿该轴释放的CRH、ACTH 和糖皮质激素等均有抑制毛发生长作用。中枢应激刺激肽能神经纤维分泌SP,激活SP 受体,诱导毛囊凋亡,并使退行期毛囊数量增多;肥大细胞分泌的蛋白酶(如类胰蛋白酶)可进一步激活肽能神经纤维上的蛋白酶激活受体(protease activated receptors,PARs),通过正反馈触发额外神经肽释放,随后通过毛囊的免疫细胞分泌炎性细胞因子(如TNF -α、IL -1β)抑制头发生长;毛囊周围巨噬细胞浸润会攻击毛囊干细胞, 破坏其再生能力[43]。因此,针对神经因素,抑制神经肽P 物质的作用可作为一种防脱发策略。
神经激肽1(Neurokinin 1,NK1)受体为毛囊干细胞上的神经肽P 物质受体,抑制NK1 受体可保护毛囊,具有治脱发的潜力[45]。压力应激诱导神经纤维分泌SP,激活NK1 受体,使巨噬细胞、γδT 细胞和肥大细胞产生炎性细胞因子,抑制毛囊中的角质形成细胞增殖并诱导细胞凋亡,毛囊过早消退导致脱发。而NK1 受体拮抗剂可以消除这种应激反应,保护毛囊并具有治脱发的潜力[43]。
3. 2 调节NGF 受体减少毛囊凋亡
神经营养因子家族参与调控毛发生长周期。神经营养因子可诱导毛囊中角质形成细胞凋亡并驱动毛囊退化,造成脱发,这种效应是由NGF 前体pro -NGF 与p75NTR 结合产生的。只有当p75NTR 单独表达时才会引发促凋亡信号,因此神经营养因子对细胞凋亡的作用依赖于p75NTR 与TrkA 受体在靶细胞上的相对表达量[46]。NGF 是毛发生长过程的关键调节剂。神经肽P 物质能够下调促生长的TrkA 免疫反应性,上调NGF 以及p75NTR [47]。抑制p75NTR或激活TrkA 信号传导可作为防脱生发的潜在方案。
p75NTR 在毛囊生长期到退行期的过渡期间呈现高稳态表达水平,加速退行期发展,干预p75NTR 信号可治疗由于过早进入退行期而导致的毛发生长障碍。pro -NGF/NGF 能够诱导TGF -β2 表达上调,激活远端毛囊上皮中半胱天冬酶3 和9,导致上皮细胞凋亡[48]。毛囊中仅表达p75NTR 而不表达Trk受体的细胞群是p75NTR 介导的细胞凋亡的靶标[46]。TrkA 在毛囊黑色素细胞和角质形成细胞中表达,调节增殖、分化和凋亡, 有利于头发生长和色素沉着[49]。利用p75NTR 拮抗剂可抑制毛囊退行期的过度发展,而激活TrkA 有利于头发生长。
4、神经系统调节皮肤色素沉着
皮肤黑色素生成由许多与神经系统有关的信号分子和转录因子调节,详见图5。黑色素细胞存活与色素生成的重要调节因子是黑色素生成相关转录因子( microphthalmia - associated transcription factor,MITF),该因子调节黑色素生成相关蛋白的表达,如酪氨酸酶(tyrosinase,TYR)、酪氨酸酶相关蛋白1(tyrosine -related protein -1,TRP -1)和多巴色素异构酶,也称为酪氨酸酶相关蛋白2(tyrosine -related protein -2,TRP -2)。MITF 还调节其他转录因子以控制黑素母细胞和黑色素细胞增殖、分化以及黑色素体运输[50]。几种不同的信号通路调节MITF 表达,包括环磷酸腺苷(cyclic adenosine monophosphate,cAMP)/蛋白激酶A(protein kinase A, PKA) 通路、干细胞因子(stem cell factor,SCF)/c -kit 通路以及Wnt/β -catenin 通路。神经激素α -MSH 和ACTH 是由POMC 水解产生的黑皮质素肽,与黑皮质素 -1 受体(melanocortin receptor type 1,MC -1R)结合激活腺苷酸环化酶,催化二级信使cAMP 水平增加,可激活PKA 使cAMP 反应元件结合蛋白(cAMP - response element binding protein,CREB)磷酸化,并进一步调节下游基因。磷酸化CREB 诱导MITF 表达, 刺激TYR、TRP - 1 和TRP -2 生成,最终合成黑色素[51]。
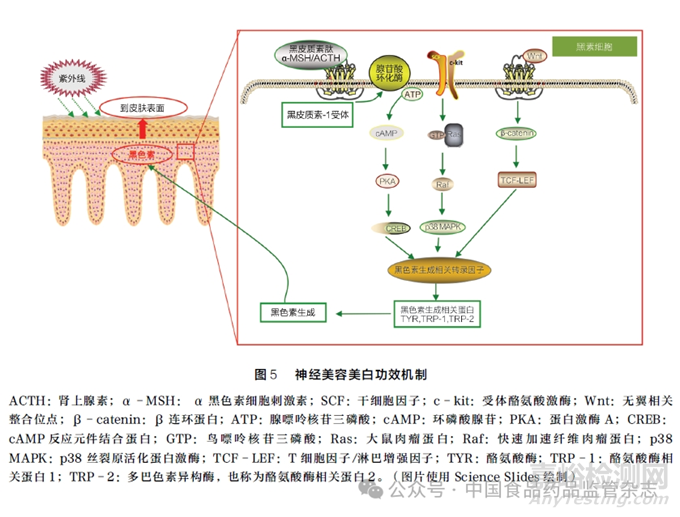
黑素细胞内合成黑色素的细胞器称为黑色素体,影响皮肤色素沉着的蛋白大多位于黑色素体,多种酶合作产生真黑素与褐黑素。黑色素体通过黑色素细胞树突结构从核周区域向角质形成细胞内转移,最终形成色素沉积[52]。皮肤神经支配与色素沉着相关联。黑素细胞起源于神经嵴,与神经纤维存在密切接触。肿瘤抑制蛋白p53 调节角质形成细胞POMC 表达,POMC 转录激活后通过旁分泌促进黑色素合成,造成皮肤色素沉着[53]。紫外线、炎症等因素会触发p53 上调POMC,而抑制POMC 表达可阻止黑色素过量产生[4]。
4. 1 黑皮质素-1 受体(MC -1R)
MC -1R 是G 蛋白偶联受体A 类家族成员,是调节黑色素细胞功能的主要受体。两种黑皮质素肽α -MSH 和ACTH 是MC -1R 的内源性激动剂,通过活化cAMP/PKA 信号通路调节下游基因,诱导MITF 转录,最终使黑色素合成增加并转移到表皮中的角质形成细胞[50]。α -MSH 是调控黑色素生成的关键激素,与受体结合增加酪氨酸酶活性、促进真黑素产生, 导致肤色变黑[54]。抑制α - MSH 或ACTH 与MC -1R 的作用可减少皮肤色素沉积。
4. 2 肾上腺素能受体
人表皮黑色素细胞表达β2 -肾上腺素能受体(β2 -adrenergic receptor,β2 -AR), 角质形成细胞响应UVB 照射释放肾上腺素,通过旁分泌作用刺激β2 -AR,导致cAMP 信号产生和黑色素生成增加。使用β2 -AR 拮抗剂可阻断紫外线诱导的黑色素生成[55 -57]。因此,抑制β2 -AR 可能具有皮肤美白功效。
4. 3 谷氨酰胺能受体
谷氨酸是中枢神经系统的兴奋性神经递质,在表皮中也具有重要功能。MITF 是黑色素合成相关酶的转录调节因子, 在黑色素生成中具有关键作用。阻断黑色素细胞上的离子型谷氨酰胺能受体会下调MITF 蛋白表达,使黑色素细胞形态变化、树突回缩[58]。此外,代谢型与离子型谷氨酸受体拮抗剂能够抑制黑色素瘤细胞增殖和迁移[59]。因此谷氨酰胺能受体可作为皮肤美白成分的靶标之一[55]。
5、神经系统与舒缓镇静
敏感皮肤(sensetive skin,SS)是指皮肤的神经反应性过于敏感、耐受性较差,容易受外界刺激而产生刺痛、灼热、瘙痒等不适感,可能伴有红斑、红肿等症状,主要发生在面部[60]。这些不良反应与皮肤中瞬时受体电位(transient receptor potential,TRP)型受体密切相关。TRP 不仅表达于神经细胞, 在非神经细胞中也存在, 如成纤维细胞、角质形成细胞、黑素细胞及肥大细胞等。TRP通道激活后引起SP、CGRP 等神经肽释放,诱导其他促炎介质扩散(如IL -1α、TNF -α),可引起皮肤神经源性炎症[61],详见图6。
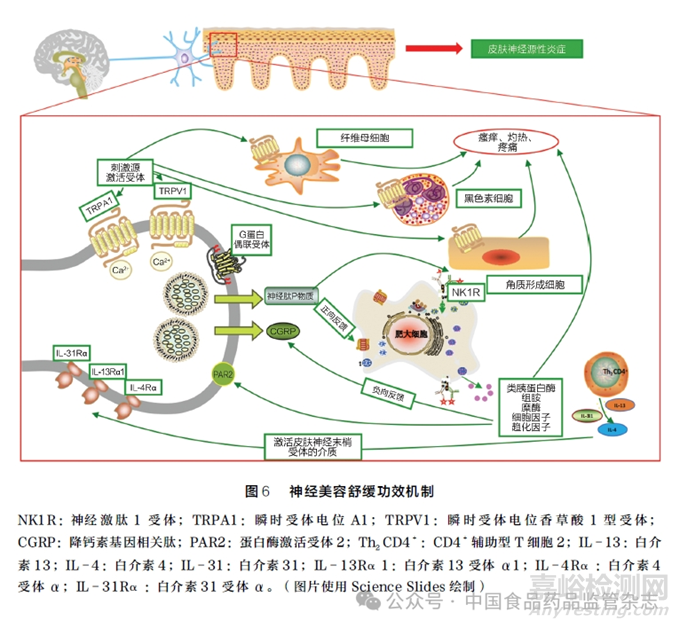
5. 1 瞬时受体电位离子通道亚家族V 成员1 介导皮肤敏感
瞬时受体电位离子通道亚家族V 成员1(transient receptor potential vanilloid 1,TRPV1)是非选择性阳离子通道家族成员,在各种刺激引起的疼痛热转导中起到重要作用,也参与瘙痒传导。该受体在神经细胞、角质形成细胞、成纤维细胞等细胞中均有表达,通过香草结合位点激活。在不同刺激源(如热量、低pH 值、紫外线以及某些化合物)作用下,该受体打开跨膜阳离子通道使Ca2+流入细胞内激活信号通路,引起神经介质释放,诱导疼痛、瘙痒与炎症反应等[62]。角质形成细胞也可感知外界刺激并与感觉神经元快速通讯,充当环境与表皮内神经纤维的中介, 传导疼痛、红肿等伤害性反应[63]。敏感皮肤产生的高度神经反应往往是由于TRPV1 受体表达水平过高或是激活阈值较低[4, 64]。针对神经源性皮肤敏感,可通过抑制TRPV1 表达或拮抗受体功能来增强皮肤耐受性,舒缓面部不适感。
5. 2 瞬时受体电位M8 镇静敏感皮肤
感觉神经元能够通过温度敏感TRP 通道感知外界温度变化,其中瞬时受体电位M8(transient receptor potential melastatin 8, TRPM8) 是一种多模态活化冷敏离子通道, 可通过低温(15 ~28℃)、电压变化、薄荷醇等因素激活,促使钙离子渗透[65]。冷却活性成分作用于感觉神经上的TRPM8,可以为皮肤提供清凉感,缓解敏感肌肤受刺激后产生的灼热不适感[66]。
6、气味分子调节皮肤
在20 世纪初,芳香疗法首次被定义为一种医学治疗方法,近年来对其作用机制研究越来越多。芳香疗法最初用于缓解压力、改善情绪,且近年来越来越多的研究表明气味分子亦具有调节皮肤状态的功能。嗅觉信号通过鼻嗅觉感受器进入嗅球,然后分别进入大脑皮层与下丘脑,可以直接或间接调节生理功能[67],详见图7。芳香疗法使用的精油等制剂含有与中枢神经系统相互作用的化学成分,如柠檬烯、芳樟醇、香叶醇和香茅醇[68 -69]。芳香气味分子通过鼻脑通道刺激大脑产生神经递质(如血清素、内啡肽)或降低皮质醇水平,并调节多巴胺、Ach、GABA 和 N -甲基 -D -天冬氨酸(NMDA)受体的表达,有助于缓解疼痛、改善焦虑抑郁、提高睡眠质量, 从而直接或间接地调节皮肤状态[ 68, 70]。
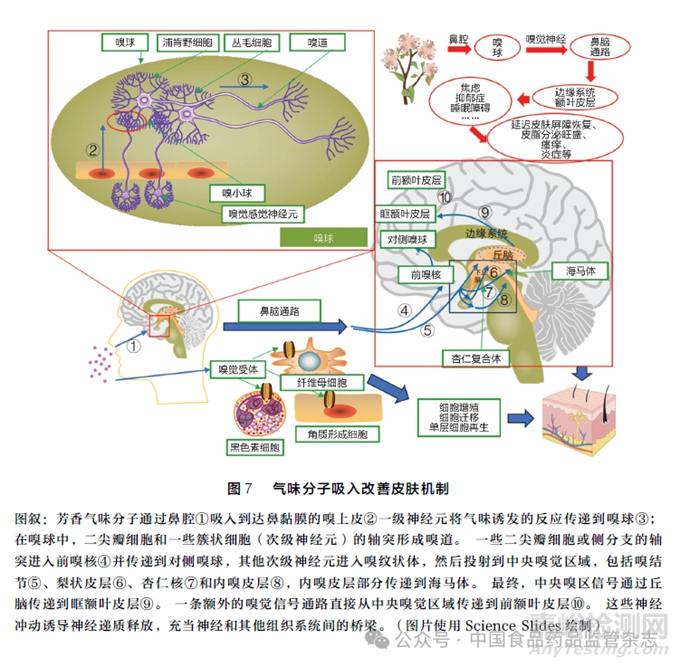
一些气味剂有助于调节皮肤免疫功能。HPA轴控制皮质醇释放,而压力激活HPA 轴会导致血浆皮质醇显著上调,对免疫系统产生重大影响。应激造成的免疫功能受损会延迟伤口愈合[34],有研究表明气味剂1,3 -二甲氧基 -5 -甲基苯(DMMB)可减轻压力对免疫反应的抑制,且缬草油能够下调应激诱导的高水平皮质酮,从而调节皮肤免疫功能[71]。压力应激会增加神经肽P 物质,引起肥大细胞活化,释放促炎介质刺激皮肤炎症,而吸入DMMB 可阻断肥大细胞活化,抑制压力的负面影响[67]。
气味剂可通过神经内分泌系统调节皮肤功能[72]。藏红花气味可以调节类固醇激素平衡。在卵泡期和黄体期用藏红花气味剂刺激可降低皮质醇并增加雌二醇水平, 从而增加胶原蛋白、改善皱纹,提高皮肤屏障功能[73]。还有研究表明,特殊香水调理可以升高女性脱氢表雄酮水平以及增加皮肤含水量[74]。
气味剂能够调节氧化应激。吸入薰衣草和迷迭香气味可降低皮质醇水平、增加自由基清除活性,防止氧化应激对皮肤的破坏[75]。
心理应激通过刺激糖皮质激素产生而损害屏障稳态,延迟屏障恢复[76]。应激抑制表皮细胞增殖分化,降低角质桥粒密度和大小,抑制表皮脂质合成,导致层状体形成和分泌减少,损害屏障功能和角质层完整性[76]。具有镇静作用的气味剂可抑制HPA 轴激活,修复皮肤屏障。吸入玫瑰精油能够抑制慢性压力引起的皮肤屏障受损,降低经表皮水分流失(trans epidermal water loss,TEWL)和唾液皮质醇[77]。还有研究表明气味剂DMMB 能够加速皮肤屏障修复[78]。
前额叶皮层诱导的HPA 轴激活能够促进皮脂腺增生和皮脂分泌,有研究发现特殊香料能够调节压力应激诱导的前额叶皮层异常活性,从而降低面部皮脂分泌水平[79]。
此外,嗅觉受体(olfactory receptors,ORs)表达不仅限于鼻上皮, 还发生在各种非嗅觉组织中,如皮肤。ORs 在皮肤细胞中表达,如角质形成细胞、黑色素细胞和成纤维细胞。气味配体能够与皮肤ORs 相互作用,发挥特定的生物学效应[80]。
角质形成细胞中表达的嗅觉受体OR2AT4 特异性激活诱导ERK 1/ 2 和p38 MAPK 磷酸化,促进表皮角质形成细胞增殖、迁移和细胞单层再生,表明OR2AT4 参与伤口修复过程[81]。激活人毛囊上皮中的OR2AT4 可抑制细胞凋亡并上调胰岛素样生长因子 -1,延长毛发生长[82]。
皮肤嗅觉受体OR2A4/7 位于表皮的基底角质形成细胞和基底黑色素细胞,激活该受体可促进角质形成细胞增殖、黑色素细胞树突化与色素沉着[83];皮肤嗅觉受体OR51B5 在基底上角质形成细胞和真皮成纤维细胞中表达,能够促进角质形成细胞单层的再生与细胞迁移[84]。皮肤嗅觉受体OR51B5 敲低会损害真皮成纤维细胞存活,胶原合成下降[85]。
此外,皮肤嗅觉受体OR10A6、OR2AG2 和OR11H4 在人原代角质形成细胞上表达,OR11H4主要位于表皮基底膜,OR2AG2 在基底上层表达,OR10A6 在基底上层较为密集[86]。这些受体参与调节皮肤应激反应, 可阻止压力应激对皮肤的损害,改善眼下区域暗沉[86 -87]。
总结与展望
皮肤与神经系统共同起源于外胚层,它们之间的密切关联代表了皮肤生物学中最重要的领域之一。从21 世纪开始,科技的进步促使神经美容科学崭露头角,而相关的功效活性物则被定义为“对皮肤神经系统表现出活性或作用于皮肤介质”,凭借其独特的作用机制与传统美容产品区别开来。近年来,随着科学技术的发展、国民经济的增长以及消费者需求的多样化提升, 化妆品行业已步入新时代,对皮肤神经美容科学的关注度日益增加,并致力于深入探索神经介质与皮肤的相互作用机制,发掘活性成分,希望通过新原料与新技术丰富化妆品产品品类、提升产品质量,从而改善皮肤外观与健康。神经美容科学作为功效护肤的重要组成部分,是值得化妆品行业着重探索的新方向。针对神经系统因素同时结合其他通路解决皮肤美容问题具有重要的现实意义与广阔的发展前景。目前本土美妆品牌在自主研发方面有着较大的进步空间, 需聚焦“高质量发展” 的行业主旋律, 提高自主创新能力,同时深入国际交流合作,打破技术壁垒,并倡导绿色可持续发展理念,进一步加大科研力度,开展前瞻性新技术与新原料应用研究,从而提升本土化妆品产业硬实力。随着全球市场上神经美容产品规模的不断扩张,这一新兴领域有望迎来研发及应用方面的更多科技突破。期待未来化妆品行业能够开发更有针对性的创新型功能进阶产品,满足市场的多样化需求。
引用本文
辛雨辰,仇红红,刘忠*.神经美容学原理与研究进展[J/OL].《化妆品与皮肤科学》网络专刊,2024(2):1-15[2024-12-06].https://www.cfdam-health.com/ebook/hzp/202402/index.html.

来源:中国食品药品监管杂志
关键词: 神经美容学