嘉峪检测网 2024-12-18 12:05
导读:近日,NMPA公布了创新医疗器械特别审查申请审查结果公示(2024年第11号),有 5 款产品进入创新通道,其中就有北京佰仁医疗科技股份有限公司(简称“佰仁医疗”)的介入肺动脉瓣及输送系统。
近日,NMPA公布了创新医疗器械特别审查申请审查结果公示(2024年第11号),有 5 款产品进入创新通道,其中就有北京佰仁医疗科技股份有限公司的介入肺动脉瓣及输送系统。
佰仁医疗研发生产的Salus®经胸介入肺动脉瓣系统,作为 “十三五”国家重点研发计划重点专项,是全球首个经胸途径植入的介入肺动脉瓣系统,属于业内首创,可以通过经胸微创切口经右室流出道穿刺直接植入瓣膜。
通过独有的经胸介入方式,对复杂病理解剖患者,术中可结合外科主肺动脉塑形,创新性地应用”植入瓣膜的同时,也让主肺动脉恢复生理解剖形态”这一理念,可适用于绝大多数肺动脉瓣反流或狭窄的患者,具有适用范围广、创伤小、手术风险低、操控性出色等优点;在解决肺动脉瓣失功的同时,有效重建主肺动脉生理形态,维持患者血流动力学稳定,改善患者心功能,提升患者生活质量。
研发背景
合并右心室流出道(RVOT)梗阻的先天性心脏病(先心病),如法洛四联症(TOF)、肺动脉瓣狭窄、完全性大动脉转位、右心室双出口、永存动脉干、肺动脉闭锁等,其行外科手术矫正时需要进行RVOT重建,纠正梗阻的RVOT。
既往,在发展中国家多采用RVOT扩大术(跨瓣补片扩大术或RVOT疏通术),较少采用带瓣的血管通道。前者术后即刻可产生肺动脉瓣反流(PR),后者晚期由于人工瓣膜衰败也会产生PR,可合并或不合并RVOT梗阻(即RVOTD)。长期的PR,导致右心负荷增加、右心扩大,继而引起右心衰竭、房性或室性心律失常甚至猝死,同时右心室容量负荷增加引起舒张期室间隔反向运动导致左心功能不全,进而导致患者长期生存期明显短于健康人。
因此,纠治严重PR是有必要的,可改善患者的症状、逆转右心室重构、提高患者心功能,并可能延长患者生存期,包括外科肺动脉瓣置换术(SPVR)和经导管肺动脉瓣置换术(TPVR)。虽然研究显示,SPVR和TPVR具有相同的围术期死亡率、中期死亡率及再次介入干预率,但是TPVR具有更低的围术期并发症发生率及更短住院时间。TPVR较SPVR具有创伤小、恢复快等优势。
在2018年美国心脏病学会/美国心脏协会(ACC/AHA)先心病管理指南,对于肺动脉瓣置换是采取TPVR还是SPVR无明确推荐,但在2020年欧洲心脏病学会(ESC)先心病管理指南指出,如果患者解剖合适,倾向选择TPVR。
TPVR手术中面临的最主要技术难题是,基于复杂的流出道解剖学,将大型号的瓣膜输送系统推送到肺动脉远端。目前国内外已上市或正在临床试验阶段的介入肺动脉瓣均为经皮/股静脉植入,尽管可以解决部分患者肺动脉瓣失功的问题,改善患者心功能,但瓣膜的植入要求患者的主肺动脉解剖学结构必须能适合人工瓣膜的支架形态。
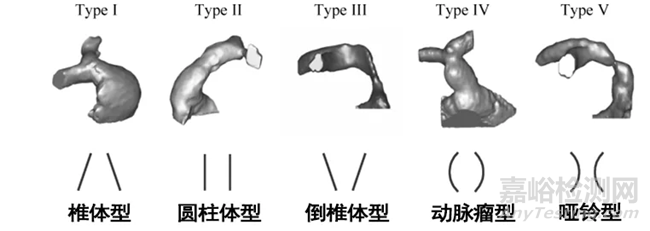
国外有学者对83例外科术后复杂的肺动脉病理解剖形态进行了分析,总结后分为五大类。其中Type I型整体呈“上窄下粗”的椎体型,瓣膜缺乏合适的锚定位置,植入后易发生移位,Type II-V型患者也需要满足合适的内径和适宜的解剖结构,最后仅有13%的患者接受了经皮(股静脉)介入肺动脉瓣治疗。因此,一款能适应绝大多数先心术后肺动脉瓣介入治疗的产品成为临床的迫切需求。
Salus介入肺动脉瓣系统
佰仁医疗与北京安贞医院苏俊武教授团队历时多年合作研发的Salus介入肺动脉瓣及输送系统,作为国家重点研发计划重点专项,于2020年7月获科技部批准立项(项目编号2020YFC1107900)。
该产品采用自膨式支架设计,瓣叶采用牛心包为材料,以成熟的外科牛心包瓣的制作工艺与处理技术加工而成,实现有效抗钙化,并具备出色的血流,全方位提高瓣膜的耐久性,是国内首个进入临床试验的经胸介入肺动脉瓣创新器械。

产品主要针对早年曾接受过右室流出道修复与重建,尤其是法洛氏四联症术后的患者,绝大多数患者因肺动脉瓣缺失导致三尖瓣大量反流而右心衰竭,需要经胸行主肺动脉重塑并经导管介入该产品再次重建人工肺动脉瓣。
Salus介入肺动脉瓣适用于可直接放瓣的肺动脉瓣反流/狭窄患者,通过独有的经胸介入方式,对于肺动脉解剖结构复杂、无法提供介入瓣膜合适锚定位置的患者,可同期行肺动脉成形术+介入肺动脉瓣植入术,达到理想的治疗效果,适用范围更广。
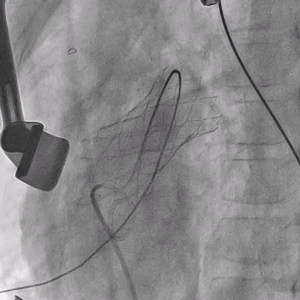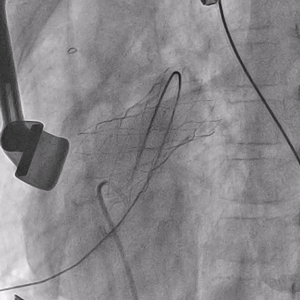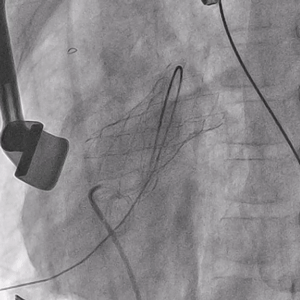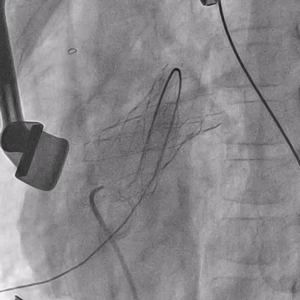
▲Salus介入肺动脉瓣支架植入后
产品临床试验
多中心临床试验
由首都医科大学附属北京安贞医院牵头,联合国内多家知名心脏中心参与,包括广东省人民医院、四川大学华西医院、复旦大学附属儿科医院、阜外华中心血管病医院等,是国内首个经胸介入肺动脉瓣临床试验。
试验设计:临床试验为多中心临床试验研究,由国家心血管病中心承担该临床试验设计及数据统计分析。针对此前曾手术重建或修复右室流出道、已具有经导管介入肺动脉瓣锚定部位的成年复杂先心患者。
试验结果:该研究共完成103例患者的成功救治,即刻手术成功率100%,初步印证了Salus介入肺动脉瓣的有效性、安全性和操控性均达到临床应用要求。
前瞻性临床研究
评估使用国产自膨式瓣膜(Salus)行经胸肺动脉瓣植入术治疗中重度肺动脉瓣反流的早期结果。共纳入患者25例,所有患者均成功植入瓣膜,术后早期未出现死亡、冠状动脉压迫、支架断裂、瓣膜移位、感染性心内膜炎等严重并发症。与术前相比,术后左心房和右心房上下径指数、右心室流出道前后径指数均明显降低;三尖瓣和肺动脉瓣反流程度均明显减轻,反流面积指数明显降低,差异均有统计学意义。
介入肺动脉瓣市场
法洛四联症(TOF)是最常见的紫绀型先天性心脏病,新生儿的发病率为0.33%,占紫绀型先天性心脏病的60%-80% ,占先天性心脏病的5%-7%。
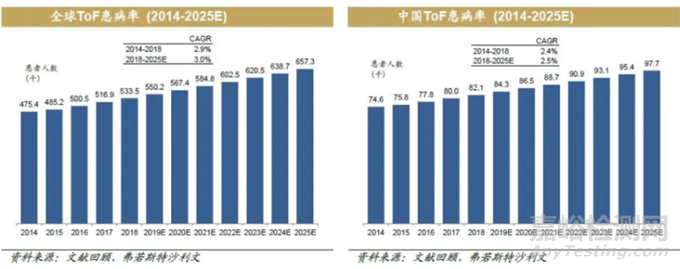
根据Frost & Sullivan的资料,全球TOF患者人数从2014年的475400人增加到2018年的533500人,预计到2025年将增加到657300人;中国TOF患者人数从2014年的74600人增加到2018年的82100人,预计到2025年将增加到97700人。保守估计目前紫绀型复杂先心病患者约为20万人。
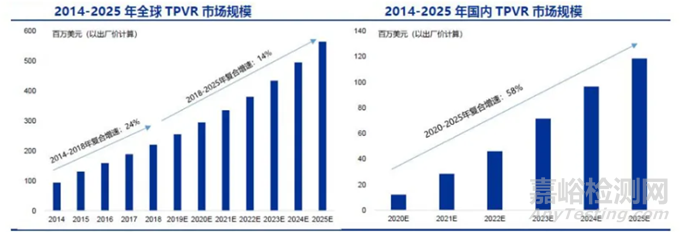
国内TPVR手术数量将从2020年的约400例增加到2025年的4400例,对应五年复合增速为61% ,同期渗透率将达到10.8%。同全球相比较而言,我国TPVR的渗透率低于全球水平,但爆发时间点将从2020年开始,且增速明显快于全球。
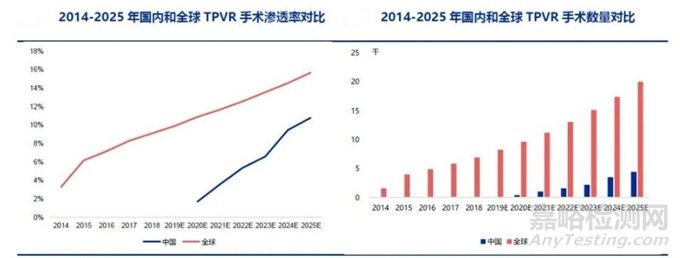
考虑到不断增长的TPVR手术数量,预计全球TPVR市场规模在经历了2014-2018年复合增速的24%之后,2018-2025年的复合增长率将会放缓至14% ,到2025年为5亿多美元;国内的TPVR市场则将从2020年的约1200万美元增长到2025年的1.19亿美元,对应年复合增速为58%。
中国市场将成全球TPVR的增长引擎;国内TOF矫治手术广泛使用跨环补片(据估计超过85% ),而近年来每年完成的手术量约1万余台,这部分患者大部分可能在10-30年后面临大量PR需要进行肺动脉瓣二次手术,未来患者数量可能更多。
截止目前,全球获批上市的TPVR产品共 5 款,分别来自美敦力、爱德华,以及启明医疗,尚无进口产品获得NMPA批准。从下表可以看出,TPVR产品主要分为球扩瓣、自膨瓣,两者最大的区别就是瓣膜直径的大小。球扩瓣膜直径较小,在临床上仅能满足不到20%的特殊患者需求;而自膨瓣的瓣膜直径大,在适用范围上也更广。
以启明医疗的自膨瓣VenusP-Valve为例,该产品有28/30/32/34/36mm五种型号,最大型号达到36mm,几乎适用于临床85%以上患者的需求。

美敦力的Melody瓣膜是第一款上市的商业化瓣膜,2017年被正式批准用于经导管肺动脉瓣治疗及瓣中瓣置入。置入Melody瓣膜的成功率高,在治疗肺动脉瓣反流,改善右心室扩张和改善心功能等方面令人满意,但其也具有应用条件苛刻、难以适用于粗大且不规则的自体右心室流出道患者等缺点。旗下Harmony经导管肺动脉瓣系统是全球首款自膨胀肺动脉瓣,曾被FDA认定为“突破性设备”。
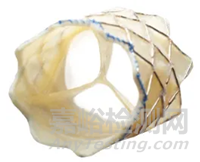
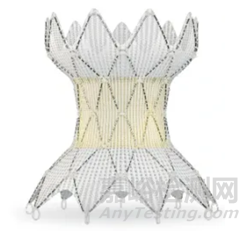
Melody瓣膜(左)和Harmony瓣膜(右)
SAPIEN 3是爱德华第三代Sapien瓣膜,它在上一代(Sapien XT)的基础上,包裹了一个聚对苯二甲酸乙二醇酯套,用于防止瓣周漏。爱德华SAPIEN 3经导管主动脉瓣膜与Alterra自适应支架联合用于严重肺动脉瓣反流患者已获批FDA。由韩国SNU-TaeWoo公司生产的Pulsta瓣膜则是一款瓣环锚定设计的TPVR瓣膜,由猪心包瓣膜和双股镍钛合金丝编织成的支架组成,于2019年获得KFDA批准。
2022年4月,启明医疗自主研发的经导管人工自膨式肺动脉瓣膜置换系统VenusP-Valve获欧盟CE MDR认证;同年7月,VenusP-Valve获国家药品监督管理局批准上市。该产品适用于严重肺动脉瓣反流(≥3+)的有自体右心室流出道的先心病术后患者(年龄≥12岁,体重≥30kg),且需符合一定的临床使用条件。

VenusP-Valve瓣膜
迈迪顶峰的PT-Valve®无菌经导管肺动脉瓣膜作为新一代国产自膨式瓣膜,主要适用于先天性心脏病矫治术后的肺动脉瓣反流或狭窄,是目前国内唯一一家通过国家药品监督管理局三类高风险医疗器械临床试验审批的介入肺动脉瓣膜,于2023年4月完成全国多中心临床试验入组。该产品还在2018年进入创新医疗器械特别审查“绿色通道”。
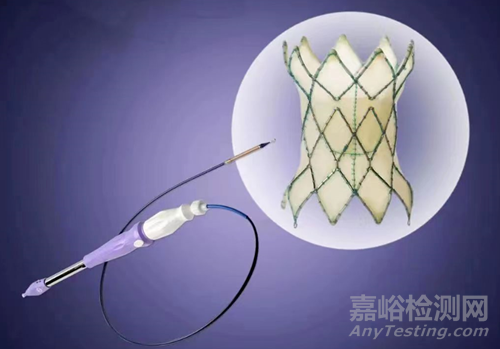
PT-Valve瓣膜
未来,TPVR赛道的竞争队伍只会越来越庞大,因此,国产企业要想率先突围,势必将结合本土临床需求,进行商业化落地调整,以获得最大的行业竞争力。
以中国市场为例,TPVR手术技术门槛高,全国符合开展手术资格的医院不过百家。并且手术复杂,医生学习周期长,且一场手术需要医院心内科、麻醉室、呼吸内科等相关科室协同。因此,对本土TPVR产品商业化落地而言,企业的学术推广、对医生的培训以及科室的建设帮扶就显得至关重要。
其次,吸纳TAVR单赛道布局脆弱性的经验,对械企而言,未来需把握整体心脏瓣膜的市场动向,及时调整单赛道投入比例,加强TPVR系统化方案的供给能力,方能在集采来临时,具备竞价优势,也更容易受到终端青睐。
关于佰仁医疗
北京佰仁医疗科技股份有限公司成立于2005年,于2019年12月成功登陆上海证券交易所科创板(股票代码:688198),是一家致力于动物源性植介入高值医疗器械研发与生产的高新技术企业,目前已获批准17个Ⅲ类医疗器械产品。
公司自主研发动物组织工程和原创化学改性处理技术,是国内技术领先的动物源性植介入医疗器械研发平台企业,产品覆盖心脏瓣膜置换与修复、先天性心脏病植介入治疗以及外科软组织修复三大领域。旗下人工生物心脏瓣膜——牛心包瓣于2003年获得注册,是国内最早注册、目前唯一有长期循证医学数据的国产产品(源自公司官方介绍)。
截至2024年三季度,公司2024Q1-Q3实现营业收入2.92 亿元,同比增长 13.57%;心脏瓣膜置换与修复治疗、先天性心脏病植介入治疗、外科软组织修复三个板块主营业务收入同比分别增长 14.78%、10.82%、14.33%,其中,人工生物心脏瓣膜实现收入 8749.25 万元,同比增长 15.54%。

来源:心未来
关键词: 介入肺动脉瓣