嘉峪检测网 2025-03-12 14:48
导读:这篇文件将为大家介绍下设计验证的基础工作内容。
下面这张流程图展示了设计验证在医疗器械整个设计开发过程中所处的阶段:

设计验证的开展首先要进行方案策划,方案一般包括如下内容:
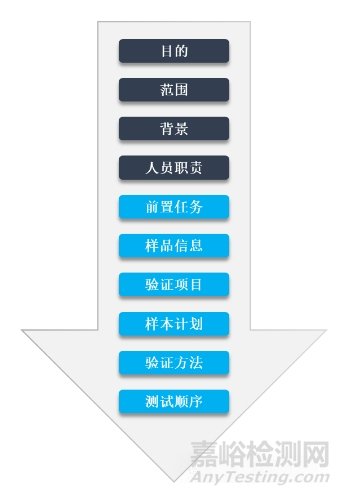
对于验证方案中的目的、范围、背景、人员职责,本文不多赘述,本文主要针对其余内容进行介绍。
1.前置任务确认

2. 样品信息
是否为最终成品:未最终完成的样品需解释理由。
样品加工信息:
所使用的DMR文件版本;
所使用的图纸版本;
所使用的原材料的批号/料号;
产品设计文档版本;
作业指导书版本、检验指导书版本等。
特殊制备样品:
说明特殊制备样品要求,并解释代表成品的理由
3. 验证项目选择
验证项目一般包括物理、化学、微生物、生物学、包装、可用性、存储和运输等产品特性。
4. 样品计划

设计验证样品计划主要包括样品规格的选择和样本量选择,这部分内容本公众号后面会单独出文章进行介绍。
5. 验证方法
优先采用产品法规标准清单适用的标准或推荐的方法,或者公司内部的STM方法。
明确测试条件的要求,列出所使用的测试仪器或工装,识别测量装置的校准情况,如果采用未经校准的测量装置,应注明合理的原因。
如果需要,应写明数据处理使用的计算方法。
非法规标准中推荐的方法,最好经过方法学验证。
6. 测试顺序
识别非破坏性测试、破坏性测试及测试对产品、部件性能影响,合理安排测试顺序。

来源:医聊器械
关键词: 医疗器械设计验证