嘉峪检测网 2025-03-28 20:39
导读:下面简述一下9097通则中包括的主要内容,以及有哪些CMC领域可以应用这些统计工具,从而帮助监管机构更好评估产出的分析数据。
2025版中国药典通则9097是对分析数据的评估与处理。这是一个新的通则,在以前版本中国药典中没有出现过,是一个很大的进步。
对于分析数据的一些科学解释与评估,是药品研发、设计、生产与检测中非常重要的步骤,在药品质量控制策略中起到了不可或缺的一环,是药品生命周期管理的重要内容。
在中国药典的各论中,存在着各种的统计术语、方法与原理,本次引入9097通则,是对各论中的这些术语、方法与原理的规范,提供了一个科学监管方法。
本通则主要内容与USP1010通则接近,核心内容包括了统计的基本概念、方法、原则的介绍,以及一些应用场景。本通则内容与药品的有效性与安全性评价没有直接相关性。
下面简述一下9097通则中包括的主要内容,以及有哪些CMC领域可以应用这些统计工具,从而帮助监管机构更好评估产出的分析数据。
首先是描述性统计部分,包括了集中趋势(如均值、中位数)和离散程度(如标准差、极差)的统计量,以及直方图、箱线图等统计学图形的应用。这些描述性统计在药典各论或者通则中常常出现,作为判断标准或者指标,用于药品或方法的可接受标准设定。描述性统计通过产出的数据,常可以利用公式直接计算得到,是比较容易理解,不需要高阶的统计学知识即可理解。
第二类是推断性统计部分,包括推断性统计:包括总体参数估计(如置信区间、预测区间、容忍区间)和假设检验(如差异显著性检验、等效性检验)。推断性统计需要更多的一些数学知识,需要进行统计假设检验,判断数据的分布,选择合理的假设检验,查找相关的检验公式,然后进行计算与判断。推断性统计难度相对描述性统计,需要一些高阶数学知识帮助理解。它很有用,可以帮助研发生产质量人员进行一些科学的判断,合理的控制研发与生产的风险,最终达到控制药品质量。
常用的推断性统计方法包括控制图(如单值-移动极差图、均值-极差图)、过程能力分析(如Cp、Cpk指数)以及贝叶斯推断统计。
总体参数估计(如置信区间、预测区间、容忍区间))和假设检验(如差异显著性检验、等效性检验)的CMC应用场景常见的有分析方法在研发实验室与QC实验室的桥接,场地转移的方法对比,产品技术转移的工艺验证数据评估,GMP管理中的偏差率分析,工艺变更后的收率分析,物料取样的AQL分析,及稳定性预测分析研究。
以上应用对于商业化产品的使用场景非常高,监管机构在审评中也会对以上场景进行统计学上的分析,帮助科学评估CMC研发与变更在药品生命周期中的管理。
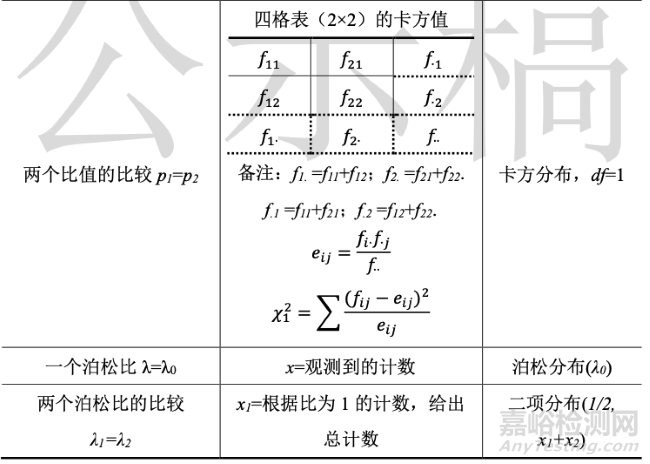
下图为常见的样品比较假设检验的统计量。其中等效性检验,即通过双单侧检验(TOST)判断两个方法的均值是否等效,在CMC研发过程中非常有用。


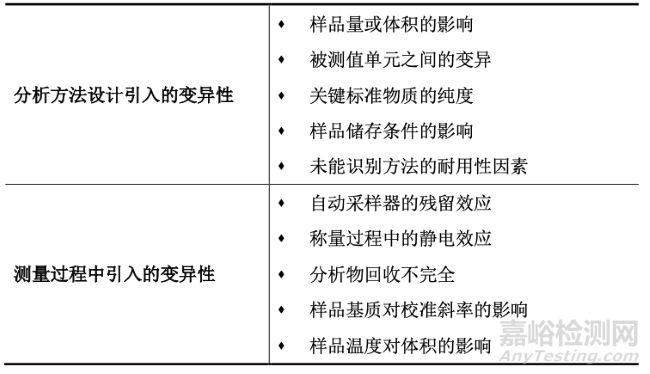
分析过程中不确定度的引入导致了误差。下述表中展示哪些分析过程会引入这些不确性,从而导致误差。
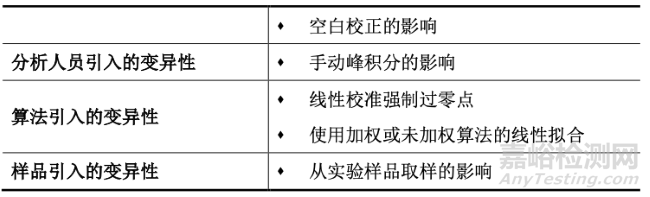
常见的统计方法中,有单值控制图:过程平均值±3×过程标准差,有检测失控结果的Nelson规则。


过程能力是指过程满足质量标准的程度,过程能力分析是将过程控制得到的结果与质量标准进行对比分析与评价。常见的过程能力指数包括Cp、Cpk、Cpu、Cpl 和Cpm。
Cp 指数是指过程满足技术要求的能力,用规格限宽度与过程特征分布宽度之比计算其大小。Cp 指数假设过程是居中的,它不包含平均值估计的过程中心
相对于规格限的信息,因此 Cp 指数也被称之为潜在过程能力。
Cpk 是指过程的最小能力指数,
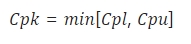
Cpl 和 Cpu 是单侧过程能力指数,适用于杂质检查和缺陷项比例等具有单侧限值的情形。Cpl 用于评估过程符合下规格限的能力,Cpu 用于评估过程符合上规格限的能力。
当强调质量特性中心偏离目标值(T)所导致的质量损失(相对偏倚)时,可以使用Cpm指数对过程能力进行度量。
小结:
9097通则的发布可以很好的帮助药物研发人员科学评估研发过程的数据质量和等效,对于生产质量管理人员来讲也必不可少,赋能药品上市后变更、药品生产全生命周期管理。也同步参照了ICH指南中要求关药典通则内容进一步协调发展的思路。

来源:蒲公英Ouryao