嘉峪检测网 2025-04-17 20:11
导读:本文介绍了有源、无源医疗器械有效期评估。
医疗器械有效期
医疗器械产品有效期是指在规定储存条件下,医疗器械保持其安全,有效性和质量稳定性,能满足预期使用要求的器械。可通过加速老化,实时老化试验,稳定性试验,包装完整性试验去验证产品有效期。
相关法规:
《有源医疗器械使用期限注册技术审查指导原则》(2019年第23号)
《无源植入性医疗器械货架有效期注册申报资料指导原则》(2021年修订)
GB/T34986-2017《产品加速试验方法》2018.5.1
GB2689.3-1981《寿命试验和加速寿命试验的简单线性无偏估计法》(用于威布尔发布)
YY/T0681.1-2018《无菌医疗器械包装试验方法加速老化试验指南》2020.1.1
详细信息
1.评价方式
根据评价或经验预先设定期限值(已确定寿命):通过一种或多种方法进行验证证明预先设定值的合理性
不预先设定期限值(未知寿命),通过一种或多种方法最终确定产品的使用期限。
2.评价路径
整机验证
分为不同部件/子系统进行验证
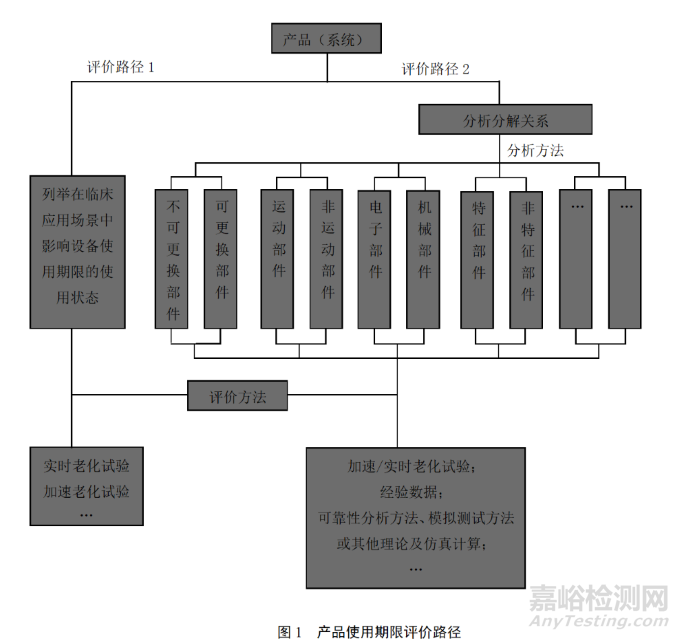
3.评价方法-加速老化计算方式
有源:参考依据:GB/T34986-2017《产品加速试验方法》
相关模型
无源:参考依据《无源植入性医疗器械货架有效期注册申报资料指导原则》,YY/T0681.1-2018《无菌医疗器械包装试验方法加速老化试验指南》
相关模型
4.有源医疗器械与无源医疗器械的区别
有源:一般为有效期限验证,因为有源器械除了受环境影响,还与内部电气元件的损耗,软件系统的更新兼容有密切习惯。
确定有效期时,有源医疗器械通常需进行模拟实际使用的老化测试,包括电气性能测试、功能稳定性测试等
无源:一般为货架有效期验证,因为无源医疗器械主要受储存环境因素制约,如温度、湿度、光照、气压等。
确定货架有效期时,无源医疗器械多采用加速老化试验和实时老化试验,模拟储存环境,定期检测物理、化学、生物性能。将医疗器械置于高温高湿环境箱中,观察不同时间点的性能变化,验证货架有效期。
5.加速老化和实施老化的区别
6.影响因数
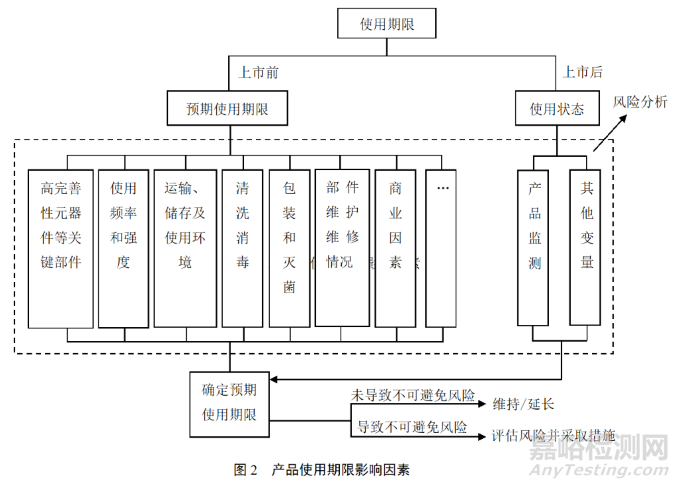
7.产品有效期在注册申报资料里的体现
说明书与标签应体现产品有效期。
研究资料-产品稳定性研究
8.产品整机的生产日期制定
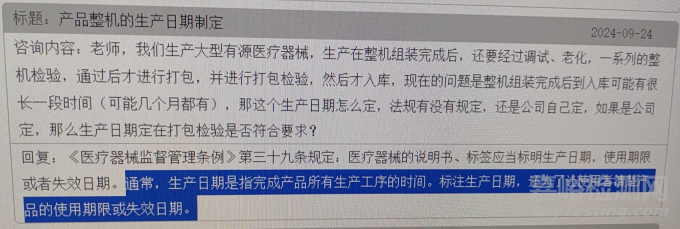
9.产品到有效期后,经使用单位或生产企业进行性能验证,评估是否可以继续使用?
根据现行法规是不可以的,《医疗器械监督管理条例》第五十五条和《医疗器械使用质量监督管理办法》第十二条明确规定,医疗器械使用单位不得使用过期的医疗器械

来源:医械铁锅炖
关键词: 医疗器械有效期