嘉峪检测网 2025-05-08 20:23
导读:研制乳粉基体己烯雌酚分析标准样品。
摘 要: 研制乳粉基体己烯雌酚分析标准样品。筛选未检出己烯雌酚的进口全脂乳粉为原料,人工添加目标物,采用湿法-喷雾干燥工艺制备乳粉样品,选用双层包装,每包按10 g分装。采用液相色谱-串联质谱法进行均匀性、稳定性评估,协同9家实验室进行定值,评定特性值的测量不确定度。结果表明,该标准样品均匀性良好,稳定性达到18个月,特性值为12.8 μg/kg,扩展不确定为0.8 μg/kg(k=2)。该标准样品可用于乳粉中己烯雌酚含量检测和分析全程的质量保证与控制,以及对检测分析方法和检测能力的评价。
关键词: 乳粉; 己烯雌酚; 标准样品; 均匀性; 稳定性; 定值
己烯雌酚是一种人工合成的雌激素类药物,具有与天然雌二醇相似的药理与治疗作用[1‒2]。此外,它还能刺激动物的正常合成代谢,调节生理功能,并促进生长,因此被用作畜禽饲料中的促进剂,特别是在牛羊等动物饲料中应用较多[3‒5]。然而,研究表明,这种药物会在动物的肝脏、肌肉、脂肪及奶源中残留,长期摄入含有己烯雌酚残留的食物,会对人体健康产生诸多负面影响,包括损害肝脏与肾脏功能,引发致畸与致癌风险,干扰内分泌系统以及影响生殖、性别分化与生长发育等[6‒7],国内外高度重视己烯雌酚在动物源性食品中的残留检测。我国农业部公告第176号中将己烯雌酚列为禁止在饲料和动物饮水中使用的药物,并在农业部公告第250号中规定禁止在食品动物中使用己烯雌酚及其盐、酯。
基体标准物质被广泛用于确保检测结果及数据的可比性、溯源性、准确性,分析仪器校准、测量方法与测量能力验证评价[8‒11]。乳及乳制品是人们生活中重要的食物来源,尤其是乳粉作为婴幼儿的主要食物,目前国内外乳粉基体的己烯雌酚标准物质尚处于市场空白。为了确保检测结果的准确可靠,防止被己烯雌酚污染的乳制品流入市场,保障乳制品品质与食品质量安全,研制乳粉基体的己烯雌酚分析标准样品,具有非常重要的意义。
笔者采用喷雾干燥法[12]制备乳粉基体己烯雌酚标准样品,按照GB/T 15000.3—2023《标准样品工作导则 第3部分:标准样品 定值和均匀性与稳定性评估》进行均匀性及稳定性评估、联合定值,以期符合要求及达到预期目标,为乳粉中己烯雌酚的日常检测和质量控制提供依据。
1. 实验部分
1.1 主要仪器与试剂
喷雾干燥器:带内置流化床,基伊埃工程技术(中国)有限公司。
混料机:TB250型,安培威机械制造(上海)有限公司。
均质机:NS3006H型,基伊埃工程技术(中国)有限公司。
巴氏系统:400L型,安培威机械制造(上海)有限公司。
浓缩系统:FF-200型,基伊埃工程技术(中国)有限公司。
液相色谱-串联质谱仪:5500型,美国艾伦-布拉德利公司。
己烯雌酚标准物质:质量分数为99.7%,标准物质编号为GBW(E) 060984,中国计量科学研究院。
己烯雌酚标准品:质量分数为97.7%,编号为46207,西格玛奥德里奇(上海)贸易有限公司。
己烯雌酚-D8同位素内标:质量分数为98.3%,上海安谱实验科技股份有限公司。
ENVI-Carb固相萃取柱、氨基固相萃取柱:美国沃特世科技有限公司。
β-葡萄糖醛酸酶-芳香基硫酸酯酶溶液:β-葡萄糖醛酸酶大于100 000单位/mL,芳基硫酸酯酶小于20 000单位/mL,上海安谱实验科技股份有限公司。
甲醇、乙腈、甲酸、二氯甲烷:均为色谱纯,上海安谱实验科技股份有限公司。
乙酸、乙酸钠:均为分析纯,上海麦克林生化科技有限公司。
全脂奶粉样品:新西兰Open Country Dairy有限公司。
包装袋:食品级,东莞市盈尔电器有限公司。
铝箔袋:苏州堂正机械有限公司。
实验用水为一级水、二级水。
实验用气为氮气发生器制备的氮气。
1.2 乳粉基体标准样品制备
1.2.1 原料筛选
采用GB/T 21981—2008《动物源食品中激素多残留检测方法 液相色谱-质谱/质谱法》筛选未检出己烯雌酚的进口全脂乳粉为原料。
1.2.2 制备流程
(1)准确称取己烯雌酚标准品适量,用甲醇配制质量浓度为0.125 mg/mL的溶液。
(2)在配料罐中用50~60 ℃的二级水溶解35 kg乳粉,配制成质量分数为25%的复原乳,备用。
(3)用量杯量取2 000 mL复原乳,加入3.64 mL的0.125 mg/mL己烯雌酚溶液,在添加过程中持续搅拌,确保混合均匀,20 min后,所有溶液转移至第2步的配料罐中,使用相同浓度的复原乳清洗量杯3次,并将清洗液一并加入配料罐,维持混合液温度为50~60 ℃,采用高剪切技术搅拌(30 min,2 900 r/min),静置30 min以促进水合作用,再次高剪切搅拌20~30 min,以获得均匀的己烯雌酚基质料液。
(4)将基质料液进行均质化处理,压力逐渐升至20 MPa并保持25 min,随后进行巴氏杀菌,杀菌后,将料液浓缩至45%(质量分数),以便于后续处理。
(5)将浓缩后的己烯雌酚基质料液进行喷雾干燥,收集乳粉塔进料30 min后的乳粉样品,将收集的乳粉样品送入乳粉干混仪中混合6 h,最终得到乳粉基体标准样品。
1.2.3 样品的分装
内层用食品包装袋抽真空包装,外层用铝箔袋抽真空包装。分装规格为10 g/包,共1 000份样品。样品包装后在冷冻条件(-20±2) ℃下存储。
1.3 标准样品中己烯雌酚的检测
1.3.1 标准溶液配制
己烯雌酚标准储备液:1.0 mg/mL。准确称取25.0 mg (精确到0.000 01 g)己烯雌酚标准品置于25 mL容量瓶中,用甲醇溶解并定容至标线。于-18 ℃以下保存,有效期为12个月。
己烯雌酚-D8内标标准储备液:1.0 mg/mL。准确称取适量己烯雌酚-D8同位素内标置于25 mL容量瓶中,用甲醇溶解并定容至标线。于-18 ℃以下保存,有效期为12个月。
己烯雌酚标准中间液I:10 μg/mL。准确移取1 mL己烯雌酚标准储备液于100 mL容量瓶中,用甲醇定容至标线。于-18 ℃以下保存,有效期6个月。
己烯雌酚-D8标准中间液Ⅰ:10 μg/mL,准确移取1 mL己烯雌酚-D8内标标准储备液于100 mL容量瓶中,用甲醇定容至标线。于-18 ℃以下保存,有效期6个月。
己烯雌酚标准中间液Ⅱ:0.1 μg/mL。准确移取1 mL己烯雌酚标准中间液I于100 mL容量瓶中,用甲醇定容至标线。于0~8 ℃保存,有效期3个月。
己烯雌酚-D8标准中间液Ⅱ:100 ng/mL。准确移取0.5 mL己烯雌酚-D8标准中间液I于50 mL容量瓶中,用甲醇定容至标线。于0~8 ℃保存,有效期3个月。
己烯雌酚系列标准工作液:准确量取一定量的将己烯雌酚标准中间液II于7只10 mL容量瓶中,并分别加入一定量的己烯雌酚-D8标准中间液Ⅰ,用甲醇-水溶液定容至标线,配制成己烯雌酚质量浓度分别为0.5、1.0、5.0、10、20、30、50 μg/L的己烯雌酚系列标准工作液,其中己烯雌酚-D8内标质量浓度均为10 μg/L。
1.3.2 提取
称取1 g乳粉样品(精确至0.000 1 g),置于50 mL具塞离心管中,准确加入己烯雌酚-D8标准中间液Ⅱ 100 μL和10 mL乙酸-乙酸钠缓冲溶液,涡旋混匀,再加入β-葡萄糖醛酸酶/芳香基硫酸酯酶溶液100 μL,于(37±1) ℃振荡酶解12 h。取出冷却至室温,加入25 mL甲醇,超声提取30 min,于0~4 ℃以15 000 r/min离心10 min。将上清溶液转入洁净烧杯中,加入水100 mL,混匀后待净化。
1.3.3 净化
将上述获得的澄清溶液全部转移到活化好的ENVI-Carb固相萃取柱上,抽干,之后加入200 μL甲醇,将残余的水去掉,然后用真空泵将小柱减压抽取30 min以上,确保将残余的水抽干。再将活化好的氨基柱串接在ENVI-Carb固相萃取柱下方(用转接头)。用6 mL二氯甲烷-甲醇溶液(体积比7∶3)洗脱,将两支小柱分别吹干,洗脱液在微弱的氮气流下吹干,用1 mL甲醇-水(体积比1∶1)溶解,旋涡振荡,过0.2 μm滤膜,供液相色谱串联质谱分析。
1.3.4 液相色谱条件
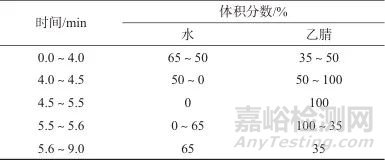
色谱柱:Acquity UPLC HSS T3柱 (100 mm×2.1 mm,1.8 μm,美国沃特世科技有限公司);进样体积:5 μL;色谱柱温度:40 ℃;流动相:A相为水,B相为乙腈;流量:0.3 mL/min;洗脱方式:梯度洗脱,洗脱程序见表1。
表1 梯度洗脱程序
Tab. 1 Gradient elution program
1.3.5 质谱条件
离子源:ESI-源;监测模式:多反应监测(MRM)模式;雾化气压力:31 kPa;辅助气压力:344.5 kPa;气帘气压力:17.2 kPa;电雾式检测器(CAD):“medium”;离子化电压:4 500 V (-);离子源温度:550 ℃。己烯雌酚及同位素内标的MRM检测参数见表2。
表2 己烯雌酚及其内标物的质谱参数
Tab. 2 Mass spectrometry parameters of diethylstilbestrol and its internal standard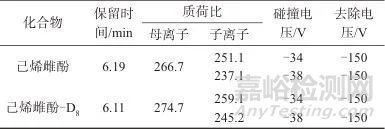
1.4 均匀性评估
采用简单随机抽样的方式,随机抽取15个样品,由相同实验人员在重复性条件下进行检测,每份样品重复测定3次。按照GB/T 15000.3—2023样品测试的要求,进行均匀性评估。采用单因素方差分析法(ANOVA) (F检验)对测定结果进行统计分析。
1.5 稳定性评估
按照GB/T 15000.3—2023,进行短期和长期稳定性研究。
1.5.1 短期稳定性研究
考察常温运输条件下和极限条件下的稳定性。运输条件稳定性是将样品置于(25±2) ℃下,分别在第0、1、3、5、7 d进行检测。极限条件的稳定性是将样品置于(60±2) ℃下,分别在第0、1、3、5、7、10 d进行稳定性检测。每个时间点随机取3个样品,每个样品平行测定2次,按照1.3所述的方法进行测试。
1.5.2 长期稳定性研究
采用经典稳定性研究方案,从最小包装单元中随机抽取代表性样品,确保样品分布能全面反映总体特征。此次长期稳定性考察为期18个月,依据时间由密至疏的原则,设定了5个检测节点,每个节点随机选取3个样品进行2次平行测定,按1.3方法进行测试。
1.6 定值与不确定度评定
按照GB/T 15000.3—2023的要求,采用一个有能力的实验室网络对操作定义的被测量进行定值。将己烯雌酚有证标准物质GBW(E) 060984同标准样品合作定值作业指导书随样品一同发送,以确保标准样品量值溯源性和准确性。每个参加定值的实验室发送3个样品,1份为测试样品,2份为定值样品,每份取3个子样,每个子样测试3次取均值。实验室按1.3方法对乳粉中己烯雌酚进行检测。所得定值数据经过正态性、格拉布斯、狄克逊及等精度检验后,综合各实验室结果计算总平均值,然后将影响标准样品量值不确定度的各项因素进行合成与扩展处理,最终确定标准样品的标准值。
2. 结果与讨论
2.1 测试方法选择
目前己烯雌酚的检测方法有GB/T 21981—2008《动物源食品中激素多残留检测方法 液相色谱-质谱/质谱法》,GB/T 22992—2008《牛奶和奶粉中玉米赤霉醇、玉米赤霉酮、己烯雌酚、己烷雌酚、双烯雌酚残留量的测定 液相色谱-串联质谱法》,两种方法的技术路线没有明显差异,对于牛奶基质的样品,GB/T 21981—2008检出限更低。由于己烯雌酚不得在动物源性食品中检出,所以进行风险监控时宜选择检出限更低的方法。GB/T 21981—2008适用的基质为牛奶,该标准样品的基质为全脂奶粉,因此需要进一步验证乳粉复原后,方法性能是否符合要求。
2.2 取样量研究
针对乳粉基体标准样品开展了1.0、2.0、3.0 g 3个不同的取样质量试验,结果显示,己烯雌酚的测定值随着称样质量的增大而减小。究其原因可能是:(1)因为称样质量增大,复原乳更加粘稠,己烯雌酚被蛋白质包裹,并未提取完全;(2)己烯雌酚的极性弱,乳粉称样质量越多则脂肪含量越多,导致更多的己烯雌酚溶于脂肪,检测结果偏小。故选择最小取样量为1.0 g。
2.3 方法性能验证
2.3.1 方法回收率和精密度
取己烯雌酚标准中间液Ⅱ进行加标回收试验。不同加标水平(2.0、10.0、50.0 μg/kg)的平均回收率及测试结果的相对标准偏差(RSD)见表3。由表3可知,己烯雌酚的平均回收率为98.64%~101.59%,RSD为3.78%~3.91%。结果表明,该方法具有良好的准确度和精密度,符合研究要求。
表3 加标回收试验
Tab. 3 Results of standard addition recovery test
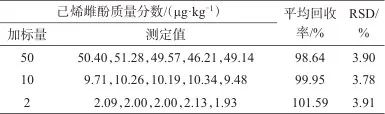
注:本底值未检出。
2.3.2 方法线性、检出限和定量限
取各个质量浓度的系列己烯雌酚标准工作液,依次上机测试,以目标物浓度为横坐标,色谱峰面积比为纵坐标,绘制标准曲线,得到线性回归方程为y=141 175x+23 441,相关系数为0.998,质量浓度线性范围为0.5~50.0 μg/L。按3倍信噪比计算检出限,按10倍信噪比计算定量限,得到检出限和定量限分别为0.04、0.14 μg/kg。
2.4 均匀性评估
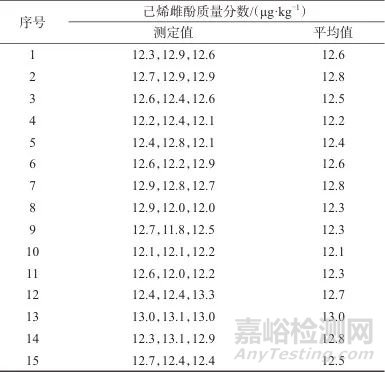
按照1.4方法对标准样品的均匀性进行检验,采用单因素方差分析法(ANOVA) (F检验)对测量结果进行统计分析,根据自由度(ν1,ν2)及给定的显著性水平α,可由F表查得临界值Fα。若F<Fα,则认为单元内与单元间无明显差异,样品是均匀的;若F>Fα,则怀疑各单元间有系统差异,即样品之间存在差异。均匀性测定结果见表4。由表4数据可以计算得F=2.03,小于临界值F0.05 (14,30)=2.04,说明标准样品均匀性良好。
表4 均匀性测定结果
Tab. 4 Results of homogeneity test
2.5 稳定性评估
2.5.1 短期稳定性
短期稳定性采用单因素方差分析,通过F检验对样品的稳定性进行评估。若F小于自由度为(f1,f2)及给定显著性水平α(通常α=0.05)的临界值Fα(f1,f2),则表明样品内和样品间无显著性差异,样品是稳定的,并用方差分析结果评估短期稳定性引入的不确定度。短期稳定性测定结果见表5和表6。
表5 25 ℃下短期稳定性测定结果
Tab. 5 Results of short-term stability test at 25 ℃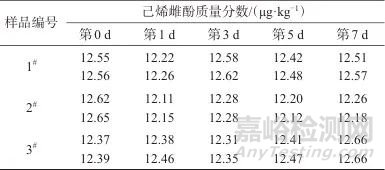
表6 60 ℃下短期稳定性测定结果
Tab. 6 Results of short-term stability test at 60 ℃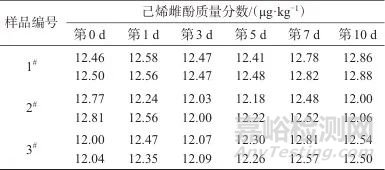
由结果数据可以计算出25、60 ℃下的F值分别为2.58和2.52,均小于F临界值(分别为2.76和2.53),说明标准样品在运输条件(25±2) ℃ 7 d内和(60±2) ℃ 10 d内,样品中己烯雌酚含量均无显著变化,样品的短期稳定性符合要求。
2.5.2 长期稳定性
长期稳定性采用特性值随时间变化的曲线来判断是否具有单方向变化趋势。X表示稳定性考察时间,Y表示稳定性考察结果,则存在Y=b0-b1X,b1、b0分别为斜率和截距。对于稳定的标准样品,b1的期望值为零。用t检验来检验斜率是否显著不等于零,若|b1|<t×s(b1),表明斜率不显著,没有观察到不稳定性。表7和表8分别为长期稳定性测定结果和长期稳定性趋势分析结果。由表8可知,乳粉中己烯雌酚拟合直线斜率|b1|<t×s(b1),斜率不显著,说明样品在18个月内稳定。
表7 长期稳定性测定结果
Tab. 7 Results of long-term stability test
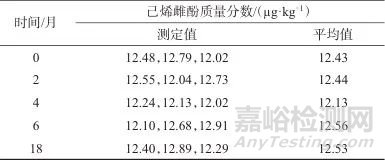
表8 长期稳定性趋势分析结果
Tab. 8 Results of Long-term stability trend analysis
2.6 标准样品的定值
乳粉中己烯雌酚分析标准样品的定值由9家实验室协同定值,定值结果见表9。
表9 参加定值实验室的结果汇总表
Tab. 9 Summary table of results from participating in the fixed value laboratory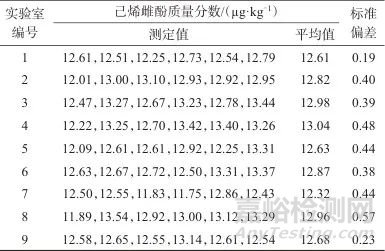
2.6.1 定值数据的异常值检验
采用狄克逊和格拉布斯法进行异常值检验,剔除异常值时,注意不能仅仅基于统计结果而剔除,还应结合技术原因进行判断。
实验室内测定数据狄克逊检验结果表明,有3个检验数据大于临界值f(0.05,6)=0.628,但该异常值在方法的精密度要求内,经技术判断,无需剔除。实验室间测定数据和所有数据的格拉布斯检验结果中,各组数据的平均值及全部数据均无异常值剔除。
2.6.2 正态性检验
采用偏态系数和峰态系数法进行正态性检验,若该组测量数据服从正态分布,则偏态系数A和峰态系数B应分别小于相应的临界值和落入区间中。表10为正态性检验数据。由表10可以看出,A=0.28,小于临界值0.49,且B在P=0.95所对应的临界值范围内,说明数据为正态分布。
表10 正态性检验数据
Tab. 10 Normality test data

2.6.3 等精度检验
采用科克伦准则进行等精度检验,表11为科克伦检验结果。其判断方法:对给定的显著性水平α,若C≤C(α,m,n),则无可疑数据组剔除,各组等精度。若C>C(α,m,n),则最大方差组数据应作为可疑数据组弃去。为慎重起见,数据统计时,若C>C(0.01,m,n),则最大方差组数据作为可疑数据组弃去;对C(0.05,m,n)<C<C(0.01,m,n)的最大方差组数据予以保留。计算得出C=0.219 1,小于临界值C (0.05,9,5)=0.328 6,说明无可疑数据,各组等精度。
表11 科克伦检验结果
Tab. 11 Results of Cochran's Q test
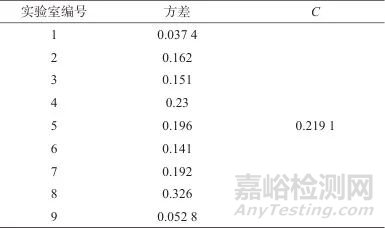
定值结果评估后全部保留,标准样品的定值结果为9家实验室测定结果的总平均值,为12.8 µg/kg。
2.6.4 测量不确定度评定
按照GB/T 15000.3—2023要求,标准样品特性值的合成不确定度包括:定值的不确定度(uchar)、均匀性引入的不确定度(uhom)、短期稳定性(usts)及长期稳定性(ults)引入的不确定度,各分量不确定度信息见表12。
表12 各分量不确定度信息汇总表
Tab. 12 Summary table of uncertainty information for each component
合成标准不确定度按式(1)计算,得uCRM=0.4 μg/kg,取包含因子k=2,扩展不确定度U=0.8 μg/kg。
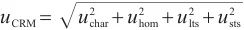 (1)
(1)
2.6.5 定值结果的表达
该标准样品的特性值为12.8 μg/kg,扩展不确定为0.8 μg/kg (k=2,p=0.95)。
3. 结语
制备了乳粉中己烯雌酚分析标准样品,采用液相色谱-质谱/质谱法对标准样品进行均匀性、稳定性评估,协同9家实验室定值并进行测量不确定度评定。结果显示,标准样品均匀性良好,长期稳定性达18个月,研制的乳粉中己烯雌酚成分标准样品的特性值为12.8 μg/kg,扩展不确定为0.8 μg/kg (k=2,p=0.95)。该标准样品可用于乳粉中己烯雌酚含量检测和分析全程的质量保证。
参考文献:
1 王丹,鄂志强,刘春波,等.婴幼儿配方乳粉中激素检测技术研究进展[J].中国乳品工业,2016(12): 30.
WANG Dan,E Zhiqiang,LIU Chunbo,et al. Progress in study of determination methods of hormone in infant formula[J]. China Dairy Industry,2016(12): 30.
2 李强,赵炜,蔡立鹏,等.气相色谱-串联质谱测定乳粉中6种雌激素[J].乳业科学与技术,2013,36(6): 18.
LI Qiang,ZHAO Wei,CAI Lipeng,et al. Simultaneous analysis of six estrogens in milk powder by GC-MS-MS[J]. Journal of Dairy Science and Technology,2013,36(6): 18.
3 张也,赵长源,高志贤,等.食品中常见雌激素类物质的危害分析[J].食品安全质量检测学报,2023,14(6): 153.
ZHANG Ye,ZHAO Changyuan,GAO Zhixian,et al. Hazard analysis of common estrogens in food[J]. Journal of Food Safety & Quality,2023,14(6): 153.
4 冒玉娟,王婧,刘佳敏,等.己烯雌酚残留检测研究进展[J].畜牧与饲料科学,2019,40(5): 28.
MAO Yujuan,WANG Jing,LIU Jiamin,et al. Recent progress on residues detection technology of diethylstilbestrol[J]. Animal Husbandry and Feed Science,2019,40(5): 28.
5 常嵘,叶巧燕,刘慧敏,等.牛奶中激素检测方法的研究进展[J].食品安全质量检测学报,2022,13(16): 5 235.
CHANG Rong,YE Qiaoyan,LIU Huimin,et al. Research progress on detection methods of hormones in milk[J]. Journal of Food Safety & Quality,2022,13(16): 5 235.
6 刘梦悦.雌激素干扰物非定向筛查方法的建立及在乳制品检测中的应用[D].济南:山东师范大学,2020.
LIU Mengyue. Establishment of non-targeted screening method for estrogenic disrupting compounds and its application in dairy product detection[D]. Jinan:Shandong Normal University,2020.
7 张思遥.典型食品基质中痕量内分泌干扰物和黄曲霉毒素的计量技术研究与标准物质研制[D].北京:北京化工大学,2023.
ZHANG Siyao. Development of measurement technology and certified reference materials of endocrine disruptors and aflatoxins in typical food[D]. Beijing:Beijing University of Chemical Technology,2023.
8 李宗旺,李鹏,李丽,等.辣椒粉中4种黄曲霉毒素和赭曲霉毒素A基体标准物质研制[J].化学分析计量,2024,33(6): 1.
LI Zongwang,LI Peng,LI Li,et al. Development of reference materials for four aflatoxins and ochratoxin A in chili powder[J]. Chemical Analysis and Meterage,2024,33(6): 1.
9 张淼,张海婧,王红伟,等.饮用水中5种金属元素混合标准物质研制[J].化学分析计量,2024,33(8): 1.
ZHANG Miao,ZHANG Haijing,WANG Hongwei,et al. Development of 5 metal elements mixed standard materials in drinking water[J]. Chemical Analysis and Meterage,2024,33(8): 1.
10 霍丽娜.水产品中甲基汞标准物质的研制[J].化学分析计量,2024,33(9): 1.
HUO Li'na. Development of reference material of methylmercury in aquatic products[J]. Chemical Analysis and Meterage,2024,33(9): 1.
11 刘天和,魏宁,武彩红,等.牛奶冻干粉中阿莫西林基体标准物质研制[J].食品与机械,39(4): 55.
LIU Tianhe,WEI Ning,WU Caihong,et al. Development of a matrix reference material for amoxicillin in lyophilized bovine milk[J]. Food & Machinery,39(4): 55.
12 李鑫.婴幼儿配方乳粉生产工艺、包装的现状研究[J].中国乳业,2021(5): 85.
LI Xin. Current situation and research on production conditions and packages[J]. China Dairy,2021(5): 85.
引用本文: 段建华,赵静,白艳梅,等 . 乳粉中己烯雌酚分析标准样品的研制[J]. 化学分析计量,2025,34(2): 1. (DUAN Jianhua, ZHAO Jing, BAI Yanmei, et al. Development of standard sample for diethylstilbestrol analysis in milk powder[J]. Chemical Analysis and Meterage, 2025, 34(2): 1.)

来源:化学分析计量