嘉峪检测网 2025-07-08 21:54
导读:根据中国药典通则1101无菌检查法的最新要求,阳性对照试验的频次和必要性需基于质量风险管理的综合评估。以下从法规调整、风险评估维度及执行策略三个方面展开扩展说明。
根据中国药典通则1101无菌检查法的最新要求,阳性对照试验的频次和必要性需基于质量风险管理的综合评估。以下从法规调整、风险评估维度及执行策略三个方面展开扩展说明:
一、法规背景与核心调整
2025年版药典对阳性对照试验的要求从“每批必做”改为基于风险动态调整,与国际药典(如USP、EP)接轨。核心变化包括:
取消强制每批阳性对照:允许实验室通过风险评估减少频次,但需提供充分的数据支持。
抑菌性产品冲洗量限制:总冲洗量从≤1000ml/膜降至≤500ml/膜,且方法适用性验证中即使抑菌性未完全消除,也不得增加冲洗量。
二、阳性对照频次的风险评估维度
1. 产品特性(抑菌性波动及溶解度)
低风险场景:若产品抑菌成分批次间稳定(如已验证含量标准差<5%)且溶解情况较好,且方法适用性试验中冲洗量远低于500ml(如仅需200ml即消除抑菌性),可减少阳性对照频次。
高风险场景:强力抗生素、中药注射剂等如果抑菌性含量波动大的产品,或方法适用性试验需接近500ml冲洗量才能消除抑菌性时,建议每批进行阳性对照。
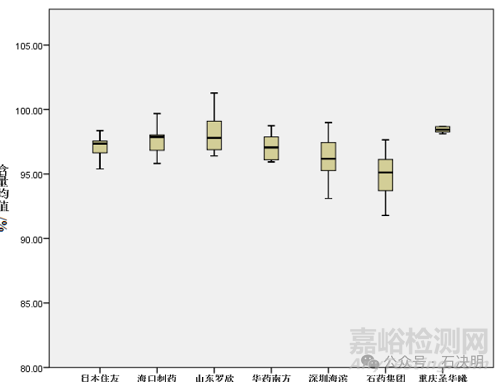
图中是一种三代抗生素的不同公司和内部批次的含量波动情况。所以,首先你需要了解你的产品(尤其是微生物以外的检测结果)。如果溶解情况不好,如果含量波动大,就不用再继续分析了。
2. 方法适用性验证结果
验证中若使用有明确效果(药理作用)的高效中和剂(如β-内酰胺酶)、低吸附滤膜或优化冲洗参数(降低转速、加热冲洗液)后仍抑菌残留,只能寄希望于500ml的冲洗,就需高频次阳性对照;反之若操作简单且抑菌性完全消除,可降低频次。
补充一点,如果方法适用性试验年度确认中有过失败也要高频,因为失败说明验证并不充分。
3. 人员操作与流程复杂度
操作简易性:如冲洗仅需“少量多次加入→抽干”标准动作,无特殊技巧(如无需首次冲洗需要注意溶液路线上下剧烈晃动等等无法描述内容),且人员培训合格率≥95%(通俗的说是个人培训后都会),可减少阳性对照。
高复杂性操作:涉及多次滤膜转移、中和剂浓度调试或冲洗参数动态调整时,需每批阳性对照以监控操作误差。
4. 实验室质量管理水平
高水平实验室(参考指标例如环境监测达标率100%、数据完整性强、偏差率<1%)可基于历史数据(如连续12个月阳性对照合格率100%)减少频次,例如每5批做1次。
管理薄弱实验室(如频繁出现假阴性/假阳性)需维持每批阳性对照。
三、阳性对照频次的执行策略
基于风险动态分级管理,频次可参考以下框架:
|
风险等级 |
评估标准 |
阳性对照频次建议 |
|
低风险 |
抑菌性稳定 + 冲洗量≤300ml + 操作简易 + 实验室管理成熟 |
每10批或每月1次 |
|
中风险 |
抑菌性轻度波动 + 冲洗量300–400ml + 操作需规范 |
每3批或每周1次 |
|
高风险 |
抑菌性波动大/新方法验证/冲洗量≥400ml/操作复杂/实验室曾出偏差 |
每批必做 |
注:频次调整需通过风险评估报告和变更控制程序审批,并定期复核(如每半年)。
结论
“抑菌性稳定、操作简单、管理成熟可减少阳性对照”符合法规精神,但需通过四步落地:
数据积累:分析至少10批产品的抑菌性波动数据和方法适用性冲洗量记录。
风险评估报告:涵盖产品特性、方法验证、人员能力、实验室历史数据等维度。
SOP修订:明确频次规则及触发条件(如方法变更后恢复每批对照)。
持续监控:每季度审查阳性对照结果与环境监测数据,频次调整后首3批需100%阳性对照。
案例:某抗生素企业通过验证酶解法(青霉素酶)将冲洗量从800ml降至200ml,结合人员操作标准化,将阳性对照从每批改为每5批1次,通过药监审计。

来源:Internet