嘉峪检测网 2025-07-17 17:48
导读:近日,北京先瑞达医疗科技有限公司(简称“先瑞达”)宣布,中国国家药品监督管理局(NMPA)正式批准了其自主研发的全球首款椎动脉紫杉醇涂层球囊扩张导管——AcoArt Verbena®的注册申请(国械注准20253031109)。
近日,北京先瑞达医疗科技有限公司(简称“先瑞达”)宣布,中国国家药品监督管理局(NMPA)正式批准了其自主研发的全球首款椎动脉紫杉醇涂层球囊扩张导管——AcoArt Verbena®的注册申请(国械注准20253031109)。
这一创新产品的获批,标志着椎动脉狭窄治疗领域迎来了重大突破,开启了“介入无植入”的新时代。
# “介入无植入”时代
“介入无植入”理念是一种新兴的冠心病介入治疗理念,其核心是在开通和修复病变血管的同时,避免永久性植入器械留存体内,从而使血管最大限度地恢复到原始的健康状态。
这一理念的出现主要是为了解决传统金属支架植入后可能引发的远期问题,如支架内再狭窄、慢性炎症反应、血管弹性受限等。
主要技术手段
生物可吸收支架:这种支架在完成血管支撑任务后会逐渐降解并最终完全消失,避免了永久植入物带来的长期风险。
药物涂层球囊:通过在球囊表面涂覆药物,将药物释放到病变部位,从而抑制血管内膜增生,减少再狭窄的发生。
切割球囊:通过物理切割病变组织,改善血管通畅性。
自灌注药物球囊:在扩张病变部位时,通过球囊上的微通道保持血流灌注,避免了传统药物球囊扩张时血流中断的问题。
优势
无永久植入物:避免了长期植入物可能引发的远期安全性问题。
恢复血管弹性:摆脱了金属支架对血管的“禁锢”,恢复血管对生理刺激的自然反应。
减少炎症反应:无慢性炎症反应的“刺激因子”,有望缩短术后双联抗血小板治疗时间。
不影响后续治疗:不影响可能出现的再次血运重建,也不受影像学检查(如核磁/CT)的限制。
适用人群广泛:特别适用于高出血风险、金属材料过敏等特殊人群。
# 关于AcoArt Verbena®
椎动脉起始段由于血流速度慢、多曲折,是最易形成动脉粥样硬化的部位之一。而椎动脉起始部狭窄(VAOS)则是导致后循环卒中的重要风险因素。
根据相关数据显示,颅外脑血管狭窄的患者中25%-40%发生在椎动脉颅外段,患者首次发病后5年内再次卒中的发生率>25%。针对椎动脉起始部血管狭窄的及时有效治疗对于预防卒中的发生和复发具有重要意义。
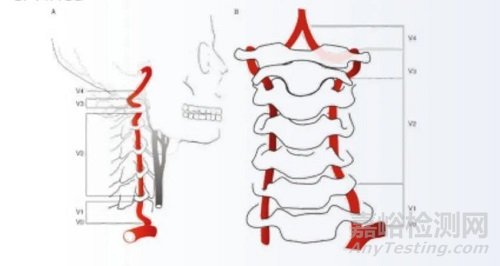
由于椎动脉起始段管径较细,而且位置特殊,肢体经常活动,介入治疗中使用支架的再狭窄发生率比较高:在既往研究中显示,VAOS支架术后再狭窄率可达20-50%,这对VAOS的治疗提出了挑战。
《椎动脉起始部狭窄血管内介入治疗中国专家共识(2024 版)》中提到,现有药物疗法难以根治狭窄,而传统支架植入术后12个月再狭窄率高达26%,且存在支架断裂(发生率4%-25%)等远期并发症。
AcoArt Verbena®是全球首个针对VAOS设计的药物涂层球囊(DCB)产品,适用于狭窄≥70%且药物治疗无效的症状性患者。其通过经皮腔内血管成形术(PTA)局部释放紫杉醇,抑制血管内膜增生,实现“介入无植入”。
AcoArt Verbena®采用了先进的药物涂层技术,通过硬脂酸镁亲脂性基质作为紫杉醇载体,能够有效提升药物涂层的稳定性和药物传输效率。紫杉醇可抑制平滑肌细胞增生,硬脂酸镁(Mg-St)亲脂基质,提升药物组织渗透率与滞留时间,减少脱落风险。
产品优势
介入无植入:无永久金属残留,保留血管生理舒缩功能,降低远期并发症。
简化术后管理:无需长期强效抗凝,减轻患者心理与经济负担。
手术微创化:局部麻醉下操作,缩短住院时间至1-3天。
临床试验结果
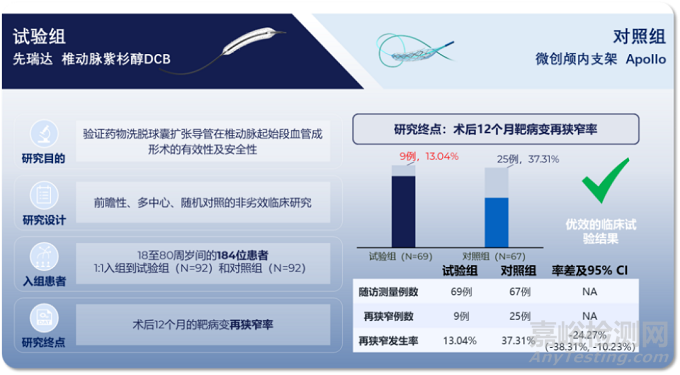
AcoArt Verbena®的临床试验是一项前瞻性、多中心、随机对照研究,共入组了184名患者,按照1:1的比例随机分配到试验组和对照组。
试验组使用AcoArt Verbena®进行治疗,对照组则使用微创的颅内支架Apollo进行治疗。
主要临床终点指标为术后12个月的靶病变再狭窄率。
再狭窄率显著降低:术后12个月靶病变再狭窄率试验组为13.04%,对照组为37.31%(P<0.01),降幅达67%。
安全性保障:无器械相关严重不良事件,避免金属支架长期植入导致的再狭窄、断裂及终身抗凝负担。
# 竞争格局研判
据QYResearch,2023年全球外周DCB市场规模49.1亿元,预计以14.1%年复合增长,2030年将达122.8亿元。国际巨头在椎动脉DCB细分领域尚属空白,而先瑞达于2020年凭借AcoArt Orchid®已占据中国外周DCB市场86.9%份额。当前技术演进呈现两大趋势:向椎动脉/膝下动脉等精细部位延伸,以及药物涂层与可降解支架的复合创新。
在我国 PTCA 球囊扩张导管市场排名前10的企业中,国外企业占据四席,国内企业占据六席,国内企业数量占比多;但从市场份额占比来看,四家国外企业合计占有率达到 60% 以上,特别是波士顿科学与美敦力,合计占有率接近 50%,而国内企业合计占有率在 40% 左右。由此来看,我国 PTCA 球囊扩张导管市场国产化替代空间依然广阔。
从国内外周介入支架和球囊整体市场竞争格局来看,先瑞达在球囊领域占有一席之地,特别是药物涂层球囊(DCB),是该产品领域的细分龙头。未来有望继续凭借性价比和产品性能优势对外资产品进行进口替代。
2025年3月24日,先瑞达医疗科技有限公司发布了其截至2024年12月31日的年度业绩报告。根据报告内容,先瑞达在2024年取得了显著的业绩增长,营业总收入达到5.34亿元人民币,较2023年同比增长12.7%;毛利润4.03亿元人民币,毛利率75.42 %。净利润为5228万元,同比增长260.9%。
核心产品膝上药球实现营收2.67亿元,同比下滑2.8%,占总营收比例约为50.0%;核心产品膝下药球实现营收0.53亿元,同比增长8.8%,占总营收比例约为10.0%。经计算,公司24H2实现营收2.41亿元,同比增长4.7%。
此外,2023年7月,先瑞达宣布与波士顿科学签署了合作框架协议及服务框架协议。根据协议,在国内市场,双方将开展交叉销售的合作模式。双方借由分销对方的产品,可以触达更多新的客户,同时巩固与客户的合作关系。得益于公司依托在外周血管药物球囊领域建立起的先发优势,以及与波士顿科学的合作,可以帮助此次新获批的产品实现快速放量。具体来看,在特定海外市场,波士顿科学拥有对选定的先瑞达产品的独家经销权(首批选定的产品包括外周药物涂层球囊,外周血栓抽吸系统、静脉腔内射频消融系统、冠脉球囊扩张导管等),通过波士顿科学的销售网络,先瑞达产品将进入更广阔的全球市场。
在2023年至2025年间,先瑞达对波士顿科学提供研发支持和CSO服务涉及交易金额的上限为6000万美金、1.1亿美金、1.45亿美金;波士顿科学对先瑞达提供研发支持和CSO服务涉及交易金额上限为5000万美金、9000万美金和1.2亿美金。
在2023年至2025年间,先瑞达采购波士顿科学产品进行销售的交易金额上限为每年200万美元。同时,波士顿科学采购先瑞达产品用于全球销售的交易金额上限分别为2000万美元(2023年)、5000万美元(2024年)和1.1亿美元(2025年)。
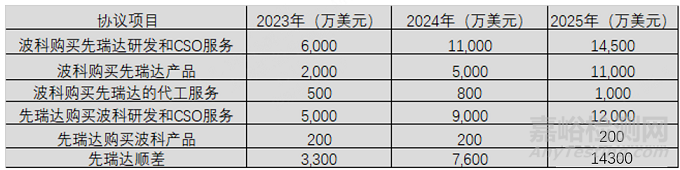
这意味着未来三年内,通过波士顿科学在海外市场的销售,先瑞达有望带来折合人民币约超过 12 亿元的收入。若达到采购上限,双方还可能进一步扩展合作,为先瑞达带来更大的利益。这种合作模式为国产高值耗材企业通过国际巨头“借船出海”提供了先例,同时也为血管介入产品的国际市场扩展打开了新的可能性,展示了通过战略合作以适应全球市场需求的有效路径。

来源:Internet
关键词: 椎动脉药物涂层球囊