嘉峪检测网 2024-10-05 21:11
导读:2024年10月1日,美国食品药品监督管理局(FDA) 将飞利浦Trilogy Evo、Trilogy EV300、Trilogy Evo O2、Trilogy Evo Universal 呼吸机的召回定为 I 级,这是最严重的级别。
2024年10月1日,美国食品药品监督管理局(FDA) 将飞利浦Trilogy Evo、Trilogy EV300、Trilogy Evo O2、Trilogy Evo Universal 呼吸机的召回定为 I 级,这是最严重的级别。
1、再次一级召回呼吸机
飞利浦表示,此次行动涉及Trilogy Evo、Trilogy EV300、Trilogy Evo O2、Trilogy Evo Universal 呼吸机,全球约 90,000 台,其中美国约 67,000 台。受影响的设备存在软件错误,包括输送给患者的氧气显示不准确、误报断电或电池耗尽警报、体积测量不准确等。之前还报告过一个安全问题,涉及内部机器流量传感器上堆积碎片,这可能会部分阻塞压力、体积或气流。
据 FDA 称,这些问题已造成 9 人受伤,1 人死亡。
FDA 表示,飞利浦伟康公司于 7 月 16 日向所有受影响的客户发送了“紧急医疗器械更正更新”,要求他们立即将设备软件更新至最新版本,并遵循用户手册附录,其中要求使用飞利浦认可的微粒过滤器来防止环境污染。
飞利浦在一份声明中表示,已加大力度,加强整个公司的患者安全和产品质量。该公司还指出,7 月份启用了一项重大软件更新,以解决之前的几个安全问题。自 2021 年初以来,飞利浦一直在努力应对涉及数百万台 CPAP 和其他呼吸设备的召回问题。
2、飞利浦召回事件回顾
2021年
2021年4月,飞利浦Respironics首次发现其呼吸机所用的PE-PUR泡沫存在分解问题,可能释放有害气体或颗粒到呼吸机的空气通道中,对使用者构成潜在危险。
2021年6月,飞利浦Respironics发布了第一次全球性的召回通知,涉及其部分呼吸机和双水平气道正压通气(BiPAP)设备。召回原因正如4月所报告中所述那样。
2021年7月,飞利浦Respironics进一步扩大了呼吸机产品的召回范围,包括更多的生产日期和型号,原因与第一次召回一致。与此同时,FDA也首次发布通知,将飞利浦的召回列为1级召回。飞利浦也因此停止接受睡眠治疗系统的订单。
2021年8月,FDA宣布了另一起关于飞利浦Respironics呼吸设备的严重召回。这次飞利浦召回了配备高流量治疗软件3.00和3.10版的V60和V60 Plus呼吸机。原因是这批呼吸机因为没有解决导致最大系统压力的问题,可能导致严重的不良事件,甚至有死亡风险。
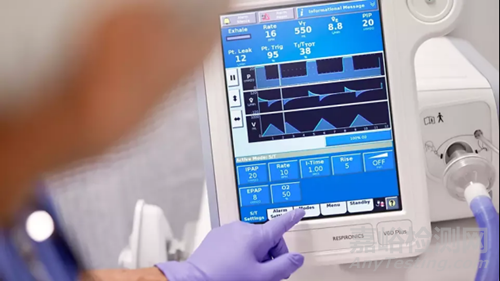
飞利浦 V60 PLUS
2022年
2022年1月,飞利浦Respironics召回某些Trilogy EVO呼吸机,原因与第一次召回一致。
2022年3月,飞利浦Respironics再度召回某些V60和V60 Plus呼吸机,因为有一部分设备中,内部电路使用了过期粘合剂组装,有导致呼吸机停止工作的风险。
2022年8月,FDA表示,它已经收到了69,000份与声音消减泡沫召回相关的医疗设备报告(MDRs),其中168份报告了死亡。
2022年9月,飞利浦Respironics呼吸设备再次召回获得I类标签。该召回涉及从2020年8月6日到2021年9月1日分发的386台呼吸机。BiPAP机器的电机中可能含有塑料,可能会释放挥发性有机化合物 (VOC)。除了用户吸入危险 VOC 的风险外,塑料还可能导致设备故障。

飞利浦BiPAP设备
2022年10月,FDA再发一级召回通告,警告购买了CPAP或BiPAP治疗面罩的用户,称面罩的带子可能会与植入式金属医疗设备产生负面的相互作用,并表示已经收到了14分相关报告。而当时飞利浦Respironics已经分发了超过1700万个面罩。
2022年11月,FDA指出,飞利浦Respironics更换过的部分呼吸机存在新的潜在问题,可能出现消音泡沫松动,并要求用户停止使用这些设备,联系飞利浦进行更换或修理。这次召回涉及到的呼吸机型号为Trilogy 100/200。
随着召回事件不断发酵,飞利浦Respironics召回的设备数量从最初的20万台扩大至550万台。远高于最初估计的300万至400万台。
2023年
2023年2月,飞利浦Respironics再次对Trilogy 100、Trilogy 200和Garbin Plus三个系列的呼吸机产品召回,召回原因主要与之前召回呼吸机所要替换的硅胶泡沫质量有关。
2023年4月,飞利浦Respironics再次召回此前召回并修理过的部分CPAP和BiPAP设备,原因是它们可能提供不准确或不充分的治疗。
2023年8月,飞利浦Respironics的第11次召回开始。这次的I级召回涵盖了美国的73,000台飞利浦Respironics三部曲Evo,Evo O2,EV300和Evo通用呼吸机。
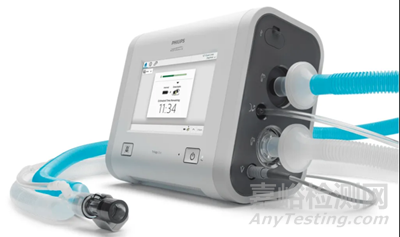
截至2023年8月底,FDA已经收到了10.5万份问题报告,其中包括与泡沫降解问题相关的385起死亡报告。
2024年
2024年5月,飞利浦表示,该公司已在美国就呼吸机引发的人身伤害案件达成一项11亿美元的和解协议。和解的消息传出后,该公司的股价飙升了46%。
飞利浦表示已与原告达成和解协议,“解决人身伤害诉讼和医疗监测集体诉讼,以结束与美国诉讼相关的不确定性”,并补充说,它不“承认任何过错或责任,也不承认任何伤害是由伟康的设备造成的。”
“对患者的睡眠治疗设备的修复工作基本完成了,迄今为止的测试结果表明,使用这些设备预计不会对健康造成明显的损害。”飞利浦首席执行官罗伊·雅各布斯在公司声明中表示。“我们对患者可能经历的担忧感到遗憾,”他说。
最新的和解协议涵盖了美国的集体诉讼以及个人人身伤害索赔。飞利浦表示,和解金预计将在2025年支付,将通过产生的现金流来支付。
面临长达三年的召回事件,飞利浦经过了一系列调整,也产生了一系列的正面影响。那么本次的召回会对飞利浦有怎样的影响呢?器械之家将持续关注。

来源:器械之家
关键词: 呼吸机