嘉峪检测网 2025-02-13 08:24
导读:建立高效液相色谱法测定异丙醇-水溶液中利血平含量。
摘 要: 建立高效液相色谱法测定异丙醇-水溶液中利血平含量。采用Eclipse Plus C18色谱柱(150 mm×4.6 mm,5 μm)分离,以甲醇-水溶液(体积比为8∶2)作为流动相等度洗脱,采用波长为268 nm的二极管阵列检测器,流量为0.5 mL/min,柱温为40 ℃。利血平的质量浓度在0.2~10 μg/mL范围内与色谱峰面积线性关系良好,相关系数为0.999 9,检出限为0.05 μg/mL。利血平的加标回收率为100.20%~100.39%,测定结果的相对标准偏差为0.43%~0.81%(n=6)。该方法简单可靠,重复性好,适用于异丙醇-水溶液中利血平含量的测定。
关键词: 利血平; 高效液相色谱法; 异丙醇-水溶液; 方法验证
利血平是从萝芙木属多种植物中提出的一种吲哚型生物碱[1],具有降低血压、减缓心率和抑制中枢神经系统等作用[2],由于其降压效果显著、价格低廉而深受高血压患者青睐。
高效液相色谱法是一种以液体作为流动相的分离与分析方法,具有强选择性、高准确性、可量化和定量分析等优点[3-4],在分离、鉴别和定量目标组分方面发挥了重要作用。
目前对利血平含量的检测方法主要包括分光光度法[5]、液相色谱-质谱联用法[6]、高效液相色谱法[7]等。其中分光光度法操作简单、成本低,但需加耦合试剂进行显色反应后才能进行检测,前处理方法复杂;液相色谱-质谱联用法方法快速、准确,能同时进行定性、定量分析,但对设备和操作技术要求较高,费用大;高效液相色谱法精密度高,准确性强,方法简便、选择性好、操作方便,是研究者的首选方法。目前对于利血平检测方法的优化研究仅包含波长、色谱柱、流动相、柱流速和柱温中的一项或几项,尚未有文献专门针对利血平的最优色谱条件进行全面的分析。
笔者采用高效液相色谱法对利血平含量的测定进行了以上五个方面的优化。以异丙醇-水溶液为溶剂,建立了一种简单、高效、准确可行的分析方法。该方法可用于异丙醇-水溶液中利血平标准物质均匀性及稳定性的检测,确保标准物质的量值不受方法影响,同时为今后利血平的检测提供了数据支撑和理论依据。
1、 实验部分
1.1 主要仪器与试剂
高效液相色谱仪:1260 Infinity型,二极管阵列检测器,美国安捷伦科技有限公司。
电子天平:ME235S型,感量为0.01 mg,赛多利斯科学仪器(北京)有限公司。
甲醇、乙腈:均为色谱纯,德国默克公司。
异丙醇:质谱纯,德国默克公司。
利血平纯度标准物质:纯度(质量分数)为99.3%,U=0.5%,k=2,标准物质编号为GBW (E)090901,广东省计量科学研究院。
超纯水机:Milli-Q系统,美国密理博公司。
异丙醇-水溶液:异丙醇与水的体积比为1∶1。
1.2 色谱条件
色谱柱:Eclipse Plus C18柱(150 mm×4.6 mm,5 μm,美国安捷伦科技有限公司);柱温:40 ℃;进样体积:20 μL;流动相:甲醇-水溶液(体积比为8∶2,下同);洗脱方式:等度洗脱;柱流量:0.5 mL/min;检测器:二极管阵列检测器(DAD检测器);检测波长:268 nm。
1.3 溶液配制
标准储备溶液:控制室温为(20±2) ℃,准确称取10.12 mg的利血平纯度标准物质,根据重量-容量法,用异丙醇-水溶液将其稀释至100 mL,制得质量浓度为100 µg/mL的标准储备溶液。
利血平样品溶液:准确移取2 mL标准储备溶液于200 mL容量瓶中,用异丙醇-水溶液稀释至标线,制得质量浓度为1 µg/mL的利血平样品溶液。
空白溶液:精密移取同体积的异丙醇与超纯水于容量瓶中,混合均匀。
系列标准工作溶液:移取标准储备溶液,通过重量法将其逐级稀释,制得质量浓度分别为0.2、0.5、1.0、5.0、10.0 μg/mL的系列标准工作溶液。
1.4 实验方法
首先根据二极管阵列检测器的光谱扫描,选择最佳吸收波长,采用单因素实验进行条件分析,通过分析色谱柱的类型、流动相的种类及比例、柱流速及柱温,根据样品与杂质的分离度、色谱峰面积的大小和出峰时间的长短等,依次选择最优分析条件[8]。为确保优化后的分析条件准确可靠,还需对优化后的条件进行验证。通过方法学试验[9-11]进行考察,验证优化后的分析条件是否可行。
2、 结果与讨论
2.1 分析方法优化
2.1.1 波长的选择
选择光谱扫描模式,在波长为190~400 nm条件下,对利血平溶液进行全扫描。利血平样品溶液在不同波长下的光谱图如图1所示,从图1中可以看出,溶液在218、268、292 nm处均有强吸收。由于292 nm处是肩峰,溶剂在低波段218 nm处有紫外吸收,易对检测结果产生影响,且在该波段基线噪声和漂移相对较大,杂质峰较多,因此218 nm和292 nm均不适合作为分析条件[12]。波长为268 nm时峰形平缓,干扰相对较少,因此选择检测波长为268 nm。
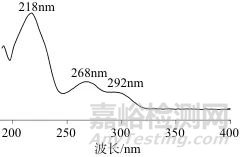
图1 利血平样品溶液在不同波长下的光谱图
Fig. 1 Spectrogram of reserpine sample solution at different wavelengths
2.1.2 色谱柱的选择
设置波长为268 nm,考察SB-C18(250 mm×4.6 mm,5 μm)、Eclipse Plus C18(150 mm×4.6 mm,5 μm)、Poroshell 120 EC-C18(150 mm×4.6 mm,4 μm)3种不同类型的色谱柱的分离效果,分离色谱图如图2所示。从图2中可以看出,由于SB-C18的色谱柱较长,利血平的出峰时间较长(12.33 min),同时相比较其他两个色谱柱,色谱峰面积也较小,峰形较差,有拖尾。Eclipse Plus C18和Poroshell 120 EC-C18 2种色谱柱的出峰时间和峰面积相差不大,Eclipse Plus C18的出峰时间稍短,面积稍大,且峰形相对于Poroshell 120 EC-C18较好,因此最终选择色谱柱为Eclipse Plus C18色谱柱。
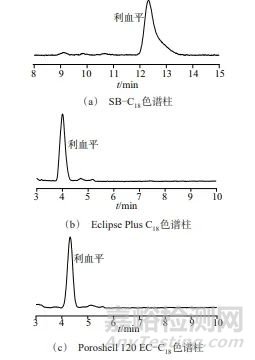
图2 不同型号色谱柱的分离色谱图
Fig. 2 Separation chromatogram of different types of column
2.1.3 流动相的选择
流动相的选择直接影响色谱峰的分离度[13],选择合适的流动相,既要将色谱峰与杂质峰完全分离开,又要尽可能缩短检测时间,增大峰面积。
根据文献[14-16]知,利血平检测的流动相种类一般为甲醇-水或乙腈-水体系。考察流动相为甲醇-水(9∶1,体积比,下同)、甲醇-水(8∶2)、乙腈-水(8∶2)、乙腈-水(7∶3)时的分离效果。结果表明,随着甲醇或乙腈比例的降低,出峰时间逐渐增长,在流动相为甲醇-水(9∶1)和乙腈-水(8∶2)时,利血平的峰与杂质峰未能分开,且峰型较差,峰有前伸或者拖尾;流动相为甲醇-水(8∶2)和乙腈-水(7∶3)时,利血平色谱峰较平缓,峰型较好。其中流动相为甲醇-水(8∶2)时,峰面积略大,出峰时间较短,因此选择甲醇-水(8∶2)作为流动相。
2.1.4 柱流量的选择
柱流量的大小直接影响色谱峰的出峰时间和峰面积。其他初始条件不变,考察不同柱流量(0.25、0.50、0.75、1.00 mL/min)时的色谱分离情况。结果表明,随着流量的减小,出峰时间逐渐增长,色谱峰形渐宽,峰面积逐渐增大,峰面积的大小受流量影响显著。柱流量为0.25 mL/min时出峰时间长导致峰形太宽,影响分离效果。综合考虑,最终选择柱流量为0.50 mL/min。
2.1.5 柱温的选择
由于液相色谱柱的寿命一般在40 ℃下可保持最优,考察色谱柱的柱温为30、35、40 ℃时色谱柱的分离情况,结果表明,随着柱温的升高,出峰时间相差不大,峰面积逐渐增大,因此最终选择色谱柱的柱温为40 ℃。
2.2 专属性试验
在1.2仪器工作条件下,将空白溶液、样品溶液以及标准物质对照品进样测定,色谱图如图3所示。从图3中可以看出,空白溶液对测定结果无干扰,对照溶液和样品溶液对应峰的保留时间一致,该方法专属性良好。
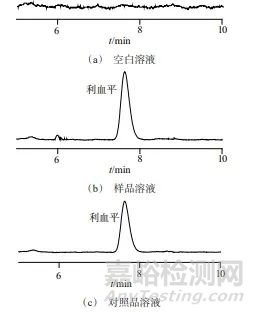
图3 空白溶液、样品溶液和对照品溶液色谱图
Fig. 3 Chromatogram of blank solution,sample solution and control solution
2.3 分析方法验证
2.3.1 线性关系及检出限
将系列标准工作溶液在1.2仪器工作条件下进行分析,以质量浓度(x)为横坐标,色谱峰面积积分值(y)为纵坐标,绘制标准工作曲线。按信噪比为3对应的利血平浓度确定方法检出限,信噪比为10对应的利血平浓度确定方法定量限。结果表明,利血平的质量浓度在0.2~10 μg/mL范围内与色谱峰面积线性关系良好。利血平溶液的线性方程为y=55.453x-6.906 6,相关系数为0.999 9。方法检出限为0.05 μg/mL,定量限为0.16 μg/mL。
2.3.2 加标回收和精密度试验
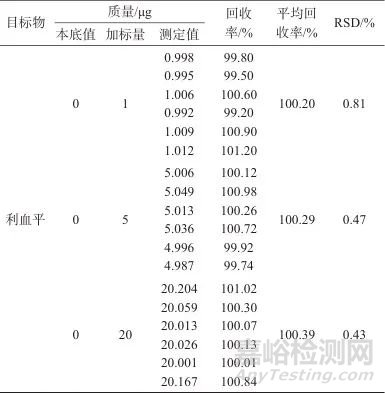
选取异丙醇-水溶液空白样品,分别置于容量瓶中,6份为一组,分别加入标准储备溶液50、250、1 000 μL,制得加标量分别为1、5、20 μg 3个加标水平的加标样品溶液,每个加标水平平行测定6次,在1.2仪器工作条件下进行分析。加标回收及精密度试验结果见表1。由表1可知,利血平溶液的平均回收率为100.20%~100.39%,相对标准偏差为0.43%~0.81%(n=6)。表明该方法的精密度良好、准确可靠。
表1 加标回收和精密度试验结果
Tab. 1 Results of standard recoveries and precision test
2.3.3 稳定性试验
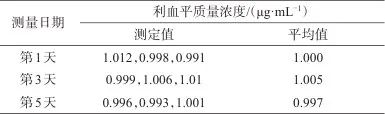
在1.2仪器工作条件下,在不同的时间内测定相同浓度的异丙醇-水溶液中利血平。每个样品测量3次,取平均值为最终测量结果,测量时间为5天,每隔两天测量一次,稳定性试验结果见表2。由表2可知,在不同的时间内测量结果未发生明显变化,表明该方法的稳定性良好。
表2 稳定性试验结果
Tab. 2 Results of stability test
3、 结语
通过色谱条件的优化,建立了高效液相色谱法测定异丙醇-水溶液中利血平,该方法精密度高、准确度高、稳定性强,可为今后利血平溶液的检测提供科学依据和参考。
参考文献:
1 王顺民,杨晓丹,曾勇,等.利血平对大鼠主动脉血管平滑肌细胞自噬的影响[J].中国医药导报,2020,17(16):4.
WANG Shunmin,YANG Xiaodan,ZENG Yong,et al. The effect of reserpine on autophagy of rat aortic smooth muscle cells[J]. Chinese Medical Journal,2020,17(16):4.
2 邓映明,吴仪,张雁,等. HPLC法测定复方双嗪利血平片含量均匀度及溶出度[J].广东化工,2022,49(21):209.
DENG Yingming,WU Yi,ZHANG Yan,et al. Determination of content uniformity and dissolution of Compound Dipyrizine and Levofloxacin Tablets by HPLC [J]. Guangdong Chemical Industry,2022,49(21):209.
3 杨慧.高效液相色谱仪在食品检测中的应用[J].中国食品工业,2023(18):82.
YANG Hui. Application of high performance liquid chromatography in food detection[J]. China Food Industry,2023 (18):82.
4 亓秀华.高效液相色谱法在药品成分分析中的应用及优化研究[J].当代化工研究,2024(3):123.
QI Xiuhua. Application and optimization of high performance liquid chromatography in drug component analysis[J]. Contemporary Chemical Research,2024(3):123.
5 龙绛雪,蒋太煜,徐文宣,等.云南萝芙木中利血平含量测定方法的建立[J].西部林业科学,2014,43(1):110.
LONG Jiangxue,JIANG Taiyu,XU Wenxuan,et al. Establishment of a method for determining the content of reserpine in Yunnan Luofu wood[J]. Western Forestry Science,2014,43(1):110.
6 樊磊磊,刘乃强,李振国. UPLC-MS/MS定性定量检测清脑保心康胶囊中非法添加的利血平[J].中国医药指南,2012,10(34):10.
FAN Leilei,LIU Naiqiang,LI Zhenguo. Qualitative and quantitative detection of illegally added reserpine in Qingnao-baoxinkang Capsules by UPLC-MS/MS [J]. Chinese Medical Guidelines,2012,10(34):10.
7 钱敏,宋冬梅,凌霞,等. HPLC法同时测定复方利血平片中7个成分的含量[J].药物分析杂志,2022,42(7):1 110.
QIAN Min,SONG Dongmei,LING Xia,et al. Simultaneous determination of seven components in compound reserpine tablets by HPLC [J]. Journal of Drug Analysis,2022,42(7):1 110.
8 李锋丽,邱黛君,杨中元,等.甲醇中灭幼脲和除虫脲溶液液相色谱仪分析方法的研究[J].工业计量,2023,33(1):9.
LI Fengli,QIU Daijun,YANG Zhongyuan,et al. Study on the liquid chromatography analysis method of chlorpyrifos and pyrethroid solutions in methanol[J]. Industrial Metrology,2023,33(1):9.
9 刘贝妮,王志伟,吴晗,等.敌草快及敌草快二氯盐中2,2'-二联吡啶的高效液相色谱分析方法研究[J].世界农药,2023,45(12):45.
LIU Beini,WANG Zhiwei,WU Han,et al. Analysis method of 2,2'-dipyridyl in diquat dibromide and diquat dichloride by HPLC[J]. World Pesticide,2023,45(12):45.
10 郑杨,李岩.3%氯氟吡啶酯乳油高效液相色谱分析方法研究[J].农药科学与管理,2023,44(6):22.
ZHENG Yang,LI Yan. Study on the high performance liquid chromatography analysis method of 3% chlorofluoropyridine ester emulsion[J]. Pesticide Science and Management,2023,44(6):22.
11 王立新,崇小萌,姚尚辰,等.阿莫西林克拉维酸钾制剂中有关物质超高效液相色谱分析方法的建立[J].中国药物评价,2021,38(4):294.
WANG Lixin,CHONG Xiaomeng,YAO Shangchen,et al. Establishment of ultra-high performance liquid chromatography analysis method for related substances in amoxicillin and clavulanate potassium preparations[J]. China Drug Evaluation,2021,38(4):294.
12 张慧颖,龚云麒,蔡传涛,等.高效液相色谱法测定萝芙木中利血平的含量[J].云南中医学院学报,2007,30(2):7.
ZHANG Huiying,GONG Yunqi,CAI Chuantao,et al. Determination of reserpine content in Lophus chinensis by high-performance liquid chromatography[J]. Journal of Yunnan University of Traditional Chinese Medicine,2007,30(2):7.
13 蔡玮,吴红,赵海波.高效液相色谱仪测定萘色谱分析方法[J].计量技术,2019(10):28.
CAI Wei,WU Hong,ZHAO Haibo. High performance liquid chromatography for the determination of naphthalene chromato-graphic analysis method[J]. Metrological Technology,2019,(10):28.
14 乔冰. HPLC法测定利血平注射液的含量[J].黑龙江科技信息,2011(29):39.
QIAO Bing. Determination of the content of reserpine injection by HPLC [J]. Heilongjiang Science and Technology Information,2011(29):39.
15 张玉娟,张晓明,张柏桃. HPLC同时测定复方利血平片中5个成分的溶出度[J].华西药学杂志,2023,38(1):100.
ZHANG Yujuan,ZHANG Xiaoming,ZHANG Botao. Simultaneous determination of the dissolution of five components in Compound Reserpine Tablets by HPLC [J]. Huaxi Pharmaceutical Journal,2023,38(1):100.
16 赵成瑞,王勇,王哲焱.生物检材中利血平的高效液相色谱/质谱和高效液相色谱的检测[J].临床医药实践,2010,19(3):90.
ZHAO Chengrui,WANG Yong,WANG Zheyan. Detection of reserpine in biological samples by high-performance liquid chromatography/mass spectrometry and high-performance liquid chromatography[J]. Clinical Medical Practice,2010,19(3):90. 上接第78页)
17 邱明鸣,朱育凤,倪昌荣.高效液相色谱法同时测定前胡药材中白花前胡甲素和白花前胡乙素含量[J]. 中国药业,2022,31(11):70.
QIU Mingming,ZHU Yufeng,NI Changrong. Simultaneous determination of praeruptorin A and praeruptorin B in Peucedani Radix by HPLC [J]. China Pharmaceuticals,2022,31(11):70.
18 高平,牛亚静.高效液相一测多评法同时测定参苏片中葛根素,迷迭香酸,白花前胡甲素,白花前胡乙素,白花前胡E素的含量[J].中国药师,2020,23(2):132.
GAO Ping,NIU Yajing. Simultaneous determination of puerarin,rosmarinic acid,Praeruptorin A,Praeruptorin B and Praeruptorin E in Shensu Tablets by HPLC-QAMS [J]. China Pharmacist,2020,23(2):132.
19 赵万晴,戚继红.高效液相色谱法同时测定止咳片中白花前胡甲素和白花前胡乙素含量[J].中国药业,2016,25(21):60.
ZHAO Wanqing,QI Jihong. Simultaneous content determination of Praeruptorin A and Praeruptorin B in Zhike Tablets by HPLC[J]. China Pharmaceuticals,2016,25(21):60.
20 胡志军,陈建秋. HPLC测定不同基原陈皮药材中橙含量[J].中国实验方剂学杂志,2012,18(10):95.
HU Zhijun,CHEN Jianqiu. Content determination of hesperidin from different kinds of pericarpium citri reticulatae by HPLC [J]. Chinese Journal of Experimental Traditional Medical Formulae,2012,18(10):95.
21 于霞,吴娟,姜雪,等. HPLC法同时测定消乳散中甘草苷、橙皮苷和甘草酸铵的含量[J].沈阳药科大学学报,2017,34(5):369.
YU Xia,WU Juan,JIANG Xue,et al. Simultaneous determination of Liquiritin,Hesperidin and Ammonium Glycyrrhetate in Xiaorusan by HPLC [J]. Journal of Shenyang Pharmaceutical University,2017,34(5):369.
22 赵磊,孙艳涛,张晗,等.高效液相色谱法测定武力拔寒散中橙皮苷的含量[J].化学分析计量,2017,26(3):50.
ZHAO Lei,SUN Yantao,ZHANG Han,et al. Determination of Hesperidin in Wuli Bahan Powders by high performance liquid chromatography[J]. Chemical Analysis and Meterage,2017,26(3):50.
引用本文: 王晓冰,宋增良,郭硕 . 高效液相色谱法测定异丙醇-水溶液中利血平[J]. 化学分析计量,2024,33(11):102. (WANG Xiaobing, SONG Zengliang, GUO Shuo. Determination of reserpine in isopropyl alcohol-aqueous solution by high performance liquid chromatography[J]. Chemical Analysis and Meterage, 2024, 33(11): 102.)

来源:化学分析计量