嘉峪检测网 2025-02-25 18:30
导读:从冷冻干燥技术的原理、影响因素、FD技术在不同类型疫苗中的研究以及未来发展趋势等方面进行了全面、系统的综述,以期为疫苗研究和疫苗产业化的进一步发展提供有益的信息和思路。
随着生物技术的飞速发展,疫苗在预防和控制传染病方面的作用越发显著,广泛的疫苗接种对全球健康至关重要。然而,在中等及低收入国家,要提高疫苗接种覆盖率还存在重大挑战。由于液体疫苗存在易分解、热稳定性差、冷链配送成本高昂等不足,限制了疫苗在这些地区的分发和接种,使一些传染性疾病在偏远地区得不到有效控制。为了保证疫苗的稳定性和有效性,冷冻干燥(freeze-drying,FD)技术成为疫苗制备和保藏的关键技术之一。从冷冻干燥技术的原理、影响因素、FD技术在不同类型疫苗中的研究以及未来发展趋势等方面进行了全面、系统的综述,以期为疫苗研究和疫苗产业化的进一步发展提供有益的信息和思路。
疫苗在传染病的预防和控制中发挥着重要作用。然而,疫苗的稳定性给疫苗的使用带来极大的挑战,在疫苗的储存和运输过程中,温度、湿度、机械应力等多种因素都可能导致疫苗效力的下降或失活[1]。注射是疫苗接种常用的方法,因而疫苗通常制备成水溶液形式。然而,液体疫苗存在易水解、稳定性差、保存期短且需要冷藏等劣势。固态疫苗在一定程度上抑制了疫苗的不稳定性,既保留了原有的生物活性[2],又具有良好的再水化能力,便于储存和运输。传统的干燥方法,在干燥过程中易造成疫苗活性的降低,因此在20世纪50 年代,科学家们开始采用冷冻干燥(freeze-drying,FD)技术[3]。FD 技术可以有效克服疫苗中抗原成分的热力学不稳定性,为疫苗制剂提供了一种有效的制备方法,以保证制剂制备和储存中物理化学性质的稳定,是目前常用的生物制品干燥方法[4]。FD 技术通过溶剂冻结和干燥两个过程实现物质的干燥,冷冻干燥后的疫苗能在常温下有效保存,有利于疫苗的储存和运输。目前,FD技术已在多种生物制品(包括疫苗)研发中得到广泛应用。本文旨在对 FD 技术在疫苗制备中的原理、影响因素、疫苗制备的研究进展进行综述,以期为FD技术在推动疫苗研发、改进疫苗储存和使用条件,及未来疫苗的接种和疾病预防方面提供更可靠的支持和保障。
1.冷冻干燥技术
冷冻干燥技术(FD)指将液态物质冻结,并在真空条件下,将冻结的水分直接从固态转变为气态,从而去除样品中的水分。FD技术可以有效地保留原材料的物理、化学、生物学特性,同时延长保存期限,在医药、食品、生物技术等领域应用广泛。相较于传统的干燥方法,FD被认为是一种较为温和的方法。传统的干燥方法在去除物质中的水分时,会使用较高热量,易使温度敏感的成分失活,而FD则通过低温固态条件下去除水分,同时有效地保留产品的结构和活性成分。FD技术过程包括样品预处理、冷冻、主干燥、次干燥和包装等步骤。
1.1FD技术的原理
FD过程可以分为冷冻阶段、主干燥阶段和次干燥阶段。在冷冻阶段,物质中的水由液态变为固态。在主干燥阶段,在真空泵的作用下系统内部产生低压环境,样品中的冰晶会直接经历升华,由固态变为气态,冰晶在较低的温度下升华,从而减少样品常温干燥降解变性的风险。在次干燥阶段,进一步去除残留的水分或其他溶剂,以确保样品或产品的彻底干燥和稳定[5]。次干燥有助于提高产品的储存寿命,减少微生物生长的可能性,有利于长期保持产品的质量[6]。
1.2FD技术的影响因素
FD 技术是疫苗制备过程中最实用的干燥技术之一,能够制备出高稳定性的冻干样品,尤其适合处理不耐热材料。然而,FD技术的最终产品受到多种因素的影响,包括冻干过程中的冷冻温度、冷冻速度、初级干燥条件、次级干燥条件以及样品配方选择。通过对这些因素进行优化,能够进一步提高冻干产品的质量和稳定性。
1.2.1 冷冻温度
冷冻温度对疫苗样品中水分子的结构和运动状态具有重要影响。选择适当的冷冻温度是FD过程的关键初始条件。FD通常要求将样品冷冻至低于玻璃化转变温度(glass transi⁃tion temperature,Tg)。Tg 是指材料在冷冻过程中转变为玻璃态的温度,而玻璃态温度是非晶态聚合物的固有特性。在玻璃态温度下,材料内部的物质无法流动或变形,类似于固体状态。当温度超过玻璃态温度时,材料会变得柔软并具有流动性。玻璃化温度取决于样品的组成和性质,不同样品具有不同的玻璃化温度。一般来说,疫苗的玻璃化温度范围在−40~−60 ℃之间,将样品冷冻至低于玻璃化温度可以减少冻结过程对样品结构的破坏和水分的损失,有利于后续的干燥步骤和样品质量的保持。此外,研究还发现,预冷冻温度对某些细菌菌株干燥后的存活率具有重要影响。在使用磷酸缓冲盐水溶液和山梨醇作为保护剂的情况下,对 AR113、AR307 和 WCFS1 菌株进行不同预冷冻温度的试验,结果显示不同菌株在不同温度下的预冷冻能够实现最佳存活率。例如,AR113 菌株在−196 ℃的预冷冻温度能够获得最高的存活率,而AR307和WCFS1菌株最佳的预冷冻温度分别是−40 ℃和−20 ℃[7]。
1.2.2 冷冻速率
冻结速率可以影响样品的结晶形态、溶剂的迁移和整体干燥时间。快速冷冻使样品形成均匀分布的冰晶,有利于保持样品的活性和质量。快速冷冻还能使样品迅速从游离水中快速冻结为固态,减少热变性并防止真空干燥过程中的起泡现象。但快速冷冻后,易造成后续升华形成小的空隙,导致升华速度较慢。有研究表明,通过控制较小程度的超冷冷却、较慢的冷冻速率,可以实现最佳的冷冻条件,从而获得最小总表面积的大冰晶,同时可以显著缩短一次干燥时间,并获得外观和形态更好的冻干产品[8]。也有研究表明,慢速冷冻会导致冰晶的尺寸增大,从而增加样品中冻结损伤和溶解损伤的风险。此外,慢速冷冻还会导致溶液中溶质的浓度变化,可能对样品的稳定性产生负面影响。缓慢冷冻形成的大冰晶和空隙,具有较小的表面积,导致在初级干燥期间质量传递阻力降低、干燥速度加快。但是大的孔隙尺寸减少了可用于非冰冻溶剂扩散的表面积,在次级干燥阶段又会限制解吸速率,不利于热传递[9]。
1.2.3 初级干燥过程中的真空度、温度和时间
与冷冻阶段相比,初级干燥阶段的真空度、温度和时间对冻干产品的最终质量具有重要影响。初级干燥是在低温低压条件下进行的,通过提供适当的低压和足够的热量,以实现冻结的结晶水的升华并去除。这一步骤主要包括降低腔室压力(chamber pressure,Pc)和逐步提高托盘温度(shelftemperature,Ts),但保持样品在 Tg 或临界温度(critical temperature,Tc)以下,且压力应低于目标温度下冰的蒸汽压力,以保证样品的质量和外观[10]。FD 过程中真空度和干燥温度是重要的影响因素,会影响 FD 产品的冻干时间和设备能耗,适当的干燥温度可以促进传热和促使冰晶升华,适当的低真空度可以提供足够的气压差和真空吸力,加速水分的脱除。然而,过低的真空度会导致水分子升华速度减慢,干燥过程变慢,整个 FD 过程的时间延长,从而增加能耗。而过高的真空度可能会给真空泵和其他设备带来过度负荷,影响设备的寿命和性能,并降低传统FD中样品的气流传热效率,反而降低了升华效率。
1.2.4 次级干燥中的真空度、温度和时间
在次级干燥阶段,通过蒸发使残留在样品中的水分子和构成抗原水合层的水分子去除。通常,在次级干燥中,货架温度要高于初次干燥,而压力则要低于初次干燥压力。由于湿度的逐渐降低,冷冻浓缩物的玻璃化转变温度也会逐渐增加。因此,为了节省时间和防止样品的聚集,温度可以逐渐升高(但必须低于Tg),以提高干燥效率[11]。Assege⁃hegn 等[12]以费森尤斯卡比公司的药物配方为案例,优化了 FD 过程中的次干燥步骤,并研究了干燥温度、干燥时间、小瓶位置和腔室压力对含湿量和玻璃化转变温度的影响。结果显示,在较短的干燥时间内,干燥温度对样品含水量和玻璃化转变温度的影响较大,增加干燥温度可以显著缩短达到设计含水量和玻璃化转变温度所需的干燥时间。腔室压力从 0.05~0.40 m 的变化对含水量和玻璃化转变温度的影响微乎其微。研究还发现,在次级干燥中,瓶子的热质量在干燥物的温度上起着主要作用,约有 95% 的热量被瓶壁吸收,从样品表面解吸出的结合水分子的过程只受到温度的影响[13]。
1.2.5 配方
样品的配方是影响 FD 的关键因素之一。在FD中,配方的组成和浓度会影响样品的稳定性,配方的选择会直接影响冻干样品最终的质量特性。选择适当的冷冻保护剂,如蔗糖、海藻糖、乳糖等多糖类物质,可以减轻冻结和干燥过程中疫苗活性的损失。此外,在 FD 过程中,应充分考虑疫苗和冻结保护剂的浓度及比例,以达到最优保护效果。在新型冠状病毒(corona virus dis⁃ease 2019,COVID-19)mRNA 脂质纳米颗粒(lipidnanoparticle,LNP)疫 苗 的 优 化 研 究 中 ,Meule⁃waeter等[14]发现脂质体和核酸的配比显著影响冻干后 mRNA 疫苗的封装效率。尤其是当脂质:mRNA 质量比为 20∶1 时,冻干后的 mRNA 疫苗的封装完整性达到最佳状态。另外,在冻干过程中使用优化的辅料(如 Tris 或磷酸盐以及 12.5 mol·L−1蔗糖)可以使冻干的 mRNA 疫苗达到最佳热稳定性,在 4、22 和 37 ℃条件下,至少可以保持 12 周,而免疫效果无明显变化。
目前,小干扰RNA(small interfering RNA,siRNA)被认为是一种有希望治疗慢性乙型肝炎的方式,有望达到潜在的治愈效果。Huang 等[15]开发了一种名为 RBP131的新型可离子化脂质纳米粒子以及先进的 siRNA 冻干技术,用于将针对载脂蛋白 B(apolipoprotein-B,Apo-B)的 siRNA 输送至肝细胞。他们利用FD技术对RBP131/siRNA脂质体制剂进行处理,通过调整冻干条件,使用蔗糖作为保护剂,建立了一套优良的冻干工艺。经过冻干的 RBP131/siRNA 脂质体可以在−20、4或25 ℃条件下储存,并且在1、2、3和4周后重新溶解,其外观、封装率、粒径、聚分散指数和电位等质量控制参数与液体制剂一致,可满足临床应用期间的储存和运输需求。Chen等[1]在多种配方中筛选出一种重组靶向肿瘤的天花病毒疫苗(recombi⁃nant tumor-targeted vaccinia virus expressing ovalbu⁃min,rTTV-OVA)和腺病毒疫苗(adenovirus serotype5 expressing envelope protein, Ad5-ENV)冻干配方,包括牛血清白蛋白(bovine serum albumin,BSA)、L-谷氨酸(L-Glu)、聚乙二醇(polyethylene glycol,PEG)和右旋糖酐(dextran,DEX),旨在提高疫苗的热稳定性和活性。通过比较 5 种不同的配方,发现配方#2(PEG∶DEX∶BSA∶L-Glu=50∶5∶4∶0)和#3(PEG∶DEX∶BSA∶L-Glu=50∶10∶9∶0)在 4 和25 ℃的温度下能保持 rTTV-OVA 的免疫反应性,并且 rTTV-OVA的免疫原性在冻干过程中得到保留。配方#4(PEG∶DEX∶BSA∶L-Glu= 50∶0∶0∶9)和#5(PEG∶DEX∶BSA∶L-Glu= 50∶1∶0∶8)在相同的条件下保持了Ad5-ENV的感染性,而Ad5-ENV的免疫原性在冻干配方#4 中得到了最大程度的保留。Matejtschuk等[16]通过比较缓冲液中是否添加氯化钠(通常被认为是冻干不利因素)对白细胞介素-6参考物质冻干的影响,发现配方对冻干生物制品至关重要。磷酸盐缓冲液是首选,可获得良好的生物活性。默克公司研发的口服轮状病毒疫苗 RotaTeq®具有良好的热稳定性,Madan 等[17]使用 RotaTeq®疫苗,进一步开发出一种安全有效耐热的冻干配方 HSRV04D5,这种配方在 5 ℃下可稳定储存超过 36 个月,在 37 ℃下稳定储存 20个月,在45 ℃下稳定储存7个月,能在高温环境中进行储存和运输,同时复溶后能够保持良好的疫苗效力。他们发现这种特性可能源于其 Tg 温度为 61 ℃,这一温度远高于疫苗制剂的储存温度。由此推测,HSRV04D5配方的稳定性与其 Tg属性直接关联。冻干产品的储存温度应尽量低于冻干制剂的 Tg,且配方的 Tg 值越高,越有利于提高疫苗的热稳定性。
1.3新型FD技术
冻干技术在疫苗等生物制品领域得到了广泛应用。作为制造固体生物制品的主要手段,冻干具有许多优势。然而,冻干也存在着周期长、能耗高和资金投入大等问题。为了克服这些难题,研究人员进行了大量的探索,开发出许多创新的冻干技术。虽然有些技术尚未在无菌疫苗方面得到广泛应用,但其中一些技术,如旋转冻干、喷雾冷冻干燥、薄膜冷冻干燥和微波辅助冷冻干燥,进一步改善了向连续生产方式的转变。这些创新的冻干技术有望提高生产效率、降低成本,并为疫苗的生产带来更多的机遇。图1展示了几种冷冻干燥技术类型。
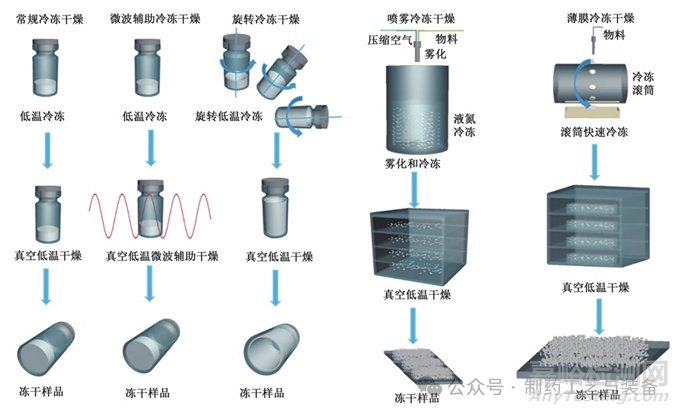
图1 各冷冻干燥示意图
1.3.1 旋转冷冻干燥
旋转冷冻干燥(rotaryfreeze-drying,RFD)技术是一种将样品放置在旋转容器中,使待冻干的样品在离心力作用下贴到容器侧壁进行冷冻干燥的方法。这种方法的优点是冻干固体的比表面积大,干燥速度快,能更好地保持样品的理化结构和生物活性。
Meyer等[18]对5种不同配方进行了测试,在所有的配方中,旋转冷冻瓶的升华速率显著提高。Leys等[19]采用在线过程分析技术对连续冷冻干燥流程进行了优化,通过控制冷却速率和冻结速率来控制冻结阶段,控制瓶温度(从而控制产品温度)到设定值并监测残余水分来控制干燥阶段。在冻结阶段,瓶温度随冷却阶段设定温度下降,并且可以通过调节冻结速率来控制结晶相。在初级和次级干燥阶段,瓶温度保持在设定温度上,每次运行后样品都能保持良好的结构。Meulewaeter等[14]探索了一种基于旋转冷冻的新型连续冷冻干燥技术,与经典的批量冷冻干燥技术相比,该技术具有干燥时间短、流程简便和产品质量更好的优点。在此项研究中,采用了较高的脂质含量,其中mRNA和辅料(Tris或磷酸盐以及12.5 g·L−1蔗糖)质量比为 20∶1,经过最佳冻干处理的 mRNA 疫苗,在4、22和37 ℃下,其活性在12周内未发生变化。同时,也有研究人员将旋转冷冻工艺和传统冻干工艺相结合,发明了一种新型的连续冷冻干燥工艺,用于制备单剂量产品[20]。这种连续冷冻干燥技术的一个主要特点是瓶装液体产品沿着纵轴旋转,因此也被称为旋转冷冻干燥。由于冻结产品遍布在瓶子内壁上,可以产生较大的表面积,从而使得分散层的冷冻/加热快速且均匀,总处理时间根据瓶子尺寸和产品配方的不同,可以比传统的冷冻干燥时间缩短10~40倍。
1.3.2 喷雾冷冻干燥技术
为了进一步增加冻干物质的比表面积,提高冻干效率,研究人员将喷雾冷冻和动态冷冻干燥技术结合,创造出了喷雾冷冻干燥技术(spray freeze drying,SFD)[21]。该技术采用频率驱动的喷孔喷嘴进行喷雾过程,液体进料以共振频率分解为圆形液滴,通过自身重力引导进入冷冻室。在冷冻室中,液滴与−80~−150 ℃的氮气进行热量交换,形成大小为 300~1000 μm的均匀冻结球体。冻结后的微球根据真空闸门的开闭情况,批次进入旋转冷冻干燥机。旋转冷冻干燥机通常采用多个转盘或轴,每次处理一批喷雾冷冻干燥的物料后,切换至下一个转盘或轴进行处理。通过这种方式,实现了大批量样品的连续冷冻干燥,显著提高了可持续的冻干效率。
白藜芦醇(resveratrol)是一种多酚类化合物,具有抗氧化、抗炎、抗癌、抗衰老和心血管保护等多种生物活性。然而,在鼻内给药时,白藜芦醇的溶解度低,且易被鼻腔清除,导致其生物利用度有限。为了克服这一问题,Di等[22]以羟丙基-β-环糊精作为络合剂和辅料,壳聚糖作为粘附增效剂,采用喷雾冷冻干燥技术制备了均匀的微粒。实验结果表明,所获得的粉末与纯白藜芦醇相比,溶解度显著提高了 1 800倍,并具有优异的抗氧化活性。Shokouh 等[23]利用 SFD 技术,通过添加糖(甘露醇或海藻糖)和氨基酸(亮氨酸、苯丙氨酸或丝氨酸),成功制备了雷扎替坦苯甲酸盐微粒。这些配方能有效喷雾化,并提供了高达 61.1% 的可接受细颗粒分数(fine particle fraction,FPF)。特别是由海藻糖和苯丙氨酸组成的喷雾冻干粉末表现出最佳的吸入性能(FPF = 61.1%),表明这些球形多孔微粒具有良好的分散性能,减少了粘附和聚集。这些结果成功证明,雷扎替坦可以制备成可呼吸微粒,成为一种有希望用于快速和有效控制偏头痛发作的给药系统。Qiu 等[24]开发了 mRNA治疗或预防一系列肺部疾病的技术,其通过喷雾冷冻干燥技术,将 PEG(12)KL4 和 mRNA 复合物干燥后,制备成干粉剂,这种干粉剂有较高的吸入性能,其活性也得到了很大程度地保留。Mutukuri等[25]考察了SFD牛血清白蛋白固体的物理稳定性,与传统冻干技术相比,SFD技术在保持或提高牛血清白蛋白物理稳定性的同时,可显著缩短其冻干周期。Pan 等[26]通过 SFD 将 IL-4受体的单克隆抗体制剂制备成干粉后,通过吸入途径用于重度哮喘的治疗。SFD 技术在制剂方面的应用,展现出令人满意的气溶胶性能,实现对抗体的脱水,同时抗体的中和活性未受影响,即使在常温环境下存放一年后,抗体仍保持稳定的理化性质和生物学活性。铜绿假单胞菌的多药耐药性是囊性纤维化(cystic fibrosis,CF)患者终末期和持久性肺部感染的主要原因。Yu等[27]组成伊伐卡托∶粘菌素∶DSPG-PEG-OMe质量比为1∶1∶1的配方,使用超声喷雾冷冻干燥方法开发了干粉剂,该配方对于难溶于水的伊伐卡托的溶解改善效果非常显著,将2种药物合并在一个微粒中,其同步溶解和良好的气雾剂性能,最大程度地提升这2种药物的协同作用和生物活性。
1.3.3 微波辅助冷冻干燥
微波辅助冷冻干燥(microwave-assisted freeze-drying,MFD)是一种在冷冻干燥过程中使用微波辐射加热的方法,用微波真空冷冻干燥技术来提高样品的冻干干燥效率。与冷冻干燥相比,干燥速度更快,能量消耗更低,可以更好地保持样品的结构和活性。Wang等[11]通 过 MFD 方 法 来 生 产 蛋 黄 免 疫 球 蛋 白(IgY),研究了 FD 和 MFD 对不同含量海藻糖的IgY 的免疫活性和结构的影响。结果显示,冷冻干燥导致 IgY 中部分二级结构的损失,从而导致活性损失。随着海藻糖含量从0增加到5%,MFD样品的活性保留率从 20.31% 增加到 75.57%,与FD样品(从23.57%增加到67.78%)相当。与传统FD 相比,MFD 的干燥周期较短,更具优势。Doreth等[28]通过MFD技术制备了吲哚美辛-聚乙烯比咯烷酮 k12 非晶固体分散剂。吲哚美辛-聚乙烯比咯烷酮 k12 非晶固体分散剂不会因 MFD 的影响而发生降解,并且形成非晶片剂的溶解速度比之前高6倍。Gitter等[29]研究了2种单克隆抗体的4种配方,发现 MFD 能够显著缩短干燥时间,未发现相关性质及稳定性降低的情况,并且批次保持了良好的均一性,体现出了 MFD 在抗体中的应用潜力。Hardter 等[30]使用 MFD 研究了 6 种单克隆抗体(mAb)制剂在干燥后的质量和储存6 个月后的稳定性,发现 MFD 的干燥过程较传统的 FD 干燥大大缩短,并且可控性良好,没有出现任何等离子放电的迹象。此外,冻干品的表征显示出良好的形状,且在 MFD 后的 mAb 中具有良好的稳定性,MFD 技术已成功制备出 mAb 制剂产品。
1.3.4 薄膜冷冻干燥
薄膜冷冻干燥(thin-filmfreeze-drying,TFFD)是一种将液体或溶解的物质直接凝固成薄膜,并在低温下进行冷冻干燥的过程,这种方法可以避免传统冷冻干燥过程中的物质结块问题,提高干燥速度和效率。Yu等[31]使用含有脂质体单磷脂 A 和 QS-21 佐剂(AdjLMQ)以及卵清蛋白(ovalbumin,OVA)作为模型抗原的疫苗,通过 TFFD 方法将含有蔗糖和脂质的液体疫苗成功转化为干粉,其中蔗糖与脂质的比例为15∶1(质量比),并考虑了羧甲基纤维素钠盐(carboxymethylcellulose,CMC)等粘附剂的存在与否。最终,选择了含有1.9%(质量分数)CMC的TFFD AdjLMQ/OVA 疫苗干粉进行进一步评估,运用 Taguchi L4正交表来确定鼻腔喷雾设备在成人和儿童鼻腔模型中将 TFF AdjLMQ/OVA/CMC1.9% 干粉送达至中下鼻腔和鼻咽区域的最佳参数。研究结果表明,通过 TFFD 技术将鼻疫苗从液体转化为干粉,并使用鼻腔喷雾包装形式将干粉送达至鼻腔中的目标区域进行鼻内接种。Hufnagel等[32]配制了 PD-1 IgG 与乳糖/亮氨酸(60∶40,质量比)或海藻糖/亮氨酸(75∶25,质量比)的配方,在磷酸盐缓冲液中,制剂经TFFD处理后,产生的干粉具有理想的喷雾性能,TFFD干粉具有多孔的结构和纳米聚合物的特性,并且 Tg介于 39~50 ℃。当在室温下储存时,TFFD制备的干粉中抗体具有比液体配方更高的稳定性。Aboul等[33]利用 TFFD 技术,采用海藻糖作为稳定剂,成功地将含 AddaVax 佐剂(一种水包油纳米乳化疫苗佐剂)的 Fluad(R)四价流感液态疫苗转化为干粉,抗原的完整性和血凝活性并未发生显著变化。此外,在小鼠模型中,重组流感疫苗的免疫原性保持不变,且干粉对重复冻融过程并不敏感,具有良好的稳定性,TFFD技术有望用于制备多价流感通用疫苗干粉。
1.4冻干技术的优化
冻干技术是一项复杂的工艺技术,优化冻干技术,可以从设备和材料选用、冻干过程参数控制、产品配方优化、储存条件优化这几方面提高冻干技术的效果。不同的物料可能需要使用不同的冻干设备,例如对于热敏性物料,需要选用能够精确控制温度和真空度的设备。同时,选用高品质的材料可以有效提高产品的包装质量和存储条件[34]。冻干过程中的温度、真空度、冻干时间等参数都需要进行精细化控制,这需要依赖于先进的设备和智能化的控制系统。通过实时监测和调整这些参数,可以确保物料的冻干效果达到最佳[35]。通过调整物料的配方,可以有效提高冻干产品的活性和质量。Guo等[36]在制备高载量胰岛素纳米颗粒时,通过优化配方发现,不添加甘露醇的喷雾干燥或冻干脱水纳米颗粒比添加甘露醇的纳米颗粒载药量更高,同时具有更小的平均颗粒,更有利于胰岛素释放,细胞摄取效果更好。合理的存储条件可以延长产品的保质期,保证产品的品质和使用效果,这需要对温度、湿度、光照等环境因素进行严格控制。通过这些优化措施,可以进一步提高冻干技术的生产效率和产品质量,降低生产成本,得到质量更好、储存期限更长的冻干产品。
2.不同类型疫苗的冷冻干燥研究
液体疫苗制剂受多种因素(如温度变化、氧化和水解等)影响,易造成活性降低。而冻干技术,可以将液体疫苗转化为干燥粉末形式,能够避免或抑制许多降解途径的发生。在干燥制剂中,特别是无水或含水量较低的情况下,疫苗制剂的稳定性可以得到显著提高。相比于液体疫苗,干燥疫苗制剂具有许多潜在的优势,包括更长的货架寿命和较宽松的冷链存储要求,这有助于减少疫苗储存和运输的成本,拓宽疫苗的接种区域。
2.1灭活疫苗
灭活疫苗是一类使用灭活的病原体制备的疫苗,具有较高的安全性,冷冻干燥技术可以提高病毒灭活疫苗的稳定性,减少在运输和储存过程中的损失。Abd等[37]对包含牛病毒性腹泻病毒(bovine viral diarrhea virus,BVDV)1和2型、牛单纯疱疹病毒 1.1 型(BoHV-1.1)、牛副流感病毒(bovineparainfluenza virus,BPSV)3型和牛呼吸道合胞病毒(bovine respiratory syncytial virus,BRSV)5 种灭活病毒的 Pneumo-5 合并病毒灭活疫苗进行了冻干处理,并对小鼠和小牛进行了无菌性、安全性和效力评估。研究结果表明,制备的Pneumo-5疫苗冻干制剂能够保护小牛对抗 BVDV 1 型、BVDV 2型、BoHV-1.1、BPI-3V 和 BRSV 病毒,且具有安全性和有效性。然而,由于灭活疫苗在灭活过程中已经对疫苗抗原造成了一次活性降低作用,灭活疫苗中通常加有佐剂以提高抗原对机体的免疫效果[38]。在冻干的过程中,由于工艺复杂,可能使疫苗抗原的活性再次降低,佐剂结构有可能发生变化,从而降低疫苗的免疫效果,因此目前大部分灭活疫苗,是以液体形式保存,而使用冻干技术较少。
2.2减毒活疫苗
减毒活疫苗是一类使用减毒的病原体制备的疫苗,能够诱导强烈的免疫反应,产生多种抗体,并且具有长久的免疫效果。冷冻干燥技术可以提高减毒活疫苗的稳定性,减少在运输和储存过程中的损失。
研究人员在处理某些新分离的呼吸道病毒时发现在低于−60 ℃的条件下,一些流感病毒和鼻病毒制剂与 2% 的牛血浆蛋白或 2% 的小牛血清共存一年甚至更长时间后会失去传染性。此外,这些冷冻的流感病毒在室温下会很快失去传染性,因此必须以冷冻状态或作为感染的组织培养物进行传输,这给实际的研究过程带来了极高的条件限制。Tyrrell 等[39]通过优化冷冻干燥条件,提高了病毒的稳定性,进一步证明了冷冻干燥技术在冷冻保存具有潜在传染性病毒中的重要作用。另外,Abayneh等[40]研究发现炭疽冻干疫苗在20 ℃储存条件下,可以在180 d 内保持较高效力,而液体悬浮疫苗的储存时间仅为 90 d。Shokri等[41]探索了 2 种新型稳定剂(海藻糖稳定剂和包含蔗糖、人血清白蛋白、山梨醇的稳定剂)对冷冻干燥活病毒风疹疫苗(高桥株)的热稳定性,并与商用的明胶稳定剂配方作对比。不同稳定剂制备并进行冻干处理后的样品,通过加速稳定性测试评估了所产生的疫苗的效力。结果表明,与商业风疹疫苗中含有明胶稳定剂和蔗糖稳定剂的配方相比,海藻糖的稳定剂冻干疫苗表现出充分的稳定性。Jamil 等[42]制备并评估了冷冻干燥的减毒腮腺炎活疫苗,发现在加速稳定性实验中即使在最严苛的37 ℃条件下存储一周,Vero细胞50%的细胞培养感染量(50% cell culture infectious dose,CCID50)下降幅度不到 10 倍,符合当时世界卫生组织对弱毒性腮腺炎活疫苗效力的要求。
在日本,冻干减毒活疱疹-带状疱疹病毒疫苗可供≥50 岁的成年人使用,以预防带状疱疹。Matsumoto 等[43]对 1200名健康成年人和 300名患有基础疾病的患者进行了疫苗安全性确认,并分析了 2016—2017 年之间 1098 名接种者和 518 名未接种者在 2016—2022 年间的发病率。结果显示,无论年龄、性别或有何合并症,冻干减毒活疱疹-带状疱疹病毒疫苗都能降低被接种者患上带状疱疹的风险。Clenet等[44]对黄热病毒疫苗进行了冷冻干燥研究,发现冷冻干燥后的样品具有较高的 Tg,确保了良好的断裂力和高抗溃散性。在为期3年的稳定性观察期间,发现在冷藏条件(2~8 ℃)下,这种干燥微粒的黄热病毒感染滴度与冷冻干燥产品相似。在 25℃和 37℃的加速稳定性研究中,微粒中的 vYF 的降解动力学与常规冻干产品无显著差异,这些结果揭示了将减毒活病毒疫苗制成微粒形式的巨大潜力。
Madan等[17]利用默克公司的冻干轮状病毒减毒活疫苗 RotaTeq®,开发出了一种安全、有效、耐热的冻干配方(HSRV04D5),在 5、37和 45 ℃条件下,根据实时稳定性数据的线性回归分析得出,HSRV04D5 在 5℃下,稳定性超过36个月,在37 ℃下可达到 20 个月,在 45 ℃下可达到 7 个月,稳定性研究结果显示出冻干轮状病毒减毒活疫苗有极佳的热稳定性。此外,他们还发现这种稳定性的特性可能源于其Tg温度为61 ℃,这一温度远高于疫苗制剂的储存温度。由此推测,HSRV04D5配方的高度稳定性与其Tg值直接关联。冻干产品的储存温度应尽量低于冻干制剂的Tg值,且配方的Tg值越高,越有利于提高制剂的热稳定性。
2.3亚单位疫苗
亚单位疫苗是由病原体的一个或多个组分(如蛋白质、多肽或多糖)构成的疫苗。这些组分可以通过化学方法从病原体中提取,或通过基因工程方法在宿主细胞中表达。由于它们不含具有复制功能的病原体,通常亚单位疫苗比减毒活疫苗和灭活疫苗更安全。同样,冷冻干燥技术可以提高亚单位疫苗的稳定性,延长其有效期。Kelly等[45]通过冷冻干燥技术制备了舌下免疫途径的结核分枝杆菌的超分子肽疫苗,通过舌下免疫可产生针对结核分枝杆菌 ESAT6 表位的抗体反应。此外,该疫苗在45℃条件下储存1周后进行免疫,舌下抗体反应并未减弱,证明其具有良好的热稳定性。
水痘带状疱疹病毒(varicella zoster virus,VZV)是一种神经和淋巴病毒,可以引起水痘和带状疱疹(herpes zoster,HZ)。初次感染时,VZV 会导致儿童患上水痘,而潜伏在感觉神经节中的病毒会导致老年人出现疼痛的带状疱疹,并可能引发严重并发症,如疱疹性神经痛。Wui 等[46]开发了一种名为 CIA09A 的新型脂质体佐剂系统,该系统由阳离子脂质体、Toll 样受体 4(toll-like receptor 4,TLR4)激动剂去酰化脂质寡糖和坎拉查皂苷分离物(quillaja saponin fraction-21,QS-21)组成。将该脂质体佐剂与重组的VZV糖蛋白E(gE)一同冻干,并没有破坏gE的免疫活性。该疫苗在诱导体液免疫和细胞免疫反应方面表现出极高的效果。此外,在接种疫苗的小鼠中,出现了干扰素-γ、肿瘤坏死因子-α 和白细胞介素-2等细胞因子表达水平的显著提高。这些数据表明,通过将蛋白抗原与 CIA09A 一起冻干制成的疫苗,能够产生强大的细胞免疫,以提高疫苗的有效性。
2.4重组病毒载体疫苗
重组病毒载体疫苗是一种利用病毒载体将合成抗原的遗传物质递送至人体的疫苗。这种疫苗利用经过改造的无病原性病毒作为载体,将目标病原体的基因序列插入到病毒载体中,生成重组病毒。当接种重组病毒载体疫苗时,病毒载体进入人体细胞,并开始表达目标病原体的抗原,以引发免疫反应。人体能产生针对目标病原体的特异性免疫应答,提供对该病原体的保护。
扎伊尔埃博拉病毒(Zaireebolavirus,EBOV)是已知最致命的传染病毒之一,人类感染病例的病死率高达 89%。自 2018 年 8 月起,默克公司的ERVEBO®重组水疱性口炎病毒-扎伊尔埃博拉病毒疫苗(recombinant vesicular stomatitis virus-ZaireEbola virus,rVSV-ZEBOV)一直被用于刚果民主共和国北基伍地区的埃博拉病毒疫情控制。该疫苗要求以冷冻固态形式存储在−60 ℃至−80 ℃温度下。解冻后,液体的 rVSV-ZEBOV 疫苗在 25 ℃下只能稳定一天,当天未被使用的疫苗即被丢弃。因此,将疫苗运送到偏远地区,对于炎热的低收入和中等收入国家来说是一项具有挑战性的任务[47]。Preston 等[48]使用 9.5%(质量体积分数)的海藻糖(280 mol·L-1)作为保护剂,通过乙酸铵调节冻干过程中的离子强度,利用冷冻干燥技术处理埃博拉病毒糖蛋白(Ebola virus glycoprotein,EBOV-GP)亚单位疫苗,结果显示这种冻干疫苗在高达 40 ℃下,可保存 12 周。通过对疫苗的物理特性研究表明,在高温条件下,液体配方中EBOV-GP 的组装状态发生了变化,而在冷冻干燥的配方中,EBOV-GP的组装状态没有受到影响。
2.5核酸疫苗
核酸疫苗是通过将病原体的核酸片段(如mRNA 或 DNA)注入人体,诱导细胞内表达病原体部分蛋白,从而引发体液免疫和细胞免疫的疫苗。经过多年的研究和开发,mRNA 递送系统取得了突破性进展,mRNA 疫苗已成为预防新型冠状病毒感染的领先技术。相比于灭活疫苗和重组蛋白疫苗,mRNA 疫苗能够迅速更新,因此针对不断出现的变异株,也具备强大的免疫效果。
mRNA 虽然具有独特的优势,但其物理化学的不稳定性仍然是限制疫苗使用的主要因素。目前,获得批准的 2种 mRNA 疫苗,BNT162b2(储存温度为−80 ℃至−60 ℃)和 mRNA-1273(储存温度为−20 ℃),均需要在低温下冷冻保存和运输。这些严格的要求源于多种脂质成分之间复杂的相互作用,以及 mRNA 对氧气、湿度、酶、pH 和其他条件非常敏感的不稳定性。Packer等[49]报道了离子化脂质的氧化和随后水解副产物加速mRNA降解的新机制。由于水、氧和离子化脂质是mRNA-脂质纳米颗粒(lipid nanoparticle,LNP)溶液中常见的组分,因此在液态下实现高稳定性的 mRNALNP在理论上是很困难的。Ai等[50]通过冻干技术研发了具有长期热稳定性的 SARS-CoV-2 mRNA脂质纳米颗粒疫苗,结果发现冻干疫苗在25 ℃条件下保持了6个月的物理化学性质和生物活性的稳定性。这种冻干的 SARS-CoV-2 mRNA 疫苗能够在小鼠、兔子和恒河猴等动物中诱导强大的体液和细胞免疫。此外,人类试验也表明,使用冻干的 Omicron mRNA 疫苗作为加强剂能够产生强大的免疫效应,并且没有出现严重的不良事件。脂质修饰聚合物聚β-氨基酯通过酶催化酯化反应合成,并与聚乳酸-共-缩乙二醇自组装成一种用于核酸递送的“颗粒内颗粒”(particle-in-particle,PNP)纳米结构。Li 等[51]在 24 种 PNP 候选者中筛选出最有效的 PNP/C12-PBAE 纳米颗粒,这些颗粒在体外和体内均表现出高效的核酸递送性能,具有增强的转染效果、持久的基因释放能力和出色的稳定性。在经过冻干后,这些 PNP 颗粒在−20 ℃的储存条件下至少能保持12个月,且无需担心转染效果损失的问题。将携带刺突蛋白编码质粒DNA 或 mRNA 的脂质修饰聚合物 PNP COVID-19疫苗封装后,即使在−20 ℃冻干储存12个月后,仍能成功激发免疫小鼠产生针对刺突蛋白的抗体和倾向于Th1型的T细胞免疫应答。因此,冻干技术不仅克服了核酸疫苗的不稳定性,同时保持了其生物学活性。
2.6病毒样颗粒疫苗
病毒样颗粒疫苗是由病毒的结构蛋白质组装而成的颗粒疫苗,由于其结构与天然病毒相似,能引起很强的细胞免疫和体液免疫,但其不含病毒的遗传物质,安全性更强[52]。冷冻干燥技术可以提高病毒样颗粒疫苗的稳定性,降低运输和储存过程中的损失。例如,人乳头瘤病毒(human papillomavirus,HPV)疫苗和乙型肝炎疫苗都采用了冷冻干燥技术。HPV 的衣壳次要蛋白质是 L2 蛋白,它存在于 HPV病毒样颗粒(virus-like particle,VLP)中,位于每个五聚体的顶点。通过对 L2 蛋白 N-端衍生的多肽进行免疫化,可以诱导人体产生广谱的抗体反应,从而产生能够交叉保护多种HPV类型的抗体。Yadav等[53]开发了混合的MS2-L2病毒样颗粒(包括MS2-31L2/16 L2 VLP和MS2-consL2(69-86)VLP)疫苗,并通过喷雾冷冻干燥技术制备得到。这种疫苗对于引起宫颈癌的大多数HPV 类型(约 95.8%)具有预防效果,并且对大多数引起生殖器疣和复发性呼吸道乳头瘤病毒的HPV 类型(约 90%)也具有预防作用,且该冻干疫苗在 37 ℃条件下存放 10个月后仍能保持良好的免疫效果。另外,研究者还开发了一种二价诺如病毒疫苗,该疫苗中包含GI.1和GII.4亚型的诺如VLP,并吸附在铝佐剂上。Xu 等[54]通过 TFFD 技术测试了将这种诺如病毒 VLP 疫苗从液体悬浮转化为干燥粉末的可行性。他们使用经过优化的海藻糖或蔗糖作为保护剂,将疫苗进行冻干处理后,抗原的相对效力在可接受范围内。在加速稳定性研究中,使用TFFD制备的冻干疫苗在40 ℃、相对湿度为 75% 的条件下储存 8 周后,抗原的效力仍然保持在可接受范围内。
2.7结合类疫苗
结合类疫苗是将病原体表面的多糖或蛋白质与载体蛋白质结合制成,以增强其免疫原性和免疫系统的反应性,从而提高对特定病原体的免疫效果。肺炎球菌结合疫苗(pneumococcal conjugate vaccine,PCV)在全球市场上尚未有冻干剂型,导致全球 PCV疫苗的分配范围差距巨大。此外,目前获得许可的 PCV疫苗仅针对一些与肺炎链球菌相关的血清型,而不是全部。Mensch等[55]开发了一种冻干佐剂的多价疫苗制剂,以符合肺炎球菌疾病的流行病学评估,并提供更广泛的覆盖范围。他们从15个配方中筛选出最佳配方,以稳定冻干疫苗的效力。在配方中添加0.5%(质量分数)的丙二醇和 6%(质量分数)的甘露醇,并与 0.5%(质量分数)的羧甲基纤维素钠和 4%(质量分数)的蔗糖一起使用,能够有效控制冻干过程中疫苗效力的下降。相对于非冻干剂型,冻干的肺炎球菌结合疫苗在稳定性和免疫效果方面均表现出了良好的效果。
冷冻干燥技术在疫苗制造中的应用,可以大大提高疫苗的稳定性和便捷性,表1 汇总了一些冻干疫苗及稳定性能。
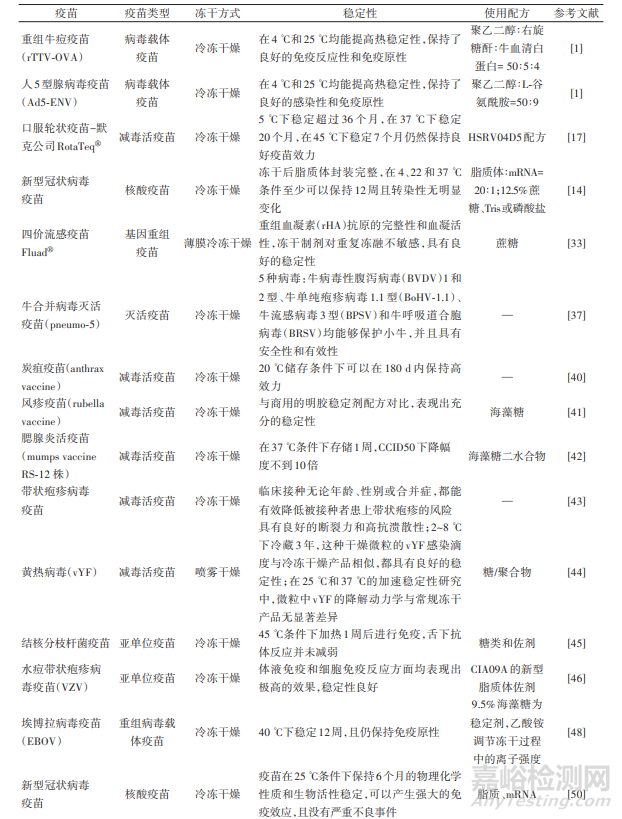

表1 冻干疫苗示例及稳定性
3.展 望
传统液体疫苗需要在低温条件下储存和运输,并具有短暂的保持时间,而冷冻干燥技术可以将疫苗冻干成干燥粉末,极大地延长了疫苗的稳定性和保质期。冻干疫苗可以在常温下储存和运输,并且更容易配送到偏远地区。此外,冷冻干燥的疫苗也更容易用于应急情况,方便大规模的疫苗接种。冷冻干燥技术具有适应突发疫情和全球疫苗需求的潜力。例如,在面对传染病突发情况下,冻干疫苗可以稳定的供应到各个地区,满足全球范围内对疫苗的需求,特别是在资源有限的地区或偏远地区,通过冻干疫苗的配送和储存,能够更好地满足人类疫苗需求,对于控制疫情起到至关重要的作用。
参考文献
[1] CHEN Y, LIAO Q, CHEN T, et al.. Freeze-drying formulationsincreased the adenovirus and poxvirus vaccine storage timesand antigen stabilities[J]. Virol. Sin., 2021, 36(3): 365-372.
[2] LYU J L, BAO L R, SHEN X, et al.. The preparation of N-IgYtargeting SARS-CoV-2 and its immunomodulation to IFN-gam⁃ma production in vitro[J/OL]. Int. Immunopharmacol., 2021,96: 107797[2021-06-25]. https://doi.org/10.1016/j.intimp. 2021.107797.
[3] HARRIS R J. Preservation of biological materials by freezedrying[J]. Nature, 1951, 168(4281): 851-853.
[4] WANG Z, LI L, REN G, et al.. A comprehensive review on sta⁃bility of therapeutic proteins treated by freeze-drying: inducedstresses and stabilization mechanisms involved in processing[J].Dry. Technol., 2022, 40(16): 3373-3388.
[5] LIU Y, ZHANG Z, HU L. High efficient freeze-drying technol⁃ogy in food industry[J]. Crit. Rev. Food Sci. Nutr., 2022, 62(12):3370-3388.
[6] FRANKS F. Freeze-drying of bioproducts: putting principlesinto practice[J]. Eur. J. Pharm. Biopharm., 1998, 45(3): 221-229.
[7] WANG G Q, PU J, YU X Q, et al.. Influence of freezing tem⁃perature before freeze-drying on the viability of various Lacto⁃bacillus plantarum strains[J]. J. Dairy Sci., 2020, 103(4): 3066-3075.
[8] SITAR A, ŠKRLEC K, VOGLAR J, et al.. Effects of controllednucleation on freeze-drying lactose and mannitol aqueous solu⁃tions[J]. Dry. Technol., 2018, 36(10): 1263-1272.
[9] NUYTTEN G, REVATTA S R, VAN BOCKSTAL P, et al.. De⁃velopment and application of a mechanistic cooling and freez⁃ing model of the spin freezing step within the sramework ofcontinuous freeze-drying[J/OL]. Rmaceutics, 2021, 13: 2076[2021-12-29]. https://doi.org/10.3390/pharmaceutics13122076.
[10] KAWASAKI H, SHIMANOUCHI T, KIMURA Y. Recent de⁃velopment of optimization of lyophilization process[J/OL]. J.Chem., 2019, 2019: 9502856[2019-05-05]. https://doi.org/10.1155/2019/9502856.
[11] WANG Z, DUAN X, LI L, et al.. Effects of freeze-drying andmicrowave vacuum freeze-drying on the activity of IgY: fromthe perspective of protein structure[J]. Dry. Technol., 2023,41(2): 222-232.
[12] ASSEGEHEGN G, FUENTE B D L, FRANCO J, et al.. Under⁃standing and optimization of the secondary drying step of afreeze-drying process: a case study[J]. Dry. Technol., 2021, 39(8): 1003-1017.
[13] YOON K, NARSIMHAN V. Understanding heat transfer dur⁃ing the secondary drying stage of freeze drying: current practiceand knowledge gaps[J]. J. Pharm. Sci., 2022, 111(2): 368-381.
[14] MEULEWAETER S, NUYTTEN G, CHENG M H Y, et al..Continuous freeze-drying of messenger RNA lipid nanoparti⁃cles enables storage at higher temperatures[J/OL]. J. Control.Release, 2023, 357: 149[2023-03-21]. https://doi.org/10.1016/j.jconrel.2023.03.039.
[15] HUANG Y, ZHENG S, GUO Z, et al.. Ionizable liposomal siR⁃NA therapeutics enables potent and persistent treatment ofHepatitis B[J/OL]. Signal Transduct. Target. Ther., 2022, 7: 38[2022-02-12]. https:// doi.org/10.1038/s41392-021-00859-y.
[16] MATEJTSCHUK P, BIRD C, EZEAJUGHI E, et al.. Impact offormulation choices on the freeze-drying of an interleukin-6reference material[J/OL]. Front. Mol. Biosci., 2022, 9: 868460[2023-12-20]. https://doi.org/10.3389/fmolb.2022.868460.
[17] MADAN M, SIKRIWAL D, SHARMA G, et al.. Rational designof heat stable lyophilized rotavirus vaccine formulations[J].Hum. Vaccines Immunother., 2018, 14(9): 2132-2141.
[18] MEYER L D, VAN BOCKSTAL P J, CORVER J, et al.. Evalua⁃tion of spin freezing versus conventional freezing as part of a con⁃tinuous pharmaceutical freeze-drying concept for unit doses[J].Int. J. Pharm., 2015, 496(1): 75-85.
[19] LEYS L, NUYTTEN G, VAN BOCKSTAL P J, et al.. Evalua⁃tion of a PAT-based in-line control system for a continuous spinfreeze-drying process[J/OL]. Int. J. Pharm., 2023, 641: 123062[2023-05-21]. https://doi.org/10.1016/j.ijpharm.2023.123062.
[20] Method and system for freeze-drying injectable compositions,in particular pharmaceutival compositions: US201815922757[P]2019-03-01.
[21] LUY B, STAMATO H. Spray freeze drying[M]//OHTAKE S,IZUTSU K, LECHUGA-BALLESTEROS D. Drying technolo⁃gies for biotechnology and pharmaceutical applications. Ameri⁃ca: John Wiley & Sons Ltd, 2020, 217-237.
[22] DI A, ZHANG S, LIU X, et al.. Microfluidic spray dried andspray freeze dried uniform microparticles potentially for intra⁃nasal drug delivery and controlled release[J]. Powder Technol.,2021, 379: 144-153.
[23] SHOKOUH M K, FAGHIHI H, DARABI M, et al.. Formula⁃tion and evaluation of inhalable microparticles of Rizatriptanbenzoate processed by spray freeze-drying[J/OL]. J. Drug Deliv.Sci. Tec., 2021, 62: 7[2019-05-05]. https://doi.org/10.1016/j.jddst.2021.102356.
[24] QIU Y, MAN R C H, LIAO Q, et al.. Effective mRNA pulmo⁃nary delivery by dry powder formulation of PEGylated synthet⁃ic KL4 peptide[J]. J. Control. Release Off. J. Control. ReleaseSoc., 2019, 314: 102-115.
[25] MUTUKURI T T, DARWISH A, STRONGRICH A D, et al..Radio frequency-assisted ultrasonic spray freeze drying for phar⁃maceutical protein solids[J]. J. Pharm. Sci., 2023, 112(1): 40-50.
[26] PAN H W, SEOW H C, LO J C K, et al.. Spray-dried andspray-freeze-dried powder formulations of an anti-interleukin4Rα antibody for pulmonary delivery[J]. Pharm. Res., 2022,39(9): 2291-2304.
[27] YU S H, PU X H, AHMED M U, et al.. Spray-freeze-dried inhal⁃able composite microparticles containing nanoparticles of combi⁃national drugs for potential treatment of lung infections caused byPseudomonas aeruginosa[J/OL]. Int. J. Pharmaceut., 2021, 610: 9[2021-10-01]. https://doi.org/10.1016/j.ijpharm. 2021.121160.
[28] DORETH M, HUSSEIN M A, PRIEMEL P A, et al.. Amor⁃phization within the tablet: using microwave irradiation to forma glass solution in situ[J]. Int. J. Pharm., 2017, 519(1-2):343-351.
[29] GITTER J H, GEIDOBLER R, PRESSER I, et al.. Microwaveassisted freeze-drying of monoclonal antibodies: product qualityaspects and storage stability[J/OL]. Pharmaceutics, 2019, 11(12):674[2019-12-18]. https://doi.org/10.3390/pharmaceutics11120674.
[30] HARDTER N, GEIDOBLER R, PRESSER I, et al.. Accelerat⁃ed production of biopharmaceuticals via microwave-assistedfreeze-drying (MFD)[J/OL]. Pharmaceutics, 2023, 15: 15[2023-04-27]. https:// doi.org/10.3390/pharmaceutics15051342.
[31] YU Y S, ABOULFOTOUH K, XU H, et al.. Feasibility of intra⁃nasal delivery of thin-film freeze-dried, mucoadhesive vaccinepowders[J/OL]. Int. J. Pharm., 2023, 640: 122990[2023-12-20]. https://doi.org/10.1016/j.ijpharm.2023.122990.
[32] HUFNAGEL S, XU H, SAHAKIJPIJARN S, et al.. Dry pow⁃ders for inhalation containing monoclonal antibodies made bythin-film freeze-drying[J/OL]. Int. J. Pharm., 2022, 618: 121637[2022-03-09]. https://doi.org/10.1016/j.ijpharm.2022.121637.
[33] ABOUL FOTOUH K, UNO N, XU H, et al.. Formulation of drypowders of vaccines containing MF59 or AddaVax by thin-filmfreeze-drying: towards a dry powder universal flu vaccine[J/OL].Int. J. Pharm., 2022, 624: 122021[2022-07-17]. https://doi. org/10.1016/j.ijpharm.2022.122021.
[34] YAN J K, WU L X, QIAO Z R, et al.. Effect of different dryingmethods on the product quality and bioactive polysaccharidesof bitter gourd (Momordica charantia L.) slices[J]. Food Chem.,2019, 271: 588-596.
[35] MEHANNA M M, ABLA K K. Recent advances in freeze-drying:variables, cycle optimization, and innovative techniques[J].Pharm. Dev. Technol., 2022, 27(8): 904-923.
[36] GUO Y, BALDELLI A, SINGH A, et al.. Production of highloading insulin nanoparticles suitable for oral delivery by spraydrying and freeze drying techniques[J/OL]. Sci. Rep., 2022, 12:9949[2022-06-15]. https://doi.org/10.1038/s41598-022-13092-6.
[37] FADEEL M R A, EL-DAKHLY A T, ALLAM A M, et al..Preparation and efficacy of freeze-dried inactivated vaccineagainst bovine viral diarrhea virus genotypes 1 and 2, bovineherpes virus type 1.1, bovine parainfluenza-3 virus, and bo⁃vine respiratory syncytial virus[J]. Clin. Exp. Vaccine Res.,2020, 9(2): 119-125.
[38] 姚舜禹,张丽琳 . 新城疫疫苗研究进展[J]. 生物技术进展,2020,10(5):470-478.YAO S Y, ZHANG L L. Progress on Newcastle disease vac⁃cine[J]. Curr. Biotechnol., 2020, 10(5): 470-478.
[39] TYRRELL D A, RIDGWELL B. Freeze-drying of certain virus⁃es[J]. Nature, 1965, 206: 115-116.
[40] ABAYNEH T, GETACHEW B, GELAYE E, et al.. Viabilityevaluation of freeze dried and suspension anthrax spore vac⁃cine formulations stored at different temperatures[J]. Vaccine,2021, 39(42): 6245-6249.
[41] SHOKRI S, SHAHKARAMI M K, SHAFYI A, et al.. Evalua⁃tion of the thermal stability of live-attenuated Rubella vaccine(Takahashi strain) formulated and lyophilized in different stabi⁃lizers[J]. J. Virol. Meth., 2019, 264: 18-22.
[42] JAMIL R K, TAQAVIAN M, SADIGH Z A, et al.. Evaluationof the thermal stability of a novel strain of live-attenuated mumps vaccine (RS-12 strain) lyophilized in different stabiliz⁃ers[J]. J. Virol. Meth., 2014, 199: 35-38.
[43] MATSUMOTO K, OHFUJI S, INOHARA K, et al.. Effective⁃ness of live attenuated varicella-zoster vaccine in adults olderthan 50 years in Japan: a retrospective cohort study[J/OL].Vaccines, 2023, 11: 9[2023-01-25]. https://doi.org/10.3390/vaccines11020259.
[44] CLÉNET D, HOURQUET V, WOINET B, et al.. A sprayfreeze dried micropellet based formulation proof-of-concept fora yellow fever vaccine candidate[J]. Eur. J. Pharm. Biopharm.2019, 142: 334-343.
[45] KELLY S H, OPOLOT E E, WU Y Y, et al.. Tabletized supramo⁃lecular assemblies for sublingual peptide immunization[J/OL].Adv. Healthc. Mater., 2021, 10: 6[2021-02-01]. https://doi.org/10.1002/adhm.202001614.
[46] WUI S R, KIM K S, RYU J I, et al.. Efficient induction of cellmediated immunity to varicella-zoster virus glycoprotein E colyophilized with a cationic liposome-based adjuvant in mice[J].Vaccine, 2019, 37(15): 2131-2141.
[47] ARNEMO M, VIKSMOEN WATLE S S, SCHOULTZ K M,et al.. Stability of a vesicular stomatitis virus-vectored Ebolavaccine[J]. J. Infect. Dis., 2016, 213(6): 930-933.
[48] PRESTON K B, MONTICELLO C R, WONG T A S, et al..Preservation of quaternary structure in thermostable, lyophi⁃lized filovirus glycoprotein vaccines: a search for stability-indi⁃cating assays[J]. J. Pharm. Sci., 2020, 109(12): 3716-3727.
[49] PACKER M, GYAWALI D, YERABOLU R, et al.. A novelmechanism for the loss of mRNA activity in lipid nanoparticledelivery systems[J/OL]. Nat. Commun., 2021, 12: 6777 [2021-11-24]. https:// doi.org/10.1038/s41467-021-26926-0.
[50] AI L, LI Y, ZHOU L, et al.. Lyophilized mRNA-lipid nanopar⁃ticle vaccines with long-term stability and high antigenicityagainst SARS-CoV-2[J/OL]. Cell Discov., 2023, 9: 9[2023-01-23]. https:// doi.org/10.1038/s41421-022-00517-9.
[51] LI Z Y, ZHANG X Q, HO W, et al.. Lipid-polymer hybrid “par⁃ticle-in-particle” nanostructure gene delivery platform exploredfor lyophilizable DNA and mRNA COVID-19 vaccines[J/OL].Adv. Funct. Mater., 2022, 32: 16 [2022-07-22]. https://doi.org/10.1002/adfm.202204462.
[52] 李岩异,吕娜,贾思凝,等 .体外组装的病毒样颗粒在疫苗和药物递送中的应用[J].生物技术进展,2023,13(2):201-209.LI Y Y, LYU N, JIA S N, et al.. Application of virus like parti⁃cles assembled in vitro in vaccine and drug delivery[J]. Curr.Biotechnol., 2023, 13(2): 201-209.
[53] YADAV R, ZHAI L, KUNDA N K, et al.. Mixed bacteriophageMS2-L2 VLPs elicit long-lasting protective antibodies againstHPV pseudovirus 51[J/OL]. Viruses, 2021, 13(6): 1113[2021-07-03]. https://doi.org/10.3390/v13061113.
[54] XU H, BHOWMIK T, GONG K, et al.. Thin-film freeze-dryingof a bivalent Norovirus vaccine while maintaining the potencyof both antigens[J/OL]. Int. J. Pharm., 2021, 609: 121126[2023-12-20]. https://doi.org/10.1016/j.ijpharm.2021.121126.
[55] MENSCH C, CHINTALA R, NAWROCKI D, et al.. Enablinglyophilized pneumococcal conjugate vaccines through formula⁃tion design and excipient selection suitable for A multivalentadjuvanted vaccine[J]. J. Pharm. Sci., 2021, 110(1): 97-107.
本文作者刘容麟、王宁、李岩异、 张卫婷、罗楚、牛维兵,华北制药金坦生物技术股份有限公司、石家庄市农业技术推广中心,来源于生物技术进展,仅供交流学习。

来源:Internet