嘉峪检测网 2025-03-19 18:42
导读:本文将详细介绍七种主要的骨科生物医用材料。
骨修复材料主要指用于直接支持、增强或替代受损骨骼的材料。这类材料的设计和应用专注于骨骼的治疗和恢复,如骨折愈合、骨缺损填充和骨质增强等,包括自然来源的骨移植材料(如自体骨和同种异体骨)、合成陶瓷(如羟基磷灰石和三钙磷酸盐)、金属(如钛和其合金)、及生物可降解材料(如聚乳酸和聚甘酸)等。
而骨科生物医用材料是一个更广泛的术语,涵盖了所有在骨科手术和治疗中使用的生物兼容材料。除了包括骨修复材料的功能外,这类材料也可能用于支持、替代或修复肌腱、软骨、肌肉等其他组织。从骨折修复到关节重建,从软骨修复到肌腱再生,每一步的治疗都可能涉及到一种或多种特定的生物医用材料。
本文将详细介绍七种主要的骨科生物医用材料,它们包括:
骨替代材料:这类材料用于替代或修复受损的骨骼,其设计旨在模拟自然骨的结构和功能。
骨移植材料:涵盖从自体、同种异体到异种骨移植的各种材料,用于填补骨缺损或增强骨愈合。
软骨替代与移植材料:专为修复或替换受损软骨设计,这些材料帮助恢复关节的功能和减少疼痛。
肌腱组织替代与移植材料:用于修复或替代受伤的肌腱,这些材料需要具备高度的弹性和强度以支持动态负荷。
骨科内固定材料:包括各种钉、钉棒、板和其他装置,用于内部固定骨折或重建手术中的骨骼。
骨科外固定器支架及应用:这些装置通过外部支架固定骨折或纠正畸形,支架设计要能适应患者的具体需求。
骨科生物可吸收内固定材料:这些材料在体内逐渐降解吸收,避免了二次手术取出的需要,同时提供了足够的初始强度以支持骨愈合。
以下摘自《2025全球骨科医疗器械创新白皮书》:
骨替代材料
骨替代材料,也称为骨移植替代材料或骨再生材料,是在骨科和牙科手术中用来替代自然骨的材料。这些材料被设计用于支持、增强或促进受损或缺失骨组织的再生和修复。骨替代材料的主要功能是提供一个支架结构,促进新骨的形成,并最终被新生骨组织所取代或整合。
以下是各类别中的一些典型产品:
接骨螺钉:用于固定骨折碎片或作为拉力螺钉将骨折片抓持在一起,常见的有PDLLA/HA复合可吸收接骨螺钉和金属钛合金接骨螺钉。

▲接骨螺钉
接骨板:紧贴于骨上提供固定,与螺钉配合使用,用于骨折内固定,如直型和异型金属接骨板,以及特殊形状的接骨板如人字形、弧形、L形等。

▲金属异型接骨板
髓内钉:用于骨折内固定,特别是长骨干骨折,如V形髓内钉和梅花形髓内钉,以及交锁髓内钉等。
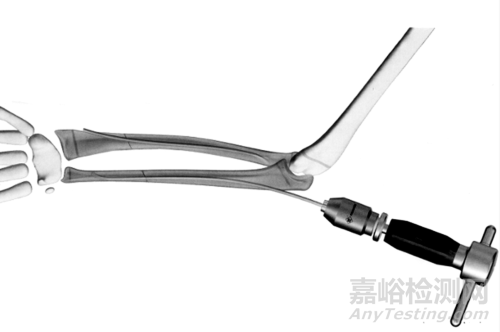
▲通用逆行髓内钉系统
脊柱植入物:用于脊柱的稳定和融合,包括椎间融合器、脊柱固定系统(如椎弓根螺钉系统)、人工椎间盘等。

▲不同形状的聚醚醚酮脊柱融合器
人工关节假体:工髋关节、人工膝关节、人工肩关节、人工肘关节、人工踝关节、人工腕关节、人工指关节等。其中,人工髋关节和人工膝关节发展最为成熟,应用最为广泛。
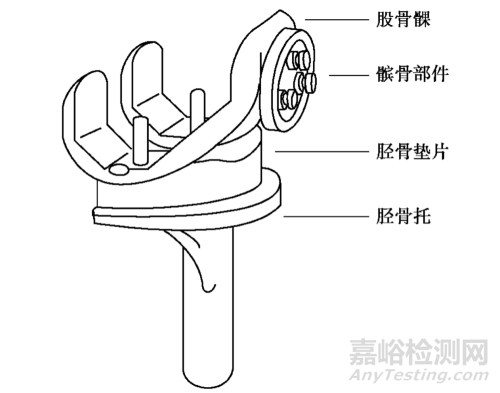
▲常见全膝关节假体
这些骨科植入物在临床上有着广泛的应用,它们通过提供稳定的固定和支撑,帮助恢复骨骼的结构和功能。随着生物材料和制造技术的进步,这些植入物的设计和材料也在不断优化,以提高其生物相容性、力学性能和促进骨愈合的能力。
骨替代材料的主要特点包括:
生物相容性:材料应当不引起宿主体内的不良反应或免疫排斥。
生物活性:一些骨替代材料具有促进骨细胞增殖和分化的能力,从而加速骨组织的再生。
可塑性:材料应易于塑形或定制,以适应不同患者的具体解剖结构和手术需求。
力学性能:材料应具有足够的强度和韧性,以支持骨组织的生长,同时与人体骨骼的弹性模量相近,防止应力屏蔽效应。
可降解性:许多骨替代材料设计为可被体内自然降解和吸收,以便随着时间推移被新形成的骨组织所取代。
骨移植材料
骨是天然的生物复合材料,具有精巧的多级结构(图4-2-1)。磷酸钙类矿物相可占骨重量的60%~70%,有机相的90%~95%为胶原蛋白,还有少量的非胶原性蛋白、多糖、脂类等。骨移植按材料来源可分为天然材料和合成材料两大类;按移植入物来源分为自体骨移植、同种异体骨移植、异种骨移植和人工骨材料移植。骨移植材料在整形外科中主要用于骨断裂修复、骨植入物的镀膜、人工关节返修、可注射骨移植材料治疗骨质疏松等适应证,在脊柱治疗中主要用于后路脊柱融合等各类脊椎骨缺损适应证,在牙科中主要用于拔牙创伤和颌面外科等适应证。
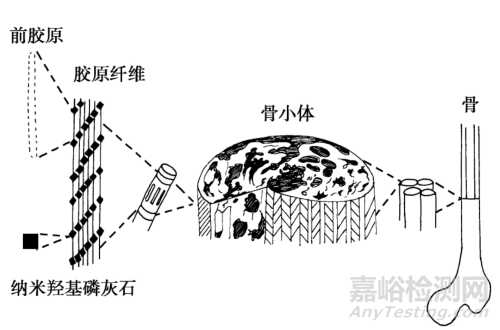
骨移植材料是用于修复或替换受损骨组织的生物医用材料。这些材料被设计来填充骨缺损或提供骨组织的结构支持,促进骨愈合和再生。骨移植材料可以是自体的(来自患者自身的骨组织)、异体的(来自同种其他个体的骨组织)、异种的(来源于其他物种,如牛或猪)、或合成的(人工制造的材料)。
天然骨移植物
天然骨移植物是骨科和牙科手术中常用的材料,用于修复或重建骨缺损和损伤。这些材料来源于自然,能够提供良好的生物相容性和生物活性。以下是对天然骨移植物的详细介绍,包括自体骨、同种异体骨、异种骨以及天然衍生骨材料的特点和应用。
1. 自体骨、同种异体骨及异种骨
自体骨移植(Autograft)
自体骨移植是指从患者自身的一个部位取骨移植到另一个部位。这种移植物被认为是理想的骨移植材料,因为它具有最佳的生物相容性和成骨能力,不会引起免疫反应。自体骨移植又可分为非血管化自体骨移植和血管化自体骨移植。非血管化移植操作相对简单,故而很早就得到了应用,随着显微外科技术的进步又发展出了血管化移植,通过血管吻合使移植骨保持良好的供血以保存骨的再生能力,大大增加了移植骨的成功率,并且提高了自体骨移植的质量。非血管化自体骨移植的来源主要有髂骨、胫骨和颅盖骨等;用于血管化自体骨移植的主要有:肩胛骨肌皮瓣、腓骨肌瓣、背阔肌骨肌皮瓣、髂骨肌瓣等。
优点:无免疫排斥反应,高成骨能力。
缺点:取骨区可能出现并发症,如疼痛和感染;可用骨量有限。
同种异体骨移植(Allograft)
同种异体骨是来自同种其他个体(通常是捐献者)的骨。这种骨移植物在骨传导性方面表现良好,经过处理还可以保留一定的骨诱导性。同种异体骨采集来源:(1)截肢的骨组织。(2)胸部手术中切除的肋骨。(3)新鲜尸体骨骼,包括死婴多采用软骨。禁忌采集来源于肿瘤、传染病、细菌性感染、骨病、血液病患者的骨组织。按移植物的不同分为同种异体骨移植、同种异体软骨移植、同种异体骨关节移植。按移植物处理的不同分为新鲜同种异体骨、库骨、人骨基质明胶。同种异体骨移植能避免自体骨移植的一些缺点,存在的主要问题是,有排斥反应和交叉感染的风险。所以同种异体骨需处理才能使用,处理目的是降低或消除异体骨的免疫原性。但经过各种处理的异体骨,骨细胞皆妥到不同程度的破坏,甚至死亡。异体骨在宿主部位的成骨生物学效应,主要表现为骨传导和骨诱导。异体骨经过处理后是死骨,一旦与宿主骨床相接触,即逐渐被吸收,即在吸收骨表面上贴覆性生长,通过吸收,异体骨将被宿主骨及骨外膜的成骨细胞所“爬行替代”,从而产生新骨。
优点:可用于大段骨缺损,提供良好的机械支持。
缺点:可能引起免疫反应,传播疾病的风险;需通过严格的筛选和处理。
处理方式:包括新鲜骨、深冻骨和冻干骨。冻干骨(lyophilized bone)由于其较低的免疫原性通常更受青睐。
异种骨移植(Xenograft)
异种骨移植是指来源于其他物种的骨材料。这些材料需经过特殊处理以降低免疫反应和疾病传播风险。异种骨材料的来源主要有牛骨、猪骨、鹿骨、绵羊骨等,其中猪骨和牛骨原料易得,是研究最多的异种骨材料。关于异种骨目 前比较一致的观点是认为异种骨免疫原性和诱导活性具有共同的物质基础,在消除抗原性的同时也破坏了诱导成骨物质,因此单纯异种骨无法解决消除抗原性和保持诱导活性之问的矛盾。将去抗原异种骨具有骨活性的物质相结合制成复合异种骨,以部分恢复异种骨的诱导成骨能力,能够在一定程度解决这一问题带来的困难,目前成为了异种骨移植研究的新方向,如:异种骨与骨形态发生蛋白(BMP)的复合,异种骨与自体红骨髓的复合、异种骨与骨基质明胶的复合以及异种骨与多种生长因子的复合等。
优点:来源广泛,适用于不需要高机械强度的场合。
缺点:免疫反应和生物相容性问题较为突出,需要精细化处理。
2. 骨衍生材料
在骨修复和再生医学领域,骨衍生材料发挥着重要作用,通过从天然生物组织提取和加工,得到具有特定生物功能性的材料。这些材料主要可以分为骨支架材料和骨基质材料,每种类型的材料都有其独特的优点和潜在的应用领域。以下是对这些材料的详细介绍:
骨支架材料
煅烧骨(Calcined Bone):煅烧骨是通过高温处理异种或异体骨,去除其中的有机成分(如脂肪和蛋白质),主要留下无机成分羟基磷灰石。
优点:
良好的生物相容性:高温处理彻底去除了潜在的抗原性物质。
优秀的骨传导性:保留了天然骨的微观结构,有助于细胞黏附和增殖。
缺点:
脆性:煅烧过程可能影响材料的机械强度,使其变得脆弱。
缺乏骨诱导性:高温处理破坏了天然骨中的生物活性成分。
珊瑚羟基磷灰石(Coral Hydroxyapatite, C.HA):来源于海生珊瑚,通过物理和化学方法转化成主要由磷酸钙和碳酸钙组成的材料。
优点:类似人骨的多孔结构:其结构模仿人体骨的松质结构,有助于新骨的生长。适合骨内生长:孔径适合新生骨的内向生长。
缺点:力学性能有限,虽具有一定的抗压强度,但抗拉和抗剪强度较低。
骨基质材料
脱钙骨基质(Demineralized Bone Matrix, DBM):主要包含脱钙后的骨胶原和其他细胞外基质。其优点如下:
促进骨愈合:富含生长因子和促进血管生长的成分。
广泛用途:常用作粘合剂,与其他骨替代物混合使用,提高复合材料的整体性能。
应用:常作为自体骨扩增剂或与其他材料如羟基磷灰石混合使用。
脱蛋白骨基质(Decellularized Bone Matrix):通过化学方法去除异种骨中的蛋白质成分,保留羟基磷灰石和天然骨结构。其优点如下:
良好的生物相容性和力学性能:保留了天然骨的三维网状孔隙系统。
低抗原性:几乎完全去除抗原性,降低免疫反应风险。
其缺点如下:
缺乏骨诱导性:处理过程中可能破坏活性成骨物质。
这些骨衍生材料各具特色,广泛应用于骨科和牙科的骨修复和再生治疗中。选择合适的材料需要根据具体的临床需求、预期的生物功能以及患者的具体情况来决定。随着材料科学的进步,未来可能开发出更高效、更具生物活性的新型骨衍生材料。
合成骨移植物
合成骨移植物在现代医疗中扮演着越来越重要的角色,特别是在骨科和牙科手术中。这些材料的开发旨在模仿自然骨的功能,同时避免了自体骨移植和异体骨移植中的一些限制和风险。合成骨移植物可以根据其成分和性能大致分为无机骨移植材料、有机骨移植材料和复合骨移植材料。
1. 无机骨移植材料
无机骨移植材料主要分为金属填充材料和陶瓷填充材料两大类。金属填充材料以其卓越的力学性能和加工易性而广泛用于制造人工关节和植入体固件,常见的材料包括不锈钢、钛及钛合金、钴基合金和镍钛合金等。这些金属材料由于其高强度和良好的生物相容性,在骨科植入物中发挥着关键作用。
另一方面,陶瓷填充材料主要用于骨移植,包括氧化铝陶瓷、羟基磷灰石和生物玻璃等。这些材料不仅具备良好的力学性能,还显示出对体液的高度惰性。特别是含钙磷盐的陶瓷,如羟基磷灰石,因其出色的生物相容性和骨诱导能力,受到了广泛的关注和深入研究。磷酸钙生物陶瓷是其中一种早期广泛使用的骨填充材料,已被证实能有效促进骨愈合,提供骨传导作用及骨诱导能力。
2. 有机骨移植材料
有机骨移植材料方面,超高相对分子量的聚乙烯因其优异的力学性能,广泛应用于耐磨植入件如髋关节和膝关节。
聚丙烯酸酯类材料中,聚丙烯酸甲酯(PMA)和聚甲基丙烯酸甲酯(PMMA)尤为突出。聚甲基丙烯酸甲酯(PMMA)与日常生活常用的有机玻璃成分相似,PMMA聚合的反应放热明显高于玻璃高分子聚合物,达到78~120°C,术中保护其接触的组织,避免造成热损伤甚至烫伤引起组织坏死尤为重要。PMMA广泛应用于关节置换术中假体和自体骨的粘合。
硫酸钙骨填充材料中半水硫酸钙因其固化速度快,常做成可注射型的。在使用时应注意使硫酸钙紧贴有活力的骨外膜或骨内膜,这样硫酸钙才具有提供血管内向性生长的骨传导性基质作用。硫酸钙在体内经过5周即可溶解而被重吸收,根据这一特点硫酸钙能够作为抗生素的缓释载体用于骨髓炎的治疗。
3. 复合骨移植材料
在复合骨移植材料的研究中,矿化胶原基复合人工骨和玻璃高分子聚合物等表现出了良好的临床应用前景。
复合骨移植材料研究较多的人工骨材料有:矿化胶原基复合人工骨,玻璃高分子聚合物等。矿化胶原基人工骨是与天然骨成分和结构接近的一种室温合成的骨移植物产品,使用效果接近自体骨。这种材料具有高孔隙率的多孔结构,便于细胞附着和生长,其主要成分是Ⅰ型胶原蛋白和羟基磷灰石晶体,这些晶体的纳米级小尺寸和特定的晶体取向使得材料具有良好的生物相容性和降解性,同时其力度可调,便于临床操作和形状定制。

材料具有四个显著的特点:
一是材料具有多孔结构、孔隙率较高,便于细胞在上面的爬行、附着、生长和繁殖以及营养物质的输运,其矿物相为具有低结晶度纳米量级含碳酸根的羟基磷灰石,并且均匀生长在胶原基质上,这些特点原则上使该材料本身便具有与骨键合的能力,用这种材料制成的骨植入体表面可提供适宜的环境促进胶原和矿物的沉积以及成骨细胞的黏附,一旦成骨细胞黏附于植入体表面,随后的骨生长便在细胞的调节下进行;
二是材料主要成分是Ⅰ型胶原蛋白和羟基磷灰石晶体,其物理及化学性能均能满足体内植入环境的要求,有很好的生物相容性以及降解性能,降解速度与成骨速度相匹配,并且降解过程中不引起周围体液环境pH值的变化;
三是材料中的羟基磷灰石晶粒非常的细小,具有纳米晶的尺度,并且羟基磷灰石晶体的C轴平行于胶原纤维的长轴,与天然骨材料结构相似,而普通羟基磷灰石骨替代品体尺寸较大,较难被破骨细胞吸收、降解,长时间植入体内也难以被吸收、替代,而小的羟基磷灰石晶粒使得其易于为破骨细胞吸收、降解;
四是复合材料的强度接近于松质骨,并可根据需要进行调整,能够方便用手术刀塑形,临床使用非常方便。临床使用情况表明,其与人体生物相容性良好,无免疫排斥反应,愈合情况良好,是安全有效的新型骨移植材料。
硫酸钙基复合材料通过与有机高分子或无机陶瓷的复合,不仅提高了其力学强度,还保持了良好的生物活性,使其成为治疗骨髓炎等疾病的有力工具。力学性能是指材料在不同环境(温度、介质、湿度)下,承受各种外加载荷(拉伸、压缩、弯曲、扭转等)时所表现出的力学特征,研究表明,硫酸钙与有机高分子或者无机陶瓷复合后,其力学强度均能得到有效提高,且介于皮质骨(90~230MPa)与松质骨(2~45MPa)之间。
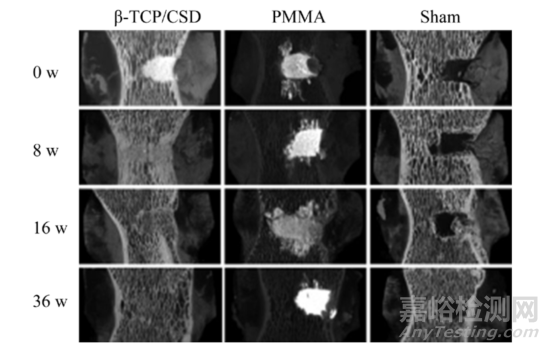
▲成熟羊椎体骨缺损填充修复术0~36 w后三维重建图
硫酸钙与有机高分子主要通过化学键形成稳定结构。在Lewis等的研究中,磁共振检测CS/羧甲基纤维素复合材料中-COOH与钙离子形成新的化学键;对于不同羧甲基纤维素含量(5%、7.5%、10%),复合材料的抗弯强度分别增加99%、103%、124%;其中7.5%、10%组的抗压强度分别增加88%、85%。Gao等也发现CS和聚乳酸复合时-COOH与钙离子形成化学键;扫描电镜下硫酸钙(硫酸钙含量低于50%)均匀分散在聚乳酸基质中;其中CS含量为40%时,抗压强度最大,为82MPa。
硫酸钙与无机陶瓷材料则主要通过物理连接形成稳定结构,不同材料类型、晶相以及比例均会影响复合材料力学强度。硫酸钙/羟基磷灰石的结构主要靠硫酸钙基质维系,羟基磷灰石只是单纯地整合到其中,因此随着硫酸钙含量降低,力学强度会有所降低。在硫酸钙的所有晶相中,半水硫酸钙通过水合作用可快速自固化为硬度更大的二水硫酸钙,这对于临床上骨缺损重建的早期负重有重要意义。
复合材料不仅提供了结构支持和骨传导性,还具备一定的骨诱导性,且在免疫排斥反应方面表现更好。这些材料的发展和应用极大地丰富了骨修复的选择,提高了治疗的灵活性和有效性。通过不断的研究和技术进步,合成骨移植材料在未来的医疗应用中将发挥更加关键的作用。
组织工程骨
组织工程骨是一种先进的医疗技术,它通过结合生物学、工程学和医学的原理,体外构建新的骨组织用于修复骨缺损。这一技术主要涉及三大核心要素:种子细胞、生物支架材料和生长因子。种子细胞是进行组织重建的基本单元,通常来源于患者自身或捐赠者,以确保细胞的生物相容性和减少免疫排斥反应。生物支架材料则提供了一个三维立体多孔的结构,这不仅支持细胞的附着和生长,还有助于维持细胞的分布和传输营养物质。生长因子则是促进细胞增殖和分化的关键因素,有助于加速组织的形成和成熟。
组织工程中使用的生物医用材料可分为天然生物材料和合成生物材料两大类。天然生物材料如胶原蛋白、羟基磷灰石和明胶等,由于其出色的生物相容性和生物降解性,能够有效地支持细胞的黏附、增殖和分化,而且通常对人体无毒副作用。这类材料的主要优势在于它们能够提供与人体细胞相似的生物化学和生物物理环境,从而促进新组织的形成和整合。然而,天然材料的主要限制在于其加工性和重现性较差,以及难以精确控制其降解速度,这可能在临床应用中带来一定的挑战。
相比之下,合成生物材料如聚乳酸、聚甘醇酸和聚己内酯等,提供了更广泛的选择范围和更好的加工性能。这些材料的生物降解速度可以根据需要进行调整,其力学性能也可以设计以满足特定的临床需求。合成材料的价格通常较低,且具有较好的重现性,便于大规模生产。然而,它们的主要缺点在于与天然材料相比,其生物相容性和细胞亲和性较差,这可能限制了它们在某些临床应用中的效果。
尽管组织工程骨的发展时间不长,但其已经显示出极大的发展潜力和应用前景。通过优化支架材料的设计、改进种子细胞的处理方法和增强生长因子的应用策略,未来的组织工程骨有望在骨修复和重建领域中发挥更加重要的作用。这一技术的持续发展不仅有助于改善传统骨移植方法的限制,还可能为治疗复杂的骨缺损病例提供更有效的解决方案。
软骨替代与移植材料
软骨是一种特殊的结缔组织,由软骨细胞(称为软骨细胞)、纤维和基质组成,具有重要的生理功能和结构特性。软骨的结构使其能够承受压力和作为骨骼系统的重要组成部分。
软骨细胞:软骨细胞,或称为软骨细胞,通常呈圆形或椭圆形,位于被称为软骨陷窝的小腔中。这些细胞负责形成纤维并分泌基质,是软骨生长和维护的活跃成分。软骨陷窝周围的区域富含硫酸软骨素,并被称为软骨囊,这种结构有助于保护细胞并与周围基质进行物质交换。
纤维性软骨膜:软骨的外部被包裹着一层纤维性软骨膜,这是一种较硬的结缔组织,可以提供额外的支持和保护。它有助于软骨承受负载和与邻近的骨结构相连接。
细胞外基质:软骨的细胞外基质是其主要组成部分,由胶原蛋白、蛋白多糖、透明质酸以及水和电解质等液相成分构成。这个复杂的网络不仅支撑着软骨细胞,也为细胞提供了必需的生长微环境。基质的高含水量和透明质酸的特性使得物质能够通过基质自由渗透,即使在无血管的条件下也能为深层软骨细胞提供营养。
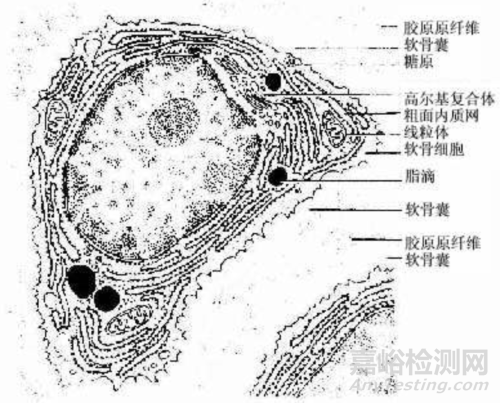
根据基质成分和结构的不同,软骨可以分为三种类型:透明软骨、弹性软骨和纤维软骨。
透明软骨是最常见的软骨类型,主要化学成分是蛋白多糖,特别是长链的透明质酸,其上附着有许多较短的蛋白多糖侧链。这些侧链主要是硫酸软骨素,它们与I型胶原蛋白纤维结合,形成一个能够承受压力的网状结构。透明软骨不具有周期性横纹,也不形成明显的胶原纤维束,但其结构足以承受较大的压力和张力。
弹性软骨含有大量的弹性纤维,使其具有更高的灵活性和弹性。这种类型的软骨主要存在于耳朵和喉结构中。
纤维软骨含有较多的胶原纤维,提供了更强的支持和抗张力能力。它主要出现在如膝盖的半月板和椎间盘等承受重压的区域。
总的来说,软骨的这些组成和特性使其能有效地承受压力和弯曲,同时提供关节和骨骼系统中关键的结构支持。
在临床上,修复软骨缺损主要采用多种方法,包括传统的手术技术和较新的生物技术。传统方法如软骨下骨钻孔和微骨折技术,通过刺激骨髓释放干细胞来促进软骨的自然修复。关节腔内的清理和灌洗术,以及关节削磨成形术,主要用于清除关节内的破碎组织和平滑关节表面,减少疼痛和改善功能。在某些情况下,严重的关节损伤可能需要通过人工关节置换来恢复关节功能。
在生物技术方面,组织移植技术,如自体或异体软骨移植,利用健康的软骨组织来填补缺损区域。自体软骨细胞移植则是一种更为精细的方法,涉及从患者自身的软骨中提取细胞,实验室中扩增这些细胞后,再将它们注射回缺损区域,通常在自体骨膜封闭的保护下进行。
最先进的方法之一是组织工程技术,它结合了种子细胞、支架材料和生长因子等元素,通过实验室培养和构建特定的软骨组织,再将其植入到损伤区域。这种方法不仅提供了修复材料,还通过生长因子促进了细胞的增殖和分化,从而加速了软骨的再生过程。
1. 骨膜及软骨膜替代关节软骨:
骨膜含有丰富的神经和血管,提供营养和感觉作用,并含有多能造血干细胞和间充质干细胞,这些干细胞具有分化成软骨的潜能。研究表明,骨膜在植入关节软骨缺损处可以促进透明软骨的形成及软骨下骨的形成。尽管骨膜具有取材方便和对机体损伤小的优点,但其在临床应用中存在固定困难、来源有限及无法完全达到生理力学要求等限制。
2. 自体或异体软骨及软骨细胞移植替代关节软骨:
自体软骨细胞移植是一种通过获取患者自身非负重区域的健康软骨细胞,经过体外培养和扩增后,再植入损伤的软骨区域的方法。这种方法已被证明能够保持软骨下骨的完整性并阻碍成纤维细胞引起的纤维修复。异体软骨细胞移植则显示出与自体软骨细胞移植相似的修复效果,但免疫反应和细胞保存是其主要问题。
3. 人工软骨的替代材料:
人工软骨替代材料应具备良好的生物力学性能、优良的润滑性和耐磨性、软骨细胞生长诱导性以及与骨基底牢固的连结性和生物相容性。当前常用的高弹性材料如硅橡胶、聚氨酯和聚乙烯醇水凝胶等各有其优缺点,例如硅橡胶易老化失效,聚氨酯的降解性能需改进。研究重点在于改进现有材料和制备工艺,探索新材料。
4. 组织工程化软骨:
组织工程化软骨是通过种子细胞和生物支架的结合来实现软骨的再生。理想的软骨组织工程种子细胞应具有如下特点:
取材方便,来源充足,对机体损伤小。
体外培养增殖能力强。
与支架材料具有很好的黏附性。
种子细胞植入人体后能够适应内在环境并保持原有软骨细胞的特性。
当前研究主要关注于自体软骨细胞、异体软骨细胞、间充质干细胞和胚胎干细胞等。支架材料的选择既有天然来源的生物材料,也有人工合成的支架材料,关键在于支架的设计和正确的材料选择,以确保支架的机械稳定性和促进种子细胞的增殖和迁移。
肌腱组织替代与移植材料
肌腱是一种典型的规则致密结缔组织,其主要作用是连接肌肉和骨骼,从而在肌肉收缩时传递力量,使骨骼移动,完成各种身体动作。肌腱的结构与功能密切相关,主要由三部分构成:胶原束、腱胶质和腱细胞。
胶原束:这是肌腱的主要成分,由大量平行排列的胶原纤维组成。这些纤维的排列方式使得肌腱具有很高的抗拉伸能力,能够承受肌肉产生的力量。
腱胶质:是填充在胶原纤维之间的基质,含有蛋白多糖和水分,帮助肌腱在承受压力时保持结构的稳定和弹性。
腱细胞:主要有纤维细胞和间质细胞,分布在胶原纤维之间,负责合成和分泌胶原蛋白及其他基质成分,维护肌腱的结构和功能。
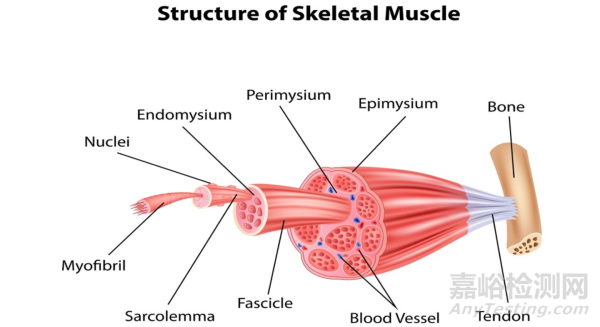
由于肌腱需要适应高度的张力,它们在运动中承受着极大的拉伸载荷。过度使用、猛烈运动或外部意外事故(如刀割、压轧伤)都可能导致肌腱损伤。常见的损伤包括肌腱撕裂或断裂,这些损伤如果不及时治疗,可能导致永久的功能障碍或残疾。
肌腱的自我修复能力非常有限,主要是因为肌腱的血供相对较差,修复过程缓慢且往往不能完全恢复原有的结构和功能。在临床上,严重的肌腱损伤可能需要通过外科手术进行修复,包括缝合断裂的肌腱或使用移植物来替代受损的部分。
肌腱损伤是常见的运动伤害,尤其在高强度或重复性使用肌肉的情况下。现代医学在肌腱损伤的修复与替代方面已发展出多种方法,主要包括自体肌腱移植、同种异体肌腱移植、异种肌腱移植和人工肌腱替代物。
自体腱移植
自体腱移植是使用患者自身的其他健康肌腱进行修复。这种方法的主要优点是避免了免疫排斥反应,因为移植材料来自患者自身。20世纪初,Kirschner及其他学者通过使用自体腱进行缺损修复的研究,证实了这种方法的可行性。然而,自体腱移植的主要缺点是可用的肌腱资源有限,且在提取肌腱的同时可能损伤供腱部位,有时还可能因供腱部位的强度不足而导致撕裂。
同种异体肌腱移植
同种异体肌腱移植使用来自同种族但不同个体的肌腱。这种方法扩展了可用于移植的肌腱资源。然而,研究表明,这种移植方法存在较高的失败率,主要问题包括植入的肌腱坏死和排斥反应。此外,还存在供体病毒传播的风险,如肝炎和AIDS,使得这种方法在临床上的应用受到限制。
异种肌腱移植
异种肌腱移植使用来自不同物种的肌腱。这种方法在理论上可以提供丰富的肌腱资源,但免疫排斥反应和生物相容性问题仍然是主要的挑战。尽管通过化学处理如使用多聚甲醛、冷冻和戊二醛等方法可以减少肌腱的免疫原性,但这些处理方法可能改变肌腱的生物力学性能,影响修复效果。
人工肌腱替代物
人工肌腱替代物涵盖了广泛的材料,包括合金、塑料、尼龙和合成纤维等。这些材料的设计旨在模拟自然肌腱的功能。然而,许多尝试因材料的机械性能不足或与周围组织的兼容性差而失败。例如,碳纤维人工腱虽在初期被认为有潜力,但由于不能吸收、拉应力衰减和严重粘连等问题,最终被淘汰。目前,研究者正在探索新的材料和技术,如人发角蛋白人工肌腱和组织工程人工肌腱,以期提高人工肌腱的性能和生物相容性。
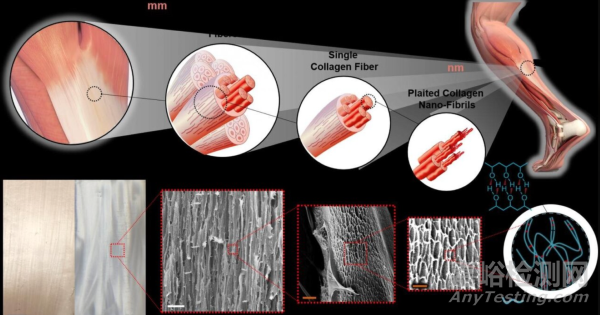
1. 人发角蛋白人工肌腱 (HHKAT)
人发角蛋白人工肌腱利用人发的角蛋白作为原料,经过特殊的生物化学处理,形成可用于肌腱修复的生物材料。这种材料的主要优点包括:
良好的生物适应性:人发角蛋白人工肌腱具有良好的生物相容性,能够在体内逐渐腱化成自体腱,与周围组织无明显粘连。
无免疫排斥反应:由于经过特殊处理,这种人工肌腱在体内不引起免疫排斥反应。
持久的力学性能:拉应力不衰减,能够承受长期的肌肉运动牵拉。
腱化工程:能够在体内被吸收的同时形成新的自体腱,这一过程被称为腱化工程。
这种材料的开发标志着人工肌腱技术的一个重要进步,尤其是在提高修复肌腱的功能性和降低手术并发症方面。
2. 组织工程化人工肌腱
组织工程化人工肌腱采用肌腱种子细胞与生物降解材料复合的方式,通过体外培养后植入缺损部位,促进肌腱细胞的增殖和分化,最终形成新的肌腱组织。这种方法的主要优点包括:
高度的自然化修复:形成的肌腱组织具有活力和功能,能够实现永久性替代。
形态和功能的完美重建:可以根据缺损肌腱的具体形态进行塑形,达到高度匹配的形态修复和功能重建。
无免疫反应和病原传播风险:使用的种子细胞可以是自体细胞,降低了免疫排斥和疾病传播的风险。
组织工程技术的关键在于选择合适的种子细胞和支架材料,以及种子细胞与支架材料的有效复合。支架材料不仅要具有良好的机械强度以支持早期活动,还要能够与细胞功能同步降解,为细胞的生长和生理功能提供空间。
骨科内固定材料
骨科内固定材料指的是种种用于内部固定的医疗器械,它们可以被植入体内,用于稳定和支持骨折、畸形、肿瘤切除后的骨缺损等情况。这些材料设计用来承受体内环境的挑战,如生物相容性、耐腐蚀性以及足够的机械强度来支持骨愈合过程。骨科内固定材料可以根据其类型、用途和所用材质进行分类。主要类型包括:
|
固定器类型 |
描述 |
用途 |
|---|---|---|
|
金属固定器 |
钢板和螺钉:用于固定长骨骨折,如股骨、胫骨和肱骨。 钉棒系统:例如股骨内钉,用于股骨骨折。 外科钢丝和销钉:用于小骨折或小骨的固定。 |
骨折固定 |
|
非金属固定器 |
聚合物固定器:如聚乳酸(PLA)和聚甘酯(PGA)制成的螺钉和板,这些材料可以生物降解,无需二次手术取出。 陶瓷固定器:用于骨缺损的填充,如磷酸钙(如羟基磷灰石)。 |
骨折固定,特别是需要生物降解材料的情况 |
|
生物固定器 |
骨移植:使用自体骨或异体骨进行骨缺损的填充。 骨形成蛋白:如生物活性材料和生长因子,用于促进骨再生。 |
骨缺损填充,促进骨再生和骨愈合 |
|
混合材料固定器 |
复合材料:将金属与聚合物、陶瓷或生物活性物质结合使用,以利用各种材料的优点。 |
需要结合不同材料优点的复杂骨折固定情况 |
在骨折治疗中,内固定技术是恢复骨折部位稳定性的关键方法,它允许早期负重和肢体活动,从而促进骨折愈合。内固定的选择和应用涉及了骨折类型、患者年龄、预后预期等多个因素。如骨折的稳定性需考虑以下五种主要力量的影响:
压缩力:通过轴向传递,增加骨骼的负重,常见于脊柱的压缩骨折。
张力:同样通过轴向传递,导致骨折分离。
弯曲力:使骨的一侧承受压力而对侧承受张力。
扭转力:使骨骼承受旋转力量。
剪切力:由压缩力引起,导致斜行骨折。
为确保骨科内固定材料的有效性和安全性,使用的材料需要满足以下关键条件:
1. 具有足够的强度
内固定设备必须具备足够的强度以支撑骨折愈合过程中的负载。不同材料的特点如下:
不锈钢:具有良好的机械性能和成本效益,易于加工,广泛用于制造各种内固定设备。生物活性相对较高,但在高负载环境下可能发生腐蚀。
钴铬钼合金:生物活性低,具有极高的耐腐蚀性和机械强度,但成本高,加工难度大。
钛合金:重量轻,抗腐蚀性强,具有良好的生物相容性和较低的生物活性。钛合金的弹性接近人骨,适合制造长期植入体。在CT和MRI检查中几乎不产生伪影,便于跟踪检查。
聚乳酸为主的可降解材料:生物相容性好,使用后可自然降解为水和二氧化碳,免去二次手术取出的需求。适用于不承受高负载的内固定场景。其长期应用的生物安全性仍在研究之中。
2. 无组织反应
材料应当是生物相容的,不引发毒性反应、炎症、纤维化或巨噬细胞活化。这些生物反应可能引起植入区域的疼痛、肿胀和功能障碍,甚至罕见情况下可能导致肿瘤形成。因此,对于年轻人而言,一旦骨折愈合,通常建议取出内固定装置。
3. 不腐蚀
植入体不应生锈或产生电解反应。使用不锈钢时,应确保其纯度高、无杂质,以防腐蚀。此外,还应采取措施防止不同内固定材料之间的接触,以避免界面腐蚀。使用相同材质的内固定组件也是防止电解腐蚀的一种有效方法。
内固定技术的演变
AO/ASIF系统是一种经典的内固定系统,由Mueller和其他骨科医生于1956年创建。该观点主要关注通过内固定技术实现骨折的解剖复位和稳定,以促进骨折的直接愈合。AO团队开发了一套全面的内固定系统,包括螺钉、钢板、髓内钉等,以及详细的手术技术和原则。AO观点的核心原则包括:
骨折端的解剖复位:尤其是关节内骨折,强调必须尽可能实现完美的解剖复位。
坚强的内固定:通过精确设计的内固定系统,提供足够的稳定性以满足生物力学需求。
无创外科操作技术:手术中尽量保护骨折端及周围软组织的血供,减少手术造成的额外损伤。
早期活动:通过稳定的内固定支持,患者可以尽早开始肌肉及关节的活动,以防止长期卧床带来的并发症。
AO观点强调机械稳定性是实现骨折愈合的关键,而操作的精确性和内固定的质量直接影响治疗的成功。
BO观点,即生物学固定观念,是对AO观点的一种补充和发展。它在20世纪末期到21世纪初期逐渐形成,主要强调在骨折治疗中保持或恢复骨折区域的生物环境和血供。BO观点认为,过度的机械固定可能对骨折部位的生物环境造成负面影响,如应力屏蔽导致骨质疏松,以及手术本身对软组织造成的损伤。因此,BO观点提出以下原则:
保护软组织和血供:在手术中尽量减少对骨折区域及其周围软组织的干扰,保持血供。
适度的内固定:使用生物相容性好、弹性模量低的材料,以减少对骨的应力屏蔽和促进骨折愈合。
避免过度复位:对于粉碎性骨折,不强求完全的解剖复位,尤其是非关节内骨折。
微创手术技术:使用微创技术以减少手术对患者整体的影响,加速恢复。
微创内固定技术(MIPO):近年来,微创手术技术的发展旨在减少手术对软组织的损伤,从而保护血供并促进更快的愈合。
随着对骨折治疗的更深入理解,传统的机械固定观点逐渐向生物学固定观念转变。生物学固定考虑到以下几点:
保护局部软组织:远离骨折部位进行复位,以保护局部软组织的附着。
不强求粉碎性骨折块的解剖复位:除非是关节内骨折,否则不必追求完美的解剖复位。
使用生物相容性好的材料:如低弹性模量的材料,减少内固定物与骨之间的接触,以减少应力屏蔽效应。
减少手术暴露时间:尽量缩短手术时间,减少对患者的整体影响。
骨科外固定器支架及应用
骨科外固定器是一种用于骨折治疗和矫形手术中的医疗设备,通过在体外固定支架稳定骨折部位或纠正畸形。它们通过皮肤穿透针或销固定在骨头上,外部结构提供必要的支撑和稳定,以促进骨折愈合或矫正骨骼畸形。外固定器适用于不能使用内固定的复杂骨折、感染或需要进行渐进式调整的情况。
骨外固定器实际上是一种介于骨科内固定与外固定之问的第三种固定方式,以微小的创伤对骨折或脱位进行部分制动式固定。它兼并了内、外固定的优点,与内固定相比,损伤更小,伤口感染率更低,与小夹板、石膏等外固定方式相比,固定更年靠、稳定。但它也有其自身的不足和缺点,因此选择应用骨外固定器时,应该严格掌握他们的适应证和禁忌证。
骨外固定器主要由固定针、连接杆及固定螺栓和螺母组成。固定针用于穿入骨骼内把持骨骼,而针尾留在体外,被连接杆连接、固定。固定针的类型主要包括斯氏针(Steinmann针),多用于成人下肢骨折;克氏针(Kirscher针),多用于成人上肢骨折及儿童的上、下肢骨折;针尖段带螺纹的半螺纹针(Schanz针),多用于半针固定;针中段带有螺纹的螺纹针,多用于全针固定。连接杆具有连接、固定各针尾作用,以钢管式、螺纹棒式和钩槽式多见。固定螺栓和螺母主要起连接固定针和连按杆的作用。
骨科外固定器可以根据其设计、功能和使用目的进行分类。主要类型包括:
单侧外固定器
定义:固定装置位于骨折一侧,通过连接杆和针销将骨片固定。
应用:适用于较简单的骨折或当局部皮肤条件不允许使用环形或双侧固定器时。
双侧或多侧外固定器
定义:固定装置位于骨折两侧或多个侧面,通过多个连接杆和针销提供更加均匀的支撑和稳定。
应用:适用于需要更稳定固定的复杂骨折或重建手术。
环形外固定器(如伊利萨洛夫装置)
定义:采用一系列环形结构通过钢丝或销钉固定骨折或畸形部位,环与环之间通过连接杆相连。
应用:广泛用于复杂的骨折、长骨延长手术或重度畸形矫正。特别是在小儿骨科中,用于治疗严重的四肢畸形。
混合型外固定器
定义:结合环形和单侧或双侧固定器的特点,利用环形结构提供稳定性,同时使用单侧或双侧支架进行局部调整。
应用:适用于极为复杂的骨折或需要高度定制的畸形矫正。
动态外固定器
定义:允许或控制特定关节的运动,同时固定周围的骨折区域。
应用:主要用于关节附近骨折的治疗,可以在保证骨折稳定的同时,促进关节功能的恢复。
选择适合的外固定器时,需要考虑以下因素:
骨折类型和位置:不同类型的外固定器适用于不同类型和位置的骨折。
患者的年龄和健康状况:儿童和成人的骨质密度、皮肤条件等因素可能影响外固定器的选择。
治疗目标:是否需要动态调整或长期穿戴,以及是否需要考虑日后的功能恢复。
外固定器的复杂性与维护:一些复杂的设备可能需要患者和医疗团队进行更频繁的监控和调整。
骨科生物可吸收内固定材料
自20世纪60年代后期以来,科学家们一直在探索和开发生物可吸收材料在医学中的应用。聚乳酸(PLA)作为一种生物降解可吸收材料,因其良好的生物相容性、可靠的力学强度、无毒副作用以及使用方便不需要二次手术取出等优点,在骨科疾病的手术治疗中取得了一定的良好效果。多年来,市场上最常见的可吸收材料是以聚乳酸为主的可吸收聚酯材料,例如聚左旋乳酸(PLLA)、丙交酯-己内酯共聚物(PLGA)、聚己内酯(PCL)等,这些材料的合成原理和路径与聚乳酸大同小异,且不同材料之间可互相“杂交”形成共聚物,因此最终可形成的种类繁多。
多种多样的生物可吸收螺钉、钉棒、接骨板、生物膜、缝线、椎间融合器等产品被研究及广泛地应用于骨科临床手术,因其特殊的优点而越来越多地被骨科医生使用以取代传统金属材料。
▲可吸收界面螺钉
材料学发展方面,聚乳酸(PLA)与高分子材料几乎同时诞生。早在18世纪的欧洲,人们就从发酵的牛奶中分离出乳酸,并通过直接缩聚的方法得到了最原始的PLA。乳酸是手性分子,它以左旋-(L)和右旋-(D)乳酸两种旋光异构体形式存在,可有以下四种不同形态的聚合物:PDLA、PLLA、PDLLA和meso-PLA,并拥有不同的性能。其中PDLLA和PLLA是两种有规立构聚合物,具有光学活性,聚合物链排列较规整,有较高的结晶度和机械强度,适合用于那些需要高机械强度和韧性的地方,如缝线、钉及矫形器械等。众多的实验研究证实PLA的降解是不需要其他酶参与的简单水解过程,可在体内水解为乳酸进入三羧酸循环,最终产物为水和二氧化碳被机体代谢排出体外。
与传统的金属材料相比,生物可吸收植入物具有各种优势,在降解过程中外力负荷逐渐转移到骨骼上,有效避免应力遮挡引起的骨质疏松;根据不同修复部位的使用设计最佳的降解速率,减少患者二次手术伤害;生物相容性好,安全无毒,高分子材料无金属磁性,因而不会对医学影像检查和出现安检产生干扰和影响。
可吸收骨折内固定植入器械已经得到医生和患者的接受和认可,逐渐替代金属器械的使用,但还有一些问题需要解决和完善:
可吸收固定器械的强度比金属器械强度低,因而应用范围受到限制,而且在术后初期,还需要配合必要的外部固定。生物力学方面,L-PLA的屈服强度为70MPa,延伸率仅为5%~10%,尚不足以满足其在骨组织修复和手术缝合的应用。生物可吸收内固定材料相比于金属材料的最主要缺陷也正是在力学强度以及吸收强度衰减变化过程不可控方面。因此许多学者在此方面进行了大量的研究。20世纪80年代至今,新的塑料增强工艺(包括自身增强、原位合成和拉伸等)的应用使生物可吸收材料的研究得到迅速发展,较之PLLA,有效强度大大增加。
近年来为了改善PLA的力学性能不足,自身增强技术被发明出来,即通过高温和高压下将缝合线纤维烧结在一起,生产出自我强化的柱形PLA棒。Tormala等自增强技术制得自增强聚左旋乳酸(SR-PLLA)棒材和螺钉,其初始弯曲强度达到250~271MPa,初始剪切强度可达94~98MPa,植入12周以后其弯曲强度仍有100MPa,36周后才降至10~20MPa达到松质骨水平,在植入的12周时间内剪切强度无明显变化。现在SR-PLLA已广泛应用于制造松质骨和四肢短管状骨骨折的内固定材料,在部分皮质骨骨折的治疗中也取得满意疗效。
骨折完全愈合后,可吸收材料仍然长期保持不必要的强度。因而,通过设计材料的组成及加工工艺,调控材料的降解速率,使其在骨折早期愈合的关键阶段保持足够强度,骨折部位完全愈合、康复(6个月左右)后快速降解、消失。
可吸收骨折内固定植入器械能够通过电子计算机断层(CT)扫描、核磁共振检测,但是在骨科常用的X射线影像中却检测不到,增加了现有手术检测的难度。
可吸收材料在体内降解过程中,如果酸性产物浓度过高,可能会造成局部的无菌性炎症,可通过在材料配方设计中加入可中和酸性物质的无机盐类组分来消除。
尽管可吸收骨折内固定植入器械还需要继续进行优化改良,但这类器械的应用仍可称得上是骨折治疗领域的一次革命性的换代。随着材料的制备和加工技术的快速发展、植入产品设计理念的不断创新、手术工具和手术方法的进步,可吸收骨折内固定植入器械必将迎来更加广阔的发展空间,更好地造福于骨折患者。

来源:骨未来
关键词: 骨科生物医用材料