嘉峪检测网 2025-03-23 13:49
导读: 本文对新版ICH《 Q9(R1):质量风险管理》的修订内容进行解读和探讨,期望为质量风险管理在制药企业的良好应用和发展提供一定的参考。
摘 要
国际人用药品注册技术协调会(ICH)发布的新版《Q9(R1):质量风险管理》是制药企业实施质量风险管理工作的重要依据,并在多部法规和指南中被提及。本文通过对新版ICH《 Q9(R1):质量风险管理》的修订内容进行解析和探讨,以期为制药企业质量风险管理的有效实施提供参考。
The International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH) released Q9(R1): Quality Risk Management, which serves as a crucial reference for pharmaceutical enterprises in implementing quality risk management and is cited in numerous regulations and guidelines. This article interprets and discusses the revised contents of the new ICH Q9(R1): Quality Risk Management with the aim of providing references for the effective implementation of quality risk management in pharmaceutical enterprises.
关键词
质量风险管理;ICH Q9(R1);解析;探讨;有效实施
quality risk management; ICH Q9(R1); interpretation; discussion; effective implementation
随着全球医药行业监管法规体系的逐步完善,质量风险管理受到越来越多的关注和认可。良好的质量风险管理既可以保证药品质量,又可以提高企业的经济效益,在药品全生命周期中发挥着不可替代的作用[1]。2023 年1月,国际人用药品注册技术协调会(ICH)正式发布了《Q9(R1):质量风险管理》[Q9(R1): Quality Risk Management],相较于《Q9:质量风险管理》(2005 年版),部分内容进行了修订和完善。
本文对新版ICH《 Q9(R1):质量风险管理》的修订内容进行解读和探讨,期望为质量风险管理在制药企业的良好应用和发展提供一定的参考。
1. 质量风险管理的发展历程
2004 年,美国食品药品监督管理局(FDA) 发布《21 世纪制药行业GMP :一种基于风险的方法》(Pharmaceuticalc GMPs for the 21st Century——ARisk-Based Approach), 首次在制药行业提出风险管理的概念[2]。2005 年ICH 正式发布《Q9 :质量风险管理》,2008 年作为附录20 收录在欧盟《人与兽用药品生产质量管理规范指南》(EU Guidelines to Good Manufacturing Practice Medicinal Products for Human and Veterinary Use),后于2010 年更新为该指南第二部分第二章。2009 年, 药品检查合作计划(Pharmaceutical Inspection Co-operation Scheme,PIC/S) 将其收录在PIC/S GMP 指南中。我国于2010 年在《药品生产质量管理规范》(Good Manufacturing Practice,GMP)第二章第四节中首次引入质量风险管理的概念和原则[1,3]。
2017 年原国家食品药品监督管理总局成为ICH 正式成员,国内制药企业需全面执行ICH 指导原则的要求,包括ICH《 Q9 :质量风险管理》[1]。2019 年国家药品监督管理局发布修订版《中华人民共和国药品管理法》,明确提出风险管理为药品管理的三大原则之一[1]。
2. 新版ICH《Q9(R1):质量风险管理》的修订内容
新版ICH《 Q9(R1):质量风险管理》的修订主要集中在质量风险管理流程图中的风险定义、质量风险管理的正式性理解、改善风险评估主观性、如何以风险为基础做决策、改善在产品供应和可及性方面的管理不足5 个方面。
2.1 质量风险管理流程的修订
质量风险管理基本流程包括:启动风险管理流程、风险评估、风险控制、质量风险过程的输出/结果、风险回顾和风险沟通。其中,风险评估由原来的“风险识别、风险分析和风险评价”修订为“危害源识别、风险分析和风险评价”。术语更改是为了与风险的定义更加一致,风险是严重性和可能性的组合,强调识别危害源时无须考虑其导致的严重程度和发生的概率,只需要识别任何有可能的危害活动。这一修订,有助于风险评估人员更多关注危害源的识别,提高对危害的感知[4]。修订后ICH《 Q9(R1):质量风险管理》流程图[5-6] 如图1 所示。
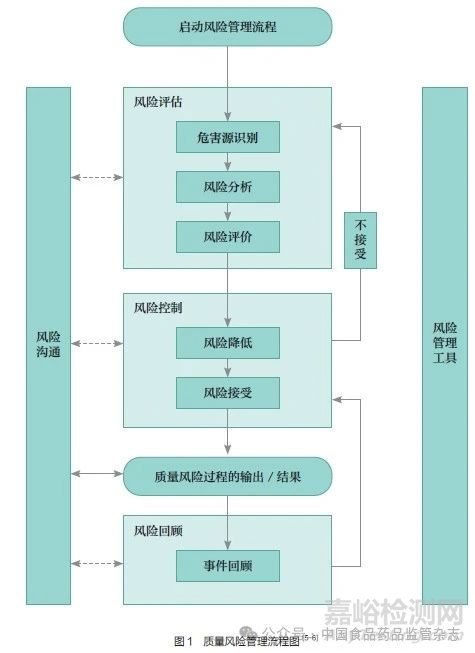
2.2 质量风险管理的正式性理解
质量风险管理应用于产品全生命周期,包括从产品研发、技术转移、商业化生产至产品退市的各个阶段[6]。考虑到不同企业对于风险评估的具体呈现形式有所不同,ICH《 Q9(R1):质量风险管理》新增了对质量风险管理的正式性和非正式性理解。
需要明确的是,非正式的质量风险管理方法和工具是可以接受的。在质量风险管理中应用正式程序,有助于资源得到有效利用。而对于低风险的问题,采用非正式的方式进行处理可节省资源,进而有助于优化资源配置,使更多的资源向高风险或者更复杂问题的处理倾斜。质量风险管理正式性的高低程度需考虑风险的不确定性、重要性和复杂性3 个因素,即不确定性、重要性或复杂性越高,则需要越正式的质量风险管理方法来支持决策。当然,应注意不应以资源限制为由,在质量风险管理过程中直接采用较低正式性的方式处理问题。这一变化也符合质量风险管理的原则之一,即质量风险管理实施过程的深度、正式性程度和文件化程度都应当与风险水平相适应[5-6]。
较高正式性的质量风险管理,需组建具有经验和专业知识的跨部门团队,应用公认的风险评估工具,遵循完整的流程(包括启动风险管理流程、风险评估、风险控制、质量风险过程的输出/结果、风险回顾和风险沟通等),并最终形成独立的风险评估报告。较低正式性的质量风险管理,不作为独立活动进行,可能包含风险评估和风险控制,穿插在质量体系其他因素的处理过程中,因此可能不会形成独立的风险评估报告,也不需要组建跨部门团队[5-6]。但风险评估的正式性并不是简单的二元概念(即正式性或非正式性),而是一个从低到高的、连续的、渐进的范围。
2.3 改善风险评估的主观性
目前,质量风险管理主要存在以下问题:①部分企业质量风险管理意识较弱,对经验的依赖性较大,判断者个人经验不同导致风险评估结果差异较大。即使存在风险管理程序,其对实际工作的正向引导作用也较小[7-8]。②风险评估工具仅限于失效模式与影响分析[7]。③风险管理评价标准不合理,缺乏科学合理评估[8]。
不同利益相关方在进行危害源识别以及风险评估时可能会有不同意见,并最终影响决策,因此ICH《 Q9(R1):质量风险管理》首次针对质量风险管理的主观性进行强调,要求最大限度降低主观性,主要方式包括降低偏见和假设、正确使用风险评估工具和最大限度运用相关数据和知识。
2.3.1 降低偏见和假设
一方面,确保决策者或高级管理者在实施质量风险管理工作中能发挥有效作用[5-6]。决策者或高级管理者负责组织协调各职能部门,并配置合理足够的资源,确保质量风险管理活动中的主观性得到控制并最大限度地减少,以促进基于风险的科学决策。
另一方面, 开展风险评估时组建跨学科团队, 组员应均为主题专家(subject matter expert,SME),即在某一特定领域有特殊技能的个人,包括产品研发专家、工艺研发专家、技术转移人员、工程技术人员、质量部门负责人、质量控制实验室负责人、公用设施负责人、确认/验证负责人或外部聘请的相关领域专家等[9]。小组成员需具备专业知识和经验,尽量减少不确定性影响。有研究表明,与非专业领域专家相比,专业领域专家受偏见和人类启发式思维的影响较小[10],其可通过头脑风暴和风险沟通的方式,有效识别潜在危害源并降低风险认知的差异和偏见,帮助作出合理决策[5-6]。
2.3.2 正确使用风险评估工具
目前常用的风险评估工具包括:失效模式与影响分析(failuremode and effects analysis,FMEA)、危害分析和关键控制点(hazard analysis and critical control points,HACCP)、故障树分析(fault tree analysis,FTA)、危险与可操作性分析(hazard and operability study,HAZOP)、鱼骨图和决策树等[4]。不同类型的风险评估应使用相应的风险评估工具, 制药企业应建立风险评估工具如何运用的文件,以提高风险评估工具的运用能力[9,11]。
在进行风险分析和风险评价时,无论采用的是定性还是定量的方式,均需要制定明确的风险等级判定标准,明确风险分级。对于不同类型的风险评估,企业应建立更有针对性的风险等级判定标准,有助于风险评估小组降低偏见,得到比较客观公正的结果[12]。严重性是衡量危害导致的可能后果,一般从对法规符合性的影响、对产品质量和(或)可及性的影响、对使用者的影响3个维度进行考虑,需要明确说明对每种因素的影响程度;可能性是风险发生的概率,可使用现有或类似的历史数据(如投诉、调查、不符合项和趋势等)来评估可能性;对于某些工具,如FMEA,也需要考虑对危害的检出能力,即可检测性,主要是通过检测失效的及时性来判定。但需要明确的是,稳健的预防/ 设计控制始终优于检出控制,不要过度依赖事后控制(如100% 最终检查),因为预防/ 设计控制可从根本上解决失效模式的问题[9,12]。
2.3.3 最大限度运用相关数据和知识
知识管理是收集、分析、储存和传递关于产品、生产工艺及组分信息的系统性方法。最大限度地运用相关数据和知识可有效降低主观性。知识的来源包括但不限于已有的知识(公开或内部的文献)、药品研发资料、技术转移以及整个产品生命周期内的工艺验证研究、生产经验、创新、持续改进和变更管理等资料[5-6]。例如,从药品研发和生产经验中所获得的信息和知识能够为建立设计空间、质量标准和生产控制提供科学依据,设计空间是输入变量(如物料属性)和工艺参数的交互作用范围,依据先前的知识和初始的实验数据,利用风险评估工具确定可能会影响产品质量的参数(如物料、设备和工艺)并对其进行排序,而后通过进一步的实验研究对这些参数进行调整和优化[13]。降低风险评估的主观性,有助于减少生产过程中的质量缺陷并降低成本,以保证使用者的安全和产品持续稳定供应,还有助于开展更多以科学知识为基础的生产操作、控制策略和验证活动等。
2.4 基于风险的决策
基于风险的决策是指通过知识解决不确定性,促进监管机构和制药企业作出明智的决策,包括识别危害源、控制措施、风险控制后残余风险的可接受性、质量风险管理活动以及输出的沟通和回顾[5-6]。
基于风险的决策也需要考虑风险的重要性、不确定性和复杂性。当决策非常重要,不确定性和(或)复杂性水平较高时,基于风险的决策应考虑更多的因素,进行较正式的风险评估;当决策非常重要,但不确定性和(或)复杂性较低时,基于风险的决策可进行非正式的风险评估,即主要利用现有知识,或采用基于规则或标准化的方法进行风险评估。
2.5 改善质量风险管理在产品供应和可及性方面管理的不足
基于全球药品供应链的复杂性和涉及范围的广泛性,ICH《 Q9(R1):质量风险管理》中新增了“产品可及性风险”这一主题并明确提出,应用质量风险管理可主动识别并实施预防措施以促进产品的可及性,保证供应链的稳定性及产品质量的合规性;同时可有效解决制药企业质量体系如何使用质量风险管理和知识管理对潜在短缺进行早期预警的问题[5-6]。
质量/ 生产问题,包括不符合GMP 等,是影响产品可及性的主要原因。同时,越来越复杂的供应链之间的相互依存关系也会导致系统的质量/ 生产风险,影响供应链的稳健性。应用质量风险管理有助于企业尽早识别风险并及时实施预防措施,以提高产品的可及性[5-6,14]。有效的药品质量风险管理体系既可以提高供应链稳健性,又可以持续保障GMP合规。相关体系的建立健全需要企业管理层的大力支持并确保提供足够的资源,通过质量风险管理和知识管理建立并不断完善早期预警系统,确保其能对企业内部及企业与供应商之间不断发展变化的质量/ 生产风险进行有效监督和响应[14]。在产品整个生命周期中,早期预警系统会主动识别影响产品可及性相关的危害源,并触发风险回顾活动,如对供应商进行持续监控;同时还会监控各种信号,包括供应商流程控制问题、投诉、质量缺陷、批量报废、超出质量标准、设施设备的老化及维护不充分、关键偏差等其他质量问题[14]。
3. 新版ICH《 Q9(R1):质量风险管理》在制药企业中的应用
质量风险管理是贯穿于产品的整个生命周期,可采用前瞻或回顾的方式,对质量风险进行评估、控制、沟通、审核的系统过程。与ICH《 Q9:质量风险管理》(2005年版)相比,新版ICH《 Q9(R1):质量风险管理》在制药企业中的应用大体上仍保持一致,主要的变化是新增了质量风险管理在供应链中的应用,即从生产工艺、厂房设施和设备、外包活动及供应商监督3 个方面识别危害源,通过前瞻式风险评估进行预判,并采取相应的控制措施,确保产品持续稳定供应。
企业应依据新版ICH《 Q9(R1):质量风险管理》,结合企业实际情况开展日常风险评估工作。本文以危害源识别与FMEA工具结合起来开展风险评估进行举例[12] :第一步进行危害源识别,识别产品质量危害源的一种方法是考虑其对关键质量属性的影响,以无菌性为例,具体见表1 ;第二步使用FMEA 工具进行风险评估,以生产有关的失效模式为例,具体风险评估过程见表2。

4. 思考
新版ICH《 Q9(R1):质量风险管理》的修订旨在通过建立更客观的风险评估体系,改进质量风险管理,优化监管部门和企业的资源配置,建立更有效的以科学为基础的控制策略,进而改善生产的持续一致性,降低费用成本,以及减少质量缺陷、召回和药品短缺等问题的发生风险[5]。基于此,建议制药企业从以下3个方面进行改进。
4.1 提高风险管理意识
企业管理层人员应重视并准确掌握药品质量相关法律法规,建立完善的风险管理文化并提供相应的资源,制定相关规章制度,加强人员培训,提高风险管理的预防性、持续性和科学性[8,15-16]。正确运用ICH《 Q9(R1):质量风险管理》的方法,主动且有前瞻性地开展质量风险管理,企业应该基于在研发阶段获得的知识和经验加强对产品工艺的理解,确定关键物料、关键工艺参数和关键质量属性的要求,并与项目立项、项目可行性研究和项目风险评估等进行有效衔接,进而制定相应的控制策略[16]。持续开展确认与验证工作,确保生产工艺和设施设备持续、稳定,使质量风险管理覆盖药品全生命周期,包括药品研发、技术转移、商业化生产和产品终止等阶段,实现质量风险管理评估、控制、沟通和审核的系统管理[13,17]。
4.2 加强企业的硬件管理
一方面,药品生产企业要加强硬件建设的投入,使厂房的安全系数更高、设施设备更加先进[15] ;另一方面,设施设备运行的稳定性是保障产品质量的重要条件,药品生产企业需要基于质量风险管理,从设计、分类、校准、维护保养、回顾等方面进行全生命周期管理,加强预防性管理力度,以便及时发现不良趋势并进行改进。
4.3 供应商的管理
质量风险管理和供应商现场审计的有效结合能为制药企业管理供应商提供很好的工具和评价方式。制药企业可依据对供应商厂家及产品风险、场地风险、工艺风险、合规风险等的掌握,将供应商划分为不同的风险等级,进而针对不同风险等级的供应商采取相应的审计措施,明确现场审计重点,有利于把有限的资源针对性地运用到供应商审计工作中,进一步确保质量管理有效和供应链安全[18-19]。
引用本文
吴菲,胡菁,高易娥,孙营,胡俊,李茜*.新版ICH《 Q9(R1): 质量风险管理》解析[J].中国食品药品监管.2025.2(253):62-79.

来源:中国食品药品监管杂志
关键词: 药品质量风险管理