嘉峪检测网 2025-04-01 08:54
导读:本文主要从原位成型植入物的分类、处方考量和开发要点出发进行总结概述。
1、概述
由于一些药物的口服生物利用度较低,为避免药物首过效应,同时解决频繁注射的潜在副作用,长效药物缓释递送系统得到迅速发展。可注射原位成型植入物(Injectable in-situ forming implants(ISFIs))作为其中之一,具有稳定的血药浓度、缓释数周乃至数月以及提高患者依从性等优势。本文主要从原位成型植入物的分类、处方考量和开发要点出发进行总结概述。
ISFI系统主要由可生物降解的聚合物组成,以液体形式注射给药,在注射后形成固体或半固体储库,根据固化机制的不同,又可分为以下几类:原位交联体系、原位固化有机凝胶体系和原位相分离体系。
1.1 原位交联系统
由于温度变化(热响应交联)、光子吸收(光响应交联)、阴离子聚合物与小阳离子之间的离子相互作用(离子响应交联)或酶的存在(酶响应交联)而形成聚合物交联,多用于递送不稳定的药物如蛋白质或多肽类。
1.2 原位固化有机凝胶系统
由不溶于水的两亲性脂质组成,这些脂质被加热并溶解在诸如乙醇的有机溶剂中,脂质在水中膨胀产生多种溶性晶体。形成的溶致晶体的特性取决于多种因素,包括所载药物的性质、脂质结构特征、水的体积和温度。该系统常用的两亲性脂质主要是甘油脂肪酸酯,如单油酸甘油酯(GMO)、单亚油酸甘油酯等。Camurus利用FluidCrystal技术开发了Brixadi/Buvidal,是一款可每周和每月用药的丁丙诺啡长效制剂,通过大豆磷脂胆碱和二油酸甘油酯包裹丁丙诺啡,注射后脂质基液体会转变为结晶凝胶,并通过缓慢降解释放丁丙诺啡。
1.3 原位相分离系统
1.3.1 pH响应系统
此类系统由环境pH变化引起的溶胶到凝胶的转变,通常由含有酸性或碱性基团的聚合物组成,其可以根据环境pH值接受或提供质子。聚丙烯酸(PAA)及其衍生物都是pH敏感聚合物。
1.3.2温度响应系统
温度敏感型原位凝胶是一类对温度变化敏感的原位凝胶,即环境温度低于最低临界相变温度时呈现液体状态,进入给药部位后由于温度升高导致高分子聚合物发生相转变,常用的凝胶基质包括泊洛沙姆、壳聚糖、聚N-异丙基丙烯酰胺。
1.3.3 光响应系统
光响应聚合物含有至少一个水溶性和可生物降解的区域和至少两个自由基可聚合的区域。水溶性区域由聚乙二醇(PEG)、聚乙烯醇、PEO-PPO共聚物、多糖组成。可生物降解区域由聚乳酸(PLA)、聚乙醇酸、聚氨基酸和聚内酯组成的聚合物。自由基可聚合区域包括丙烯酸酯、二丙烯酸酯或其他生物上可接受的光聚合基团。
1.3.4 溶剂交换系统
制剂在注射后,溶剂随体液流走,可生物降解的聚合物沉淀固化在原位包裹药物缓慢释放。基质主要采用可生物降解的聚合物包括聚乳酸、聚乳酸羟基乙酸共聚物、聚己内酯等。采用PLA或PLGA作为高分子聚合物,以NMP作为生物相容性有机溶剂的Atrigel系统上市药物主要有盐酸多西环素(Atridox®)、醋酸亮丙瑞林(Eligard®)、丁丙诺啡(Sublocade®)和利培酮(Perseris®)。采用乙酸异丁酸蔗糖酯实现缓释并以苯甲醇作为溶剂为长效布比卡因制剂(Posimir®)。
2、基于溶剂交换相分离系统的处方考量
基于溶剂交换相分离系统处方通常由可生物降解的聚合物(常用的PLA/PLGA)、与水混溶的有机溶剂(常用的为NMP/DMSO)以及活性成分组成。该系统的形成、溶剂交换、药物释放的示意图见如图1,下文主要对处方中各组分影响药物释放的因素进行介绍。
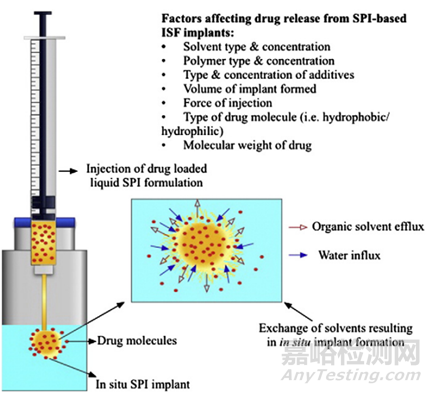
图1 植入物形成、溶剂交换、药物递送示意图[3]
2.1溶剂
用于该递送系统的的溶剂的性质需具备水和体液的混溶性、聚合物的良好溶解度、生物和化学相容性、无毒和无刺激性。溶剂的代谢产物不应有任何有害作用。溶剂粘度应适中且不应在注射时引起疼痛,例如高粘性的溶剂与约30%聚合物和药物制备的制剂会给注射带来困难。用于溶解聚合物的溶剂分为两类:高水溶性溶剂和低水溶性溶剂。
2.1.1高水溶性溶剂
常用的高水溶性溶剂通常包括N-甲基吡咯烷酮、二甲基亚砜、2-吡咯烷酮和低分子量PEG等。上述溶剂表现出快速的相反转,导致形成高度多孔的原位系统。此外高水溶性的溶剂黏度较低,制备的体系易于注射给药,其通过提供亲水性环境也可增强生物相容性。
2.1.2 低水溶性溶剂
低水溶性溶剂最大限度地降低聚合物溶液与水之间的亲和力,从而降低液-液相分离速率,表现为缓慢的形成相反转,这些溶剂包括苯甲酸乙酯、乙酸乙酯、三乙酸甘油酯、柠檬酸三乙酯和苯甲醇等,形成的原位系统孔隙较少,与高水溶性溶剂形成的体系相比突释降低,如三乙酸甘油酯水溶性有限仅为7%,以其作为溶剂制备制剂后其不仅会降低体系的初始释放甚至降低整体释放速率,同时溶剂的疏水性也使得原位系统的可注射性降低。将上述两种溶剂混合可能是实现合理粘度、适当的相转化和低突释的较好选择之一。
2.2聚合物
可降解聚合物包括PLGA/PLA是调控原位体系释放的关键组分,影响药物释放主要包括以下几点(1)PLGA链内丙交酯和乙交酯的比例和分布:其是调节系统疏水性和结晶度并影响溶剂-水交换速率和降解的基本参数,乙交酯比例的增加可以提高水解速率,从而加快药物释放。(2)分子量:PLGA聚合物的分子量是影响药物释放的另一个参数。它可以影响系统的物理化学和机械特性,如粘度、玻璃化转变温度、溶解度和扩散系数,通常分子量较高的PLGA降解速率和释放动力学较慢,但也有文献研究显示低分子量的PLGA具有更低的突释,主要归结于具有较低分子量PLGA制备的制剂在水中的溶解度增加,因此需要更多的时间来实现相转化并释放药物。(3)处方中聚合物的浓度:聚合物浓度的增加会导致植入物相转化速率变慢,从而导致药物释放速率的降低,植入物的孔隙形态从手指状的多孔结构转变为海绵状的致密结构,与增加聚合物分子量类似,增加聚合物浓度也会产生一系列影响,如改变粘度,性能,降低扩散系数,增加体系疏水性等。(4)PLGA端基:使用酯封端的 PLGA聚合物可以减慢药物的释放速率并延长药物的释放期,而酸封端的 PLGA则促进了更快的药物释放,酸封端聚合物还会催化酯键降解,同时还可能会与药物间发生相互作用。
2.3 药物
药物在体系中的溶解度、载药量和稳定性也是影响释放的重要因素,药物可以以溶解或分散的状态存在于原位系统中,形成均相或不均相溶液。高载药量的注射制剂的优点是施用的固定剂量时可以减少制剂注射体积,但药物不同载药量高低对释放的影响也不同,无特定规律。此外应关注某些药物与聚合物之间的化学相互作用,例如阿司匹林其高亲水性有助于与聚合物链形成氢键进而促进聚合物降解,综上该系统不适合于易被水解的药物,也不适合于聚合物降解后对酸性环境高度敏感的药物。
在此前一个小分子药物制备成原位凝胶制剂研发过程中,在筛选活性物质不同盐型制备制剂以调节释放过程中发现,选用较强的有机酸与其成盐后制备制剂,制剂的分子量会随着时间的放置显著下降,导致释放变快,在选择药物时应注意此点。此外当药物以完全溶解的形式存在于制剂中,即整个体系为均相溶液状态,制剂初始突释及后期的释放均会高于混悬体系。
2.4 添加剂
添加剂可分为亲水性、疏水性和两亲性三种。使用亲水性添加剂如甘露醇和聚乙烯吡咯烷酮,有助于增强液液分离,并产生高突释制剂。疏水添加剂的加入可以降低药物突释,这些添加剂包括硬脂酸、单硬脂酸甘油、庚酸甲酯、庚酸乙酯和壬酸乙酯,这些添加剂可以产生更少的多孔海绵状基质,减少药物的初始突释并使后期释放减慢。使用两亲性添加剂,如Pluronic可以减少药物的突释,从而实现微小的形态变化。Pluronic浓度和链长的选择有助于实现亲水-亲脂平衡,这种平衡表现在亲水性PEO末端的高吸水性和亲脂性PPO链的扩散屏障之间,亲脂性PPO链嵌入到聚合物基质中,减少药物吸附,增强系统生物相容性。
3、原位成型植入物优劣势
原位成型植入物具有良好的缓控释效果,可提高患者顺应性,具有可注射性及良好的生物相容性,提供稳定的血药浓度,并可以通过液体给药实现精准定量,制备工艺及设备简单易于放大。但同时该系统也存在一定的局限性,以下是处方开发中需考量的几点:(1)原位成型系统在注射后存在形状、比表面积不一致导致的药物释放行为差异较大,例如快速注射形成棒状,缓慢注射则为球形,然而不规则的形状也使得这些系统适合于组织工程;(2)注射后的初始突释,其通常可通过处方调控得以解决和控制;(3)由于药物制剂与组织反应是复杂的,故原位成型植入物释放评价时体内外相关性较差。开发时尽量建立体内外相关模型,若不能也应建立具有区分度的体外释放质控方法;(4)原位成型植入物系统需使用大量有机溶剂,开发时应关注有机溶剂的安全性和刺激性,许多药物在有机溶剂中不稳定,此类问题在开发时可通过改变包装方式,通过两支注射器,临用前连接推注混合的方式解决(例如Eligard-一支装有聚合物溶液的注射器+一支活性药物粉末的注射器;Okedi-一支装有有机溶剂的注射器+一支装有活性药物粉末和聚合物粉末的注射器),此外还应关注包装系统密封性问题;(5)部分制剂粘度较大在注射过程中易引起疼痛,导致注射部位坏死或瘢痕结节生成,在开发过程中应关注注射剂黏度,保证通针性并考虑注射器残留问题;由于制剂黏度过大无法过滤除菌还应根据制剂的具体情况选择合适的灭菌方式,比如辐照灭菌等;(6)原位成型植入物在降解过程中会导致pH下降,在开发如蛋白质、多肽和对酸性pH敏感的药物应该此类问题。有研究表明在降解或释放研究过程中,使用聚己内酯等聚合物不会导致酸性环境的产生。通过使用各种新技术和新策略,原位成型植入物一定会有越来越多的药物上市。
参考文献:
[1] P.D.D. Graham, K.J.J. Brodbeck, A.J.J. McHugh, Phase inversion dynamics of PLGA solutions related to drug delivery, J. Control. Release 58 (1999) 233–245.
[2]田虹,樊瑜波.聚丙交酯-乙交酯降解研究进展[J].现代生物医学进展, 2011, 11(1):3.DOI:CNKI:SUN:SWCX.0.2011-01-049.
[3]Thakur RR, McMillan HL, Jones DS. Solvent induced phase inversion-based in situ forming controlled release drug delivery implants. J Control Release. 2014 Feb 28;176:8-23. doi: 10.1016/j.jconrel.2013.12.020. Epub 2013 Dec 27. PMID: 24374003.
[4] J.R. DesNoyer, A.J. McHugh, Role of crystallization in the phase inversion dynamics and protein release kinetics of injectable drug delivery systems, J. Control. Release 70 (2001) 285–294

来源:药事纵横
关键词: 注射剂