嘉峪检测网 2025-04-28 08:43
导读:如何建立可区分关键影响因素的IVRT和IVPT方法是仿制药申办方最为关注的问题,本文将汇总阿昔洛韦乳膏的相关研究,为研究人员开发外用制剂IVRT和IVPT方法提供研发思路;
阿昔洛韦是一种合成嘌呤核苷类似物,可高度选择抑制I型及II型单型疱疹病毒和水痘状疱疹病毒编码的胸苷激酶活性,并在胸苷激酶作用下转化为单磷酸阿昔洛韦,进一步转化的三磷酸阿昔洛韦可以抑制疱疹病毒DNA复制;阿昔洛韦乳膏主要用于治疗成年人和12岁以上青少年复发性唇疱疹治疗;由于单型疱疹病毒的感染和复制发生在表皮基底细胞层,阿昔洛韦乳膏的疗效取决于药物皮肤渗透和表皮药物滞留,且相关研究显示阿昔洛韦乳膏5%体内暴露量低[1],因此FDA发布的《阿昔洛韦乳膏生物等效性指导意见草案》[2]有两种方法可选择证明仿制药和参比制剂生物等效性:(1)两项体外生物等效性研究(即IVRT和IVPT)和其他鉴定试验;(2)体内临床终点生物等效性研究。但复发性唇疱疹发病迅速,病毒脱落期短,且能迅速自愈[3],使得体内临床终点研究难度大;绝大多数仿制药申办方选择通过体外IVRT和IVPT等相关研究证明与参比制剂生物等效性,然而在制剂处方和工艺中存在多种因素影响药物的释放和透皮,如何建立可区分关键影响因素的IVRT和IVPT方法是仿制药申办方最为关注的问题,本文将汇总阿昔洛韦乳膏的相关研究,为研究人员开发外用制剂IVRT和IVPT方法提供研发思路;
影响阿昔洛韦乳膏药物释放和透皮的关键因素
阿昔洛韦乳膏为水包油型乳膏,辅料组成有鲸蜡硬脂醇、白凡士林、矿物油、泊洛沙姆、十二烷基硫酸钠、丙二醇、水;处方分析如下表1所示:

阿昔洛韦在最终乳膏中可能以溶解态和混悬态,两种形式存在水相和油相中,阿昔洛韦pKa值为2.27和9.25,在水中的溶解性差且受pH值影响,阿昔洛韦在水相中的溶解量对药物的皮肤渗透有显著影响[4],溶解在水相中的药物存在两种平衡:1)溶解态和未溶解态平衡,2)油相和水相的分布平衡;而水相中溶解的药物受pH值的影响呈现阳离子、中性离子、阴离子的状态,不同离子状态皮肤渗透能力不同,如下图1所示:
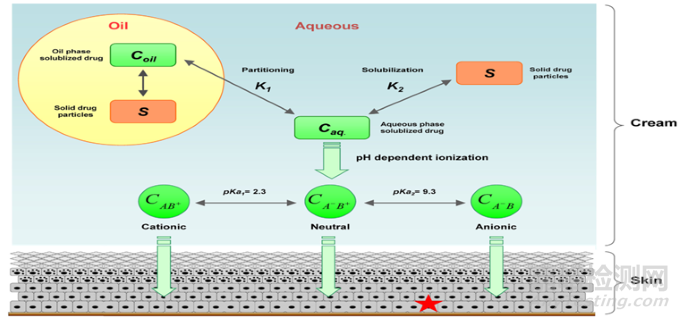
图1阿昔洛韦乳膏水相药物浓度对皮肤渗透影响
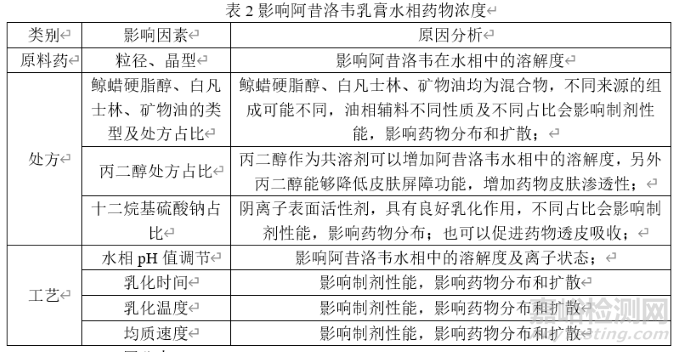
从原料药、处方、工艺三方面分析,影响阿昔洛韦乳膏水相药物浓度可能因素如下表2所示:
IVRT区分力
IVRT反应了药物从制剂中释放的重要信息,具有区分影响药物释放因素能力,可以用于评估制剂处方工艺变更的关键质量属性,但IVRT方法包括多种测定装置和测定条件,结果可能会受到设备、膜、接受介质、搅拌速度、取样点、上样量等选择的影响;
在Dalia S.M等人的研究[5]中IVRT可以区分鲸蜡硬脂醇、白凡士林辅料来源,不同来源鲸蜡硬脂醇熔点不同,阿昔洛韦释放速率随着熔点降低而升高;不同来源的白凡士林凝固点、滴点和运动粘度不同,阿昔洛韦释放速率90%置信区间不能满足75~133.3%要求;
在Yellela S.R.K等人的研究[4]中不同乳化时间(15、22.5、30min)、不同均质速度(2500、3750、5000rpm)、不同乳化温度(70、80、90℃)及水相pH值(5、6.75、8.5),阿昔洛韦释放速率90%置信区间均能满足75~133.3%要求;
在Nahid S.K等人的研究中[6]处方中丙二醇占比及原料药粒径对阿昔洛韦乳膏药物释放速率有显著影响,药物的释放速率随着丙二醇占比增加、原料药粒径减少而增加;
从上述研究可知IVRT可以区分原料药粒径、处方组成对阿昔洛韦乳膏药物释放的影响,工艺参数对阿昔洛韦乳膏药物释放的无显著影响,不同研究IVRT方法对比汇总入下表3所示:

不同研究中膜材及取样截止时间相同,设备、接收介质、搅拌速度及上样量不同,文献中并未说明IVRT方法验证内容,无法判定各个方法的优劣;IVRT是基于菲克第一定律认为药物的释放速率与时间的平方根呈正比,方法中膜材不应是限速因素,上样量不应影响药物的稳态释放动力学(一般情况下剂量消耗应低于30%),搅拌速率需确保介质能够充分混合,由此认为接受介质的选择对IVRT区分力有很大影响,研究者需根据制剂特性分析,筛选适宜的接受介质;
IVPT区分力
IVPT反应药物从制剂中释放在皮肤中渗透的信息,在一些情况下可以替代体内临床试验评估仿制药和参比制剂相对生物利用度。IVPT方法几乎与IVRT一致,除了膜使用皮肤、上样量通常在2-15mg/cm2范围内,不是伪无限上样量、接受介质药物浓度远低于IVRT,故IVPT试验结果的变异性较高。
在Yellela S.R.K等人的研究[4]中对与参比制剂Q1、Q2、结构特性(粘度、屈服应力、粒径、水相药物浓度)及IVRT相似,水相pH不同的三个制剂进行IVPT研究发现,pH较低的两个制剂24h药物渗透量比参比制剂高,分析可能是由于阿昔洛韦极性随着pH增加而增加,而非极性小分子比极性分子皮肤渗透性好。
在L.Trottet等人的研究中[7]对丙二醇占比不同的制剂进行IVPT研究发现40%丙二醇占比制剂24h经皮通量是15%丙二醇占比制剂3~5倍。丙二醇可以增加药物水相浓度,也可以增加药物皮肤渗透性,有相关研究表明处方中丙二醇占比在30~40%之间药物皮肤渗透性最强。
在Nahid S.K等人的研究中[6]中水相pH值对阿昔洛韦皮肤渗透和皮肤内滞留影响小,丙二醇和十二烷基硫酸钠含量对阿昔洛韦皮肤滞留有显著影响,主要因为乳膏涂抹在皮肤表面后,丙二醇和十二烷基硫酸钠的亲水性羟基和羧基结合水分子氢键给皮肤补充水分,这些水与细胞内角质蛋白结合,迅速增加皮肤渗透性,另外丙二醇可以溶剂化a-角蛋白并占据氢键位点促进药物扩散。
上述研究中丙二醇增强药物皮肤渗透性结论相同,水相pH值对皮肤渗透性结论不同,不同研究IVPT方法对比汇总入下表4所示:

不同研究中的IVPT方法差异较大,Yellela S.R.K等人的研究和Nahid S.K等人的研究在水相pH对药物皮肤渗透性影响方面得出不同结论,可能是由于IVPT区分分力不同导致的,Nahid S.K等人的研究中取样时间短,接受介质阿昔洛韦检测值较低,IVPT区分力可能相对较差,对比两项研究IVPT方法,分析IVPT区分力可能受皮肤处理、上样量、取样时间、接收介质的影响,影响因素较多。
讨论
通过对阿昔洛乳膏IVRT、IVPT研究文献总结可知,IVRT和IVPT对影响阿昔洛韦乳膏药物释放和透皮的关键因素有较好的区分力,可以帮助研究员筛选制剂处方工艺;IVRT的区分力根据相关技术要求分析,容易受到接受介质的影响,研究者需根据制剂特性分析,选择适宜的接受介质;IVPT研究结果由于皮肤的多样性和接受介质中药物浓度低等原因,变异性较大,其区分力的影响因素较多,需要参比制剂(阳性对照)或与参比制剂不同的制剂(阴性对照)进行验证,并应用统计学知识对结果进行分析,排除无关的影响因素,建立适宜的IVPT方法。
[参考文献]
[1] FDA. Zovirax® Clinical Pharmacology and Biopharmaceutics Review(s). [EB/OL]. https://www.accessdata.fda.gov/drugsatfda_docs/nda/2002/21-478_Zovirax_biopharmr.pdf
[2] FDA. Draft Guidance On Acyclovir (Cream) . [EB/OL]. https://www.accessdata.fda.gov/drugsatfda_docs/psg/PSG_021478.pdf
[3] Johan. H, Bo ÖBERG, Spotswood. S. Prevention of UIcerative Lesion by Episodic Treatment of Recurrent Herpes Labialis: A literature Review. [J]. Acta Derm Venereol 2010, 90: 122-130
[4] Yellela S.R.K, Xiaoming Xu, Ziyaur. R, et al. Development of performance matrix for generic product equivalence of acyclovir topical creams. [J]. International Journal of Pharmaceutics 475 (2014) 110-122
[5] Dalia. S. M, Flavian. S. R, Victor A.V, et al. Rheological and in vitro release measurements of manufactured acyclovir 5% creams: confirming sensitivity of the in vitro release. [J]. PHARMACEUTICAL DEVELOPMENT AND TECHNOLOGY 2021, 26(7): 779-787
[6] Nahid S. K, Yellela S.R.K, Xiaoming Xu, et al. Identificaltion of critical formulation parameters affecting the in vitro release, permeation, and rheological properties of the acyclovir topical cream. [J]. International Journal of Pharmaceutics (2020)
[7] L. Trottet, H. Owen, P. Holme, et al. Are all acyclovir cream formulations bioequivalent ? .[J]. International Journal of Pharmaceutics 304(2005): 63-71

来源:药事纵横