今日头条
江苏威凯尔P2Y12R拮抗剂美国报产。江苏威凯尔医药宣布已向FDA递交其维卡格雷胶囊用于治疗冠心病ACS、缺血性脑卒中以及确诊外周动脉性疾病等血栓性心脑血管疾病的新药上市申请(NDA)。维卡格雷是新一代口服P2Y12R拮抗剂,其在体内代谢生成的活性代谢物可有效抑制血小板的活化聚集,同时有望解决“氯吡格雷抵抗”问题。这也是江苏威凯尔创新药管线中的首个新药上市申请。
国内药讯
1.罗氏眼科双抗中国获批新适应症。罗氏眼科VEGF-A/ANG-2双抗法瑞西单抗(罗视佳®,Vabysmo®)获国家药监局批准新适应症,用于治疗新生血管性年龄相关性黄斑变性。Ⅲ期临床(TENAYA和LUCERNE)两年治疗数据显示,在达到与以每2个月接受活性对照治疗患者相似视力改善的前提下,有超过60%的Vabysmo组患者可以每隔4个月的间隔接受治疗。此前,该新药已在中国获批用于治疗糖尿病黄斑水肿。
2.珠海贝海改良型多西他赛美国报产。贝海生物多西他赛改良型抗肿瘤新药BH009的上市申请获得FDA受理。BH009不含吐温80,可消除与吐温80相关的严重毒副作用如超敏反应、体液潴留、肾毒性和神经毒性等,临床给药时不需要给予预防性使用糖皮质激素地塞米松,临床安全性及用药依从性更优。BH009已在治疗晚期三阴性乳腺癌的Ⅱ期临床达到主要终点,患者接受BH009治疗后,过敏反应发生率为0%。
3.AZ/第一三共HER2-ADC拟纳入突破性品种。阿斯利康与第一三共开发的HER2靶向ADC德曲妥珠单抗(DS-8201a,Enhertu)获CDE拟纳入突破性治疗品种,拟定适应症为:存在激活HER2(ERBB2)突变且既往接受过至少一种系统治疗的不可切除或转移性非小细胞肺癌成人患者。在DESTINY-Lung02研究中,Enhertu达到58%的确认客观缓解率,中位缓解持续时间为8.7个月。
4.本导基因创新地贫疗法获批临床。本导基因1类生物制品“BD211自体CD34+造血干细胞注射液”获国家药监局临床许可,拟开发用于治疗输血依赖型β-地中海贫血。BD211通过一系列优化技术,高效表达β珠蛋白,对β0/β0、β0/β+等多种基因型地贫有效。研究者发起的临床研究(IIT)显示,两例β0/β0地贫患者均摆脱了输血依赖,随访时间超过两年,初步验证了BD211的有效性和安全性。
5.普利抗肿瘤纳米新药美国获批临床。普利制药纳米创新药注射用PLAT001获FDA临床许可,拟开发用于治疗胰腺癌等晚期或转移性实体瘤患者。这是一款聚合物偶联小分子药物,已在临床前药效试验中的胰腺癌、肝癌等动物模型上显示出显著的肿瘤抑制作用,有望为晚期或转移性实体瘤患者的治疗提供新的选择。目前,我国尚无本土原创纳米药物获批上市。
6.BI与瑞博合作开发治疗NASH的RNAi疗法。苏州瑞博生物及瑞博国际研发中心与勃林格殷格翰达成研发合作,将利用瑞博的RIBO-GalSTAR技术平台合作开发治疗非酒精性脂肪性肝炎(NASH)或代谢功能障碍相关脂肪性肝炎(MASH)的RNAi疗法。根据协议,瑞博将获得预付款,临床研究、药物注册和商业化里程碑后期付款,以及产品的销售分成,总金额超过20亿美元。
国际药讯
1.FIC丙酮酸激酶激活剂地贫Ⅲ期临床成功。Agios公司“first-in-class”口服丙酮酸激酶激活剂mitapivat治疗成年非输血依赖性(NTD)α或β地中海贫血患者的Ⅲ期临床ENERGIZE达到主要终点和关键性次要终点。与安慰剂相比,Mitapivat治疗第24周与基线相比平均血红蛋白水平增加≥1g/dL的患者比例显著更高(42.3%vs1.6%,双侧p<0.0001);两组不良事件发生率相当。预计2024年底递交其用于治疗地中海贫血的监管申请。
2.靶向药物递送器械AD临床见刊NEJM。Insightec公司开发的能够安全、暂时地打开血脑屏障的聚焦超声系统,联合抗β淀粉样蛋白抗体治疗阿尔茨海默病(AD)的首次人体研究成果发表于《新英格兰医学杂志》上。带有1,000多个超声换能器的FUS MRI引导治疗头盔被引导到具有高淀粉样蛋白-β斑块的特定大脑区域,并经过六个月的抗体治疗。结果显示,与没有血脑屏障开放的区域相比,血脑屏障开放的大脑区域的淀粉样蛋白-β斑块平均减少32%。
3.罗氏超10亿美元开发RNA靶向小分子药物。罗氏与Remix公司将利用后者专有REMaster药物发现平台,联合开发调节RNA序列以控制基因表达的小分子候选疗法。根据协议,Remix将获得3000万美元的预付款和1200万美元的近期里程碑付款,以及临床前、临床、商业和销售里程碑后期款项,总交易金额可能超过10亿美元。Remix将与罗氏一起进行发现和临床前活动,罗氏将负责产品的开发和商业化。
4.Galapagos公司超7亿美元开发小分子药物。Galapagos公司与BridGene公司将利用后者专有化学蛋白质组学平台IMTAC™,针对Galapagos指定的肿瘤靶点,合作开发新型小分子候选药物。根据协议,BridGene将获得2700万美元的预付款和临床前研究里程碑付款,超过7亿美元的临床和商业里程碑潜在付款,以及产品净销售额的分层版税。Galapagos将拥有小分子候选药物的开发和商业化的独家权利。
5.基因编辑公司Tome拟1.85亿美元收购Replace公司。Tome Biosciences公司宣布收购Replace公司,并获得该公司新型程序化基因组整合(PGI)技术平台。Replace的技术将CRISPR/Cas9的位点特异性与DNA连接酶相结合,从而能够精确地编辑小DNA序列。Replace的这种小DNA编辑技术将补充Tome公司的大DNA整合技术。根据协议,Tome公司将支付6500万美元的预付款和近期里程碑付款,以及高达1.85亿美元的股票和现金。
6.CG Oncology公司申请纳斯达克IPO。CG Oncology公司宣布递交了纳斯达克IPO申请并获得受理。CG Oncology的核心管线CG0070是一款临床后期的溶瘤病毒疗法,已在去年12月获得FDA同时授予突破性疗法认证和快速通道资格,用于治疗高危、卡介苗治疗不响应非肌肉侵袭性膀胱癌(NMIBC)。在Ⅲ期试验中,CG0070单药治疗的完全缓解率为75.7%。乐普生物拥有CG0070的大中华区权益。
医药热点
1.新版医保目录1月1日起执行。2024年1月1日,新版医保目录正式落地实施。新版医保目录新增126种,调出一种,目录内药品总数增至3088种,其中西药1698种、中成药1390种;中药饮片仍为892种。本次调整,慢性病、罕见病、儿童用药等领域的保障水平得到进一步提升。叠加谈判降价和医保报销因素,预计未来两年将为患者减负超400亿元。
2.张金保任首都儿科研究所党委书记。2023年12月29日,首都儿科研究所召开中层干部大会。会上,市委组织部行政干部处处长代金鹏同志宣布了市委任命决定,张金保同志任中共首都儿科研究所委员会委员、党委书记(副局长级),免去刘中勋同志中共首都儿科研究所委员会书记、委员职务,调首都医科大学附属北京中医医院工作。张金保同志表示,将尽快进入角色,依靠班子,带领全所干部职工谋事、创业,攻坚克难,推进首儿所高质量发展。
3.GSK前高管入职Biotech。腾盛博药宣布,Brian Alvin Johns自2024年1月3日起担任首席科学官,他将全面负责新药开发项目,并制定公司的未来管线策略和优先事项。Brian Alvin Johns拥有化学博士学位,在创新药物的发现和早期开发项目方面拥有丰富的经验。此前,Brian Alvin Johns曾在HemoShear Therapeutics担任首席科学官,以及曾在ViiV Healthcare和葛兰素史克担任新药开发副总裁。
评审动态
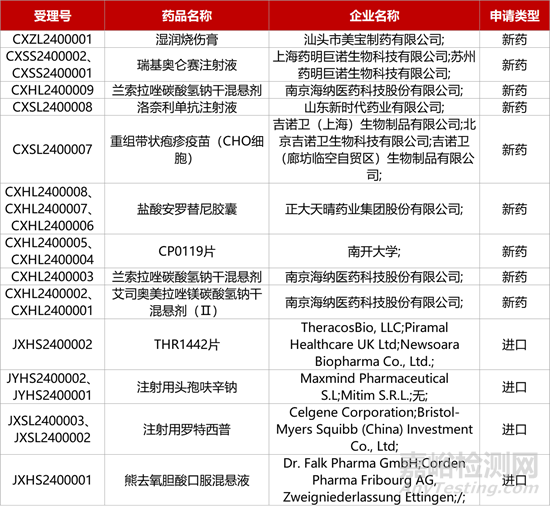
1. CDE新药受理情况(01月04日)
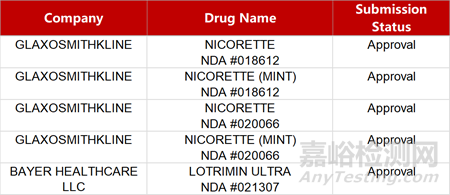
2. FDA新药获批情况(北美01月03日)
来源:药研发
关键词:
药物研发
医药研发
药品研发