嘉峪检测网 2024-08-29 17:51
导读:本文介绍电子舌的发展情况及其在药品口感评价中的应用进展,并提出相关建议。
摘要
药品口感会显著影响其临床应用效果。传统的药品口感评价方法包括人口尝试验、动物偏好试验和体外分析方法(如体外溶出试验)等。本文介绍一种新型药品口感评价工具——电子舌。电子舌运用体外仿生学技术,以样品整体味觉信息输出药品口感情况,具有较好的客观性,检测速度也快,可避免人口尝试验中的潜在安全风险和主观因素影响。本文介绍电子舌的发展情况及其在药品口感评价中的应用进展,并提出相关建议。
关键词
药品口感 / 电子舌 / 味觉
药品口感会显著影响药品的临床应用效果,不良的口感可能对患者的服药依从性产生影响,导致难以达到或维持预期的治疗效果,并可能使得体内的药物暴露量不稳定,由此带来安全隐患[1-2]。特别是对于吞咽前状态(包括经溶剂或唾液分散溶解后的状态)为真溶液或混悬液的制剂,服用时因会与口腔味蕾充分接触,药品的口感对患者服药依从性的影响更加明显。
传统的药品口感评价方法包括体内方法,如人口尝试验、动物偏好试验、临床试验中服药依从性和觅药行为评价,以及体外方法,如基于分析方法的味道定量评价、体外溶出试验等[3]。目前,人口尝试验仍是药品口感评价所使用的主要方法,具体还可分为排序评分法、模糊数学综合评价法、视觉模拟评分法等,但其因会受到评价者个体差异和主观因素的影响,评价结果具有较大的变异性和不确定性。因此,开发和应用能客观、高效、完全模拟人舌味觉受体的体外味觉评价方法显得十分重要。电子舌是一种新型仿生味觉分析测定系统,可客观、快速地提供药品口感评价所需要的信息,在药品口感评价方面的应用越来越广泛。
1、 舌头、味觉和药品口感评价方法
舌头是一种柔软、灵活和敏感的肌肉器官,其感受味道的主要部分为味蕾(味觉感受器)和离子通道。味蕾呈卵圆形,由味觉细胞和支柱细胞组成,细胞基部有神经纤维,顶端有一小孔,即味孔,开口于上皮表面。当味觉刺激物进入味孔时,味觉细胞受到刺激而兴奋,将刺激的化学能转化为神经能,然后沿舌咽神经传至大脑中央的味觉神经中枢,产生味觉。人味蕾的数量随年龄增大而减少,味阈值逐渐增高,味觉敏感度随之下降。
哺乳动物和人的舌头能够感知的5种基本味觉分别是甜、苦、酸、咸和鲜味。不同味觉的产生机制并不完全相同,其中甜、苦和鲜味的识别通常被归因于味觉受体细胞,而酸和咸味的识别则被归因于味觉受体细胞上的特定膜通道(图1)。
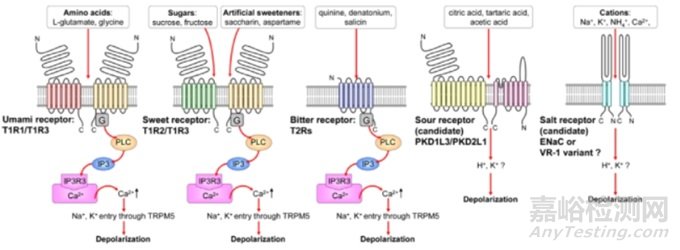
图1 5种基本味觉的味觉受体和信号转导途径[4]
药品口感评价方法包括人口尝试验、动物偏好试验和体外评价方法等。其中,人口尝试验可快速而直观地反映受试者对药品在口腔内的真实感受,但受试者有潜在安全性风险,且人口尝的主观性强、重复性较差,评价结果不易量化。动物偏好试验能避免人口尝存在的潜在安全性问题,但试验结果仍需通过人口尝进行验证,且试验还有周期长、成本高、操作流程复杂等缺点。体外评价方法如溶出试验等可对口服药品中的特定组分进行定量分析,但味道是很多化学成分相互作用的综合表现,单成分的分析无法表征药品口感。
2、 电子舌的发展历史与工作原理
1985年,日本九州大学的Kiyoshi Toko课题组首次使用传感器阵列检测样品味道。1995年,俄罗斯圣彼得堡大学的Andrey Legin研究团队构建了一种由非特异性传感器阵列组成的新型味觉检测系统,并参考电子鼻的名称第一次正式提出了“电子舌”这个名称。2005年,国际纯粹与应用化学联合会在其技术报告中作出定义:电子舌是一种低选择性、非特异性的交互敏感传感器阵列,配以合适的模式识别方式和多元统计方法,进行定性定量分析的现代化味觉检测仪器。简而言之,电子舌是一种模拟生物味觉工作机制对复杂液体中多种物质进行有效测量和表征的新型味觉检测系统[5]。
电子舌一般由味觉传感器、信号处理系统和模式识别系统3大部分组成。电子舌利用味觉传感器阵列采集不同物质的特征性响应信号(类似于人味觉细胞受呈味物质刺激产生化学信号),经信号处理系统转换成电信号(类似于人体内化学信号转换为神经能并传递至大脑味觉皮质),再通过模式识别系统利用计算机对样品信息进行识别、分析和处理(类似于人大脑味觉皮质对神经转导的信号进行综合处理),最后以样品整体味觉信息输出(图2)。
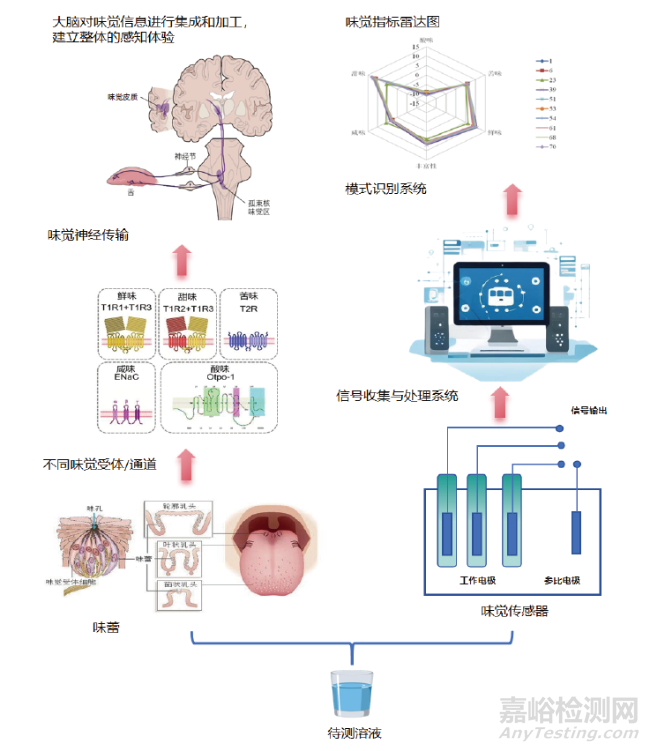
图2 人味觉系统与电子舌工作机制对照图
与传统的类似于“锁与钥匙”的特异性分析方法不同,电子舌基于具有所谓交叉选择性的非特异性受体而不是特定受体对特定分析物的高亲和力,由来自多个传感单元的响应模式组成的复杂响应会产生给定样品的唯一“指纹”,这是其能够识别味觉的基础。由于重叠或干扰信号会导致信息失真,接收到的信号被转换为数据矩阵后需使用各种机器学习算法和化学计量方法对相关信息进行判断、分类和识别,输出的不是单个成分的定量或定性分析结果,而是对样品整体味道的综合评价[6]。目前电子舌中使用的主要模式识别和定性定量分析方法有主成分分析法、聚类的独立软模式、最小偏二乘法、人工神经网络、判别函数分析和支持向量机等。
3、 电子舌的分类及研究进展
味觉传感器是电子舌的关键组成部分。根据味觉传感器工作原理的不同,电子舌可分为电位型、伏安型、阻抗谱型、生物传感器型等类型。很多味觉传感器具有交叉敏感性,即传感器对一类或几类物质皆有响应[7]。近年来,电子舌的研发主要围绕味觉传感器的传感材料、电极设计和不同传感器的组合优化等方面展开,用作电子舌传感器的传感材料包括脂质膜、导电聚合物和二维材料等[8⇓-10]。
3.1 电位型电子舌
电位型电子舌主要检测传感器与溶液相互作用所产生的电信号,通过分析电位差来研究样品的特性。这类电子舌成本低、设置简单、易于制造,至今仍是电子舌中应用最为广泛的类型,但其信号响应较弱,一般具有温度依赖性,使用寿命较短。
味觉受体蛋白在人味觉感知中起着关键作用。不过,由于蛋白质的化学和热力学稳定性较差,很难制造出基于蛋白质的味觉传感器。Kamo等[11]发现,在从牛舌上皮细胞中提取的脂质中浸渍的滤纸对盐和酸具有与活体味觉受体细胞相似的膜电位响应。在此发现的基础上,Toko等[12]研究和开发出基于人工脂质膜的系列味觉传感器,并于1993年在日本推出了第一种商用的味觉传感系统(SA401味觉传感系统)。目前最新的类脂膜味觉传感系统为日本Insent公司生产的TS-5000Z味觉分析系统,其能识别苦、涩、酸、咸、鲜、甜等味道,同时还可分析苦、涩和鲜的回味(丰富度)。
类脂膜味觉传感器的传感膜由类脂质(如十四烷基溴化铵、三辛基甲基氯化铵、油酸等)、塑化剂(如二辛基苯基磷酸酯、2-硝基苯基辛醚、三辛酯等)和聚合物载体(如聚氯乙烯等)组成。Ag/AgCl电极为参比电极,KCl和饱和AgCl溶液为内溶液(图3)。类脂膜味觉传感器对味道的选择性和灵敏度与所用类脂质、塑化剂的具体种类和浓度有关,选用合适的类脂质和塑化剂可得到对某种味道有选择性响应的传感器[4]。
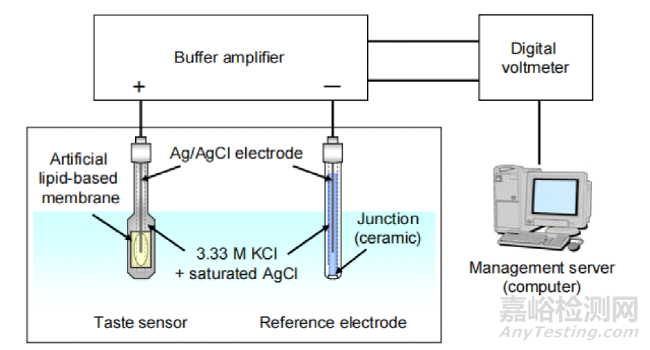
图3 类脂膜味觉传感器[13]
在电位型电子舌中,法国Alpha M.O.S公司开发的Asteree电子舌采用晶体场效应电极,仪器的集成性较好,软件系统也较完善,但仪器的清洗、校正时间长,传感器成本高、寿命短。Vlasov等[14]采用硫属玻璃传感器阵列作为工作电极,配以聚氯乙烯薄膜实现电位检测,具有良好的交叉敏感性。
3.2 伏安型电子舌
伏安型电子舌常采用三电极结构,分别为金属(铂、金、钯、铱、铼、铑等)裸电极或修饰电极等工作电极、Ag/AgCl参比电极和不锈钢辅助电极。伏安型电子舌系在工作电极阵列上施加循环伏安、常规大幅脉冲伏安和多频脉冲伏安等阶跃电势,不同待测溶液将产生不同大小的极化电流,通过对电流进行整体差异评价来定性和定量分析样品味觉的。
伏安型电子舌采用惰性贵金属传感器阵列,后者具有良好的耐腐蚀性和抗氧化性,使用寿命长,可以检测腐蚀性较强的样品,对于油类、脂类等电位型电子舌无法检测的样品也能正常检测。但伏安型电子舌响应信号的专属性差、冗余信息多,对后续数据处理要求高[15]。瑞典Winquest课题组和国内邓少平课题组研发的电子舌以伏安型电子舌为主。
3.3 阻抗谱型电子舌
阻抗谱型传感器最早由Riul Júnior等[16]提出,其以电化学阻抗谱法为基础,在贵金属电极上覆以导电聚合薄膜作为工作电极,通过测量系统阻抗谱来进行样品分析。阻抗谱型电子舌的响应灵敏度较高,但对电极修饰膜的制作要求也较高,重现性和稳定性较差,目前还没有整机应市[17]。
3.4 生物传感器型电子舌
生物传感器型电子舌的特点是在其传感器阵列中包含一个或多个生物传感器。生物传感器通过生物分子或组织如酶、抗原、抗体、受体、细胞、组织来采集信号。生物传感器型电子舌已被应用于某些口味特征和食品成分的选择性检测,但其发展仍处于早期阶段,实际应用较少[18]。
3.5 其他类型电子舌
Wang等[19]开发出一种不同于传统电化学方法的新型一体化太赫兹味觉传感器。该传感器利用太赫兹技术成像和感应太赫兹半导体发射器表面的化学反应,由离子敏感膜、蛋白质、DNA适配体、有机受体进行表面功能化,从而能够检测各种物质如溶液、生理离子、糖、有毒化学物质、药物、爆炸物的味觉。
Kim等[20]基于TiC丰富的表面官能团和金属导电性,通过将微流控通道与互指电极和Nafion层(一种常用的筛分层,只允许小阳离子迁移,同时防止大阳离子渗透)集成在一起,开发出高灵敏度、高选择性、可靠、可逆的pH传感器,用于检测样品的酸味。
Kossakowska等[21]开发出一种基于非离子表面活性剂泊洛沙姆的稳定、具有亲脂性核心的氨基敏感纳米颗粒,并用这种纳米颗粒来开发电子舌,以用于神经递质氨基部分鉴别,包括2-苯乙胺、多巴胺、γ-氨基丁酸、谷氨酸、天冬氨酸、乙酰胆碱、组胺和牛磺酸等。通过使用开发的电子舌尝试识别含有各种神经递质的膳食补充剂,结果证明了所开发的氨基敏感纳米颗粒传感系统在口感分析中的应用潜力。
受人舌头涩味感知机制的启发,Yeom等[22]开发出一种基于软水凝胶的人造舌,模仿人舌头的薄唾液层。这种人造舌由一个3×3传感器阵列组成,唾液状水凝胶充当传感层。水凝胶由黏蛋白作为分泌蛋白、氯化锂作为电解质、聚丙烯酰胺作为三维多孔聚合物网络组成,以促进电解质的流动。单宁酸是一种典型的多酚类物质,具有涩味。当单宁酸溶液扩散到水凝胶基质中后,单宁酸分子与黏蛋白结合形成疏水聚集体,而后将微孔水凝胶转化为分层微/纳米孔水凝胶,水凝胶的离子电导率随之增强。使用该人造舌测量不同浓度的单宁酸溶液时,可根据测量到的不同电流变化来判断单宁酸溶液的涩味。
4、 电子舌在药品口感评价中的应用现况
电子舌在药品口感评价中的应用包括药物掩味作用评价、药品处方筛选与优化,以及中药鉴别、质量评价与控制等[23]。
李学林等[24]采用经典人群口感评价法和电子舌探究羟丙基-β-环糊精等不同类型掩味剂在不同浓度时对苦味中药水煎液的抑苦效能和抑苦规律,不仅建立了掩味剂对苦味中药水煎液的抑苦效能评价方法,而且初步掌握了分子包合、高效增甜等不同抑苦机制掩味剂对苦参等苦味中药水煎液的抑苦规律。Monteagudo等[25]运用电子舌评价并优化苯巴比妥脂质体处方,改善了该处方的掩味作用、化学稳定性和增溶能力。Cilurzo等[26]运用电子舌评价双氯芬酸钠麦芽糊精口溶膜的苦味与合适掩味剂的抑苦效能,结果表明该技术可以帮助甚至替代口溶膜开发中的人感官评价法。
Li等[27]运用电子鼻、电子舌和电子眼收集智能感官数据,并通过高效液相色谱仪获得色谱数据,然后利用每组单源数据构建最小偏二乘法判别分析、支持向量机和反向传播神经网络模型,用于鉴定白芨及其类似药材(天麻、玉竹、黄花白芨)汤剂。采用无监督方法(如主成分分析法)和监督方法(如最小偏二乘法判别分析)从所有数据集中提取特征,再利用中级数据融合将4个数据集的特征组合在一起,比较特征提取方法对模型性能的影响。
Abu-Khalaf等[28]以头孢地尼混悬液为例,开发出一种运用电子舌鉴定不合格药品的方法。先对头孢地尼混悬液进行溶出行为、pH、相关物质和微生物污染等多项质量属性测试,然后运用电子舌对其味道进行10 d的随访。Pearson相关性分析显示,常规化学分析结果(头孢地尼含量、防腐剂含量、溶出行为、杂质总量、未知杂质总量)与混悬液味道变化之间呈显著相关性,即电子舌能将头孢地尼悬浮液的稳定性检测结果与其味道变化联系起来。
盐酸西替利嗪是常用抗过敏药物,但其味极苦,掩味是一个巨大挑战。Amelian等[29]运用电子舌评价了一种共聚物对盐酸西替利嗪的掩味效果,结果发现当药物与聚合物的质量比为0.5:1时,共聚物的掩味效果较好。该方法也可用于设计盐酸西替利嗪的口腔分散剂。
5、 结语与展望
电子舌是一种新型仿生味觉检测系统,兼有人口尝试验和理化性质分析的双重优势。味觉传感器是电子舌的关键组成,目前已商业化生产的有电位型和伏安型味觉传感器,其他如阻抗谱型、生物传感器型等味觉传感器尚在开发中。电位型味觉传感器的成本低、设置简单、易于制造,是电子舌中应用最为广泛的类别,但存在响应信号较弱、具有温度依赖性和使用寿命短等缺陷。伏安型味觉传感器具有良好的耐腐蚀性和抗氧化性,使用寿命长,但响应信号的专属性差、冗余信息多,数据处理要求高。电子舌在药品口感评价中的应用包括药物掩味作用评价、药品处方筛选与优化,以及中药鉴别、质量评价与控制等,但受味觉传感器和计算机算法发展的局限,现有电子舌还不能对所有检测对象均有很强的响应信号,准确度不高,无法完全模拟人舌的全部味觉受体,其结果尚无法直接作为药品口感评价的结论,且仪器体积较大,不方便使用。相信未来电子舌必会在进一步提高味觉传感器精度、减小仪器体积、优化算法和使用体验、提高检测准确度等方面取得显著进步,从而在药品口感评价中发挥更大的作用。
参考文献:
[1]
国家药监局药审中心. 国家药监局药审中心关于发布《儿童用药口感设计与评价的技术指导原则(试行)》的通告[EB/OL]. (2022-11-02) [2024-04-07]. https://www.cde.org.cn/main/news/viewInfoCommon/35fa15bba5721b0c653262d14792f3b6.
https://www.cde.org.cn/main/news/viewInfoCommon/35fa15bba5721b0c653262d14792f3b6
[2]
国家药品监督管理局药品审评中心. 国家药监局药审中心关于发布《儿童用药(化学药品)药学开发指导原则(试行)》的通告[EB/OL]. (2020-12-31) [2024-04-07]. https://www.cde.org.cn/main/news/viewInfoCommon/95102a5facaf8fd4430d0916a24eab53.
https://www.cde.org.cn/main/news/viewInfoCommon/95102a5facaf8fd4430d0916a24eab53
[3]
孙艳喆, 丛端端, 耿莹, 等. 儿童用药口感研究设计与评价的审评考虑[J]. 药学学报, 2023, 58(11): 3160-3164.
[4]
Kobayashi Y, Habara M, Ikezazki H, et al. Advanced taste sensors based on artificial lipids with global selectivity to basic taste qualities and high correlation to sensory scores[J]. Sensors (Basel), 2010, 10(4): 3411-3443.
本文引用 [2]
[5]
戚淑叶, 耿利华, 赵悦, 等. 电子舌在药品口感评价中的应用进展[J]. 药学学报, 2023, 58(11): 3151-3159.
[6]
陈淼, 任连杰. 电子舌在儿童用药口感评价中的应用[J]. 药学与临床研究, 2023, 31(6): 523-527.
[7]
Arab Hassani F. Bioreceptor-inspired soft sensor arrays: recent progress towards advancing digital healthcare[J]. Soft Sci, 2023, 3: 31.
[8]
黄嘉丽, 黄宝华, 卢宇靖, 等. 电子舌检测技术及其在食品领域的应用研究进展[J]. 中国调味品, 2019, 44(5): 189-193; 196.
[9]
王莉, 惠延波, 王瞧, 等. 电子舌系统结构及其检测技术的应用研究进展[J]. 河南工业大学学报(自然科学版), 2012, 33(3): 85-90.
[10]
Latha RS, Lakshmi PK. Electronic tongue: an analytical gustatory tool[J]. J Adv Pharm Technol Res, 2012, 3(1): 3-8.
[11]
Kamo N, Miyake M, Kurihara K, et al. Physicochemical studies of taste reception.Ⅰ. Model membrane simulating taste receptor potential in response to stimuli of salts, acids and distilled water[J]. Biochim Biophys Acta, 1974, 367(1): 1-10.
https://www.ncbi.nlm.nih.gov/pubmed/4472820
[12]
Toko K, Matsuno T, Yamafuji K, et al. Multichannel taste sensor using electric potential changes in lipid membranes[J]. Biosens Bioelectron, 1994, 9(4/5): 359-364.
[13]
Kobayashi Y, Hamada H, Yamaguchi Y, et al. Development of an artificial lipid-based membrane sensor with high selectivity and sensitivity to the bitterness of drugs and with high correlation with sensory score[J]. IEEJ T Electr Electr, 2009, 4(6): 710-719.
[14]
Vlasov Y, Legin A, Rudnitskaya A. Cross-sensitivity evaluation of chemical sensors for electronic tongue: determination of heavy metal ions[J]. Sensor Actuat B Chem, 1997, 44(1-3): 532-537.
[15]
戚淑叶, 毛岳忠, 耿利华, 等. 现有电子舌设备的技术现状与发展趋势[J]. 药学学报, 2023, 58(11): 3165-3172.
[16]
Riul Júnior A, Malmegrim RR, Fonseca FJ, et al. An artificial taste sensor based on conducting polymers[J]. Biosens Bioelectron, 2003, 18(11): 1365-1369.
https://www.ncbi.nlm.nih.gov/pubmed/12896837
[17]
白杰, 高利利, 张志勤, 等. 电子舌技术的原理及在中药领域的应用[J]. 中南药学, 2021, 19(1): 78-84.
[18]
Ha D, Sun Q, Su K, et al. Recent achievements in electronic tongue and bioelectronic tongue as taste sensors[J]. Sensor Actuat B Chem, 2015, 207(Part B): 1136-1146.
[19]
Wang J, Sakai K, Kiwa T. All-in-one terahertz taste sensor: integrated electronic and bioelectronic tongues[J]. Sens Diagn, 2023, 2(3): 620-626.
[20]
Kim HJ, Lee CW, Park S, et al. MXene-based high performance microfluidic pH sensors for electronic tongue[J]. Sensor Actuat B Chem, 2024, 409: 135636.
[21]
Kossakowska A, Szajda E, Jędryka N, et al. Development of lasalocid A-based amine-sensitive nanoparticles for “smart tongue” sensing of dietary supplements[J]. Sensor Actuat B Chem, 2024, 407: 135463.
[22]
Yeom J, Choe A, Lim S, et al. Soft and ion-conducting hydrogel artificial tongue for astringency perception[J]. Sci Adv, 2020, 6(23): eaba5785.
[23]
Wasilewski T, Migoń D, Gębicki J, et al. Critical review of electronic nose and tongue instruments prospects in pharmaceutical analysis[J]. Anal Chim Acta, 2019, 1077: 14-29.
https://doi.org/S0003-2670(19)30591-4
https://www.ncbi.nlm.nih.gov/pubmed/31307702
[24]
李学林, 康欢, 田亮玉, 等. 不同类型掩味剂对龙胆、苦参、穿心莲、莲子心4种中药水煎液的抑苦效能及抑苦规律评价[J]. 中草药, 2018, 49(22): 5280-5291.
[25]
Monteagudo E, Langenheim M, Salerno C, et al. Pharmaceutical optimization of lipid-based dosage forms for the improvement of taste-masking, chemical stability and solubilizing capacity of phenobarbital[J]. Drug Dev Ind Pharm, 2014, 40(6): 783-792.
https://doi.org/10.3109/03639045.2013.787536
https://www.ncbi.nlm.nih.gov/pubmed/23607724
[26]
Cilurzo F, Cupone IE, Minghetti P, et al. Diclofenac fast-dissolving film: suppression of bitterness by a taste-sensing system[J]. Drug Dev Ind Pharm, 2011, 37(3): 252-259.
https://doi.org/10.3109/03639045.2010.505928
https://www.ncbi.nlm.nih.gov/pubmed/20704459
[27]
Li H, Wang PP, Lin ZZ, et al. Identification of Bletilla striata and related decoction pieces: a data fusion method combining electronic nose, electronic tongue, electronic eye, and high-performance liquid chromatography data[J]. Front Chem, 2024, 11: 1342311.
[28]
Abu-Khalaf N, Zaid AN, Jaradat N, et al. Identification of substandard drug products using electronic tongue: cefdinir suspension as a pilot example[J]. Drug Des Devel Ther, 2019, 13: 3249-3258.
[29]
Amelian A, Szekalska M, Ciosek P, et al. Characterization and taste masking evaluation of microparticles with cetirizine dihydrochloride and methacrylate-based copolymer obtained by spray drying[J]. Acta Pharm, 2017, 67(1): 113-124.

来源:Internet
关键词: 药品口感评价