嘉峪检测网 2024-09-17 20:12
导读:在这篇小综述中,我们讨论了从文献调查中收集的ADCs的物理和化学稳定性方面,并说明了稳定性研究如何促进未来更有效ADC分子的开发。
摘要:抗体药物偶联物(ADCs)是一种新兴的化疗癌症治疗剂,它们结合了抗体的靶向特异性和小分子细胞毒性药物的高效杀伤潜力。与它们的蛋白质和小分子治疗对应物不同,ADCs的稳定性和降解特性相对未知。理论上,ADC的稳定性可能由来自抗体和连接子-毒素化学的属性和过程所控制。最近,在主要文献中提出了对ADC分子内在稳定性的系统性研究。由于工业和学术界正在努力开发下一代ADCs的优化偶联化学和抗体工程方法,因此捕捉对ADC稳定性当前理解的状态非常重要。在这篇小综述中,我们讨论了从文献调查中收集的ADCs的物理和化学稳定性方面,并说明了稳定性研究如何促进未来更有效ADC分子的开发。
1.引言
抗体药物偶联物(ADCs)代表了肿瘤学治疗领域的一类新型疗法。这些混合分子结合了单克隆抗体(mAb)的位点特异性和小分子细胞毒性化合物的强大抗肿瘤效果。最初被认为是Schofields的魔法子弹,这一愿景随着Kadcyla和Adcetris两种ADC产品最近获得FDA批准而逐渐成为现实,2014年的估计显示有超过38种不同的ADC分子正在进行实体瘤和血液恶性肿瘤的临床试验。Kadcyla由单克隆抗体Herceptin通过赖氨酸侧链连接到细胞分裂抑制剂DM1。赖氨酸侧链首先使用琥珀酰亚胺4-(N-马来酰亚甲基)环己烷-1-羧酸盐(SMCC)连接子转化为活性形式。DM1分子末端的自由硫醇然后允许与马来酰亚胺功能化的抗体偶联。Adcetris由人鼠嵌合抗体cAC10通过半胱氨酸残基连接到微管聚合抑制剂单甲基奥瑞司他丁E(MMAE)。首先对mAb进行部分二硫键还原,以提供有限数量的自由硫醇用于随后的偶联。与单独的mAb相比,ADC分子提供了一种潜在的更有效的形式,同时利用了高效细胞毒性剂的肿瘤杀伤活性。这些高效抗癌药物的系统性给药会带来严重的毒性问题;因此,ADC平台提供了一种靶向输送系统,以扩大这些药物的治疗潜力,否则这些药物可能无法提供给患者。
尽管概念上是合理的,但由于结合了连接子和毒素化学(连接子载荷)以及由此产生的修饰位点的异质性分布,ADCs比mAb或小分子成分要复杂得多。mAb本身的表征并不简单,因为必须监控许多关键质量属性(CQAs)以确保最终产品接受。除此之外,表征是对药物分子和药物产品的长期稳定性的深入理解。幸运的是,治疗性mAb的物理和化学稳定性已经得到了广泛的研究,并且降解途径与通常观察到的其他蛋白质一致。在单克隆抗体的开发过程中进行表征和稳定性研究,以了解物理化学负债,并建立控制策略,以确保适当的产品质量。
mAbs遇到的降解过程直接与ADCs相关,但除此之外,ADC与其mAb前体相比的化学和物理性质的改变引入了在ADC药物开发和制造过程中必须解决的额外稳定性考虑。ADC、连接子载荷和mAb的不稳定可能会影响分子的毒性、免疫原性和效力。ADC分子的制备涉及一系列激活、偶联、缓冲液交换或其他处理步骤,以从mAb和小分子起始材料中产生ADC分子。
尽管这些步骤对成品ADC材料稳定性的影响在主要文献中才刚刚开始显现,但下一代ADCs在开发和临床管道中的密集管道显然需要对ADC稳定性的当前状态信息进行评估。本文提供了对主要文献中关于ADCs物理和化学稳定性的独特方面以及所使用的测量方法的当前理解状态的综述。
关于物理稳定性,学到的经验可以应用于不同偶联方法的ADC格式。另一方面,化学ADC稳定性研究主要集中在基于半胱氨酸或马来酰亚硫醇偶联上,因为特定的降解或可逆性途径已经详细检查。这些研究实现了提供更稳定和均匀ADC分子的预期目的。基于半胱氨酸或工程氨基酸而不是赖氨酸的偶联方法也在ADC稳定性研究中占主导地位,因为这些技术产生的ADC分子具有较低的药物载荷和较窄的分布,这些属性已被确定为对治疗窗口有益。
2.抗体药物偶联物的物理稳定性
2.1.与偶联过程相关的不稳定性
ADCs的物理稳定性和降解研究主要解决mAb聚集问题,以及由处理步骤或连接子和药物修饰的物理影响带来的聚集倾向增加。治疗性mAb本身的聚集已经得到了广泛的研究,并为扩展到ADCs提供了一些必要的理论和概念框架。在工业追求ADCs之前,已经确定了硫醇修饰或IgG1抗体的部分还原对四元结构和结合性质的影响。首个获批的ADC,Mylotarg,由卡利奇霉素衍生物ozogamicin与抗CD33抗体gemtuzumab偶联。这个ADC代表了将疏水性小分子连接到大型亲水性蛋白质的困难。对于Mylotarg,偶联需要高达20%的二甲基甲酰胺(DMF)以保持疏水性ozogamicin连接子载荷的溶解性。DMF的存在被证明促进了过度的(高达约50%)聚集形成,通过尺寸排除色谱法(SEC)测量。甘油、丙二醇和辛酸等偶联添加剂被证明可以减轻聚集问题,并允许在偶联过程中使用较低的DMF浓度。
ADCs的聚焦物理稳定性评估可能最初是在Trastuzumab(Tmab)、赖氨酸激活的Tmab T-MCC(使用SMCC激活)和完全偶联的ADC分子T-DM1之间的比较中描述的。在一系列通过差示扫描量热法(DSC)、SEC、液相色谱-质谱(LC-MS)和电泳分析的扩展压力稳定性实验中,明确确定T-MCC和T-DM1比Tmab更容易聚集,聚集倾向的顺序是T-MCC>T-DM1>Tmab。在DSC实验中,观察到T-MCC、T-DM1和Tmab的可逆热转变;然而,T-MCC还展示了一个不可逆的成分,表明了聚集。在40°C下储存7天后的SEC分析中也展示了聚集趋势,其中在T-MCC中观察到高达32%的高分子量物种(HMWS)的丰度。通过质谱和电泳确认了共价聚集作为这些T-MCC中HMWS的主要贡献者。在添加游离氨基酸(Cys、Tyr、Ser)的情况下观察到共价聚集的抑制,支持了T-MCC中游离暴露的马来酰亚基团能够交联的假设。这些发现说明了在处理马来酰亚胺或其他活性化学物时控制副反应的重要性。
Acchione等人使用差示扫描量热法研究了赖氨酸连接、硫醇连接和糖基连接模型IgG1-生物素偶联物的热稳定性。这项工作的一个主要观察结果是,与赖氨酸连接相比,硫醇偶联对抗体的破坏性影响更大。还观察到,使用TCEP进行的部分抗体还原对整体热稳定性的影响非常小,表明观察到的稳定性损失不是直接由于部分mAb还原。
2.2.温度诱导或光诱导不稳定性
典型的稳定性测试策略在小分子和生物分子治疗剂中使用,是通过提高温度暴露来加速潜在不稳定性问题的出现。Adem等人使用温度和离子强度作为压力条件,检查每抗体高达8个偶联药物的硫醇连接MMAE药物载荷增加的影响。通过制备性疏水作用液相色谱(HIC)分离出具有不同药物-抗体比(DAR)的抗体偶联物,允许检查与MMAE逐渐增加的疏水性相关的效应。高DAR组分的HMWS形成增加,在更高的离子强度条件下效果更加明显。已经建立了更高DAR与降低体内性能之间的联系。高DAR物种的结构不稳定化可能促成了体内加速清除。Lyon等人最近对疏水性的检查表明,通过亲水性连接子设计或附加聚乙二醇(PEG)链(“PEG化”)获得的更亲水的auristatin ADCs可以提高效力。
Beckley等人使用多种光谱和分离工具检查了随DAR增加而诱导的温度诱导聚集。具有不同DAR值的半胱氨酸偶联ADCs在40°C下孵化,之后收集单个SEC分数并通过DSC、远紫外圆二色光谱、电泳和反相高效液相色谱(RP-HPLC)分析。综合来看,研究表明DAR 6和DAR 8物种在压力条件下更容易形成聚集体,SEC分析中观察到的HMWS主要由DAR 6和DAR 8物种组成。更具体地说,DSC证据表明,由偶联引起的CH2/铰链区的部分展开是聚集形成的原因。
Guo等人最近对物理不稳定性的检查以高级光谱工具结合量热学和分子建模进行高阶结构分析。通过这些技术,与mAb相比,二级和三级ADC结构的不可逆不稳定化得到了精心确认。
在处理和最终制造过程中,ADCs也间歇性地暴露于光线下。由于一些ADC载荷携带光吸收和光敏取代基,Cockrell等人在模型ADC系统中评估了光照暴露。通过SEC和动态光散射分别观察到ADC中的聚集体和颗粒形成,而在起始抗体或单独的连接子载荷中没有观察到这些现象。
3.抗体药物偶联物的化学稳定性
一般来说,mAbs或其他治疗蛋白可能会发生许多潜在的化学降解途径。尚未特别研究临床上相关的连接子载荷对这些mAb降解过程的影响。然而,正如本节所讨论的,已经确定并研究了一些影响连接子-载荷稳定性和偶联稳定性的ADCs的化学降解过程。
3.1.与偶联过程相关的化学不稳定性
ADCs的制造需要一些特定的工艺步骤将药物部分偶联到mAb上。对于赖氨酸和半胱氨酸偶联,使用激活步骤以提供一定程度的位点特异性。激活和偶联步骤本身涉及与活性剂的孵化期,有时在提高的温度下(通常为37°C)。最终ADC制造还涉及额外的缓冲液交换、溶剂去除和浓度步骤。前面已经描述了赖氨酸激活和偶联以及溶剂暴露的一些潜在陷阱,与物理不稳定性有关。特别是,赖氨酸激活步骤引入了激活物种交联的风险。基于半胱氨酸的偶联利用部分二硫键还原来生成控制数量的游离硫醇,这个过程本身引入了潜在的四元结构不稳定化。其他mAb化学降解途径也可能作为游离硫醇形成的间接后果而发生。Amano等人最近描述了IgG1的铰链区半胱氨酸种族化在几个月的储存期间发生。这一观察强调了mAb在处理过程中遇到的高温和高pH暴露可能会促进许多铰链区氨基酸异构化途径。这些修饰最终影响mAb支架的关键质量属性,包括结构完整性和结合亲和力。另一个潜在的问题是,如前所述,CH2/铰链区不稳定化与ADC聚集有关。
下一代ADC偶联技术的目标是通过使用众多分子工程方法或通过新型化学方法的出现完全绕过控制二硫键还原步骤。Badescu等人描述了一种可能限制最终ADC分子中残留游离硫醇存在的偶联方法。这种方法源自于生成PEG偶联蛋白的类似方法,首先在温和条件下还原二硫键,然后引入双功能试剂以启用顺序Michael加成/消除反应。二硫键通过带有PEG连接药物载荷的3碳间隔子桥接。据报道,该反应几乎是定量的(95%),所得ADC在存在DTT的情况下抗还原且对解偶联稳定。该方法提供了一个更均匀的ADC药物物质,并限制了暴露游离硫醇的风险。最重要的是,安装带有连接子载荷或PEG基团的3碳间隔子与原始二硫键形式相比没有损害三级mAb结构。
3.2.载荷释放
在ADCs的背景下,对载荷本身的降解或直接释放后偶联的研究有限。通常,通过HPLC或LC-MS直接监测制剂,载荷损失很小,例如Francisco等人在研究通过缬氨酸-瓜氨酸连接的cAC10基半胱氨酸偶联物时观察到的<2% MMAE损失在10天血浆孵化期间。Doronina等人通过直接检查替代连接子化学,确认了MMAE和auristatin E(AE)化合物在长期稳定性试验中不会在缓冲液中或在存在人类肝脏溶酶体提取物或蛋白酶的情况下释放。这些研究还证实,常用的腙连接子比蛋白酶敏感的缬氨酸-瓜氨酸连接子化学和生化稳定性差。腙连接子的不稳定性以及过早的ozogamicin载荷释放被认为是Mylotarg效力差的主要原因,该药物在2010年被撤出市场。
在最近的研究中,使用单甲基auristatin D(MMAD)载荷的位点特异性偶联化学,观察到MMAD的末端dolaphenine基团在啮齿动物血浆中容易裂解。这种降解通过HIC和LC-MS/MS分析观察到,发现这种反应的程度取决于偶联位点。重要的是,血浆中MMAD的裂解反应也被发现是物种依赖的,在人类血浆中没有观察到ADC的可检测降解,尽管在小鼠血浆中观察到了对效力的明显影响。已经证明,通过赖氨酸激活SMCC连接子制备的偶联物可以释放高达5%-6%的游离药物。在这种情况下,载荷释放更与原始SMCC激活步骤的非预期副反应有关,而不是直接的赖氨酸解偶联。在HPLC和LC-MS实验中观察到SMCC连接子与赖氨酸之外的半胱氨酸和酪氨酸侧链反应。所得的硫酯和酯键被证明比与赖氨酸胺形成的酰胺键不稳定。
3.3.马来酰亚胺-硫醇偶联物中偶联的可逆性
关于ADCs化学稳定性的主要研究领域是关注连接子载荷与mAb上半胱氨酸的共价连接的稳定性。最终,ADCs的设计是不稳定的,它们会经历生化降解以释放自由药物,作为它们药理学的一部分。在这篇综述中,我们主要关注从化学、制造和控制的角度来看ADC药物物质的化学和物理稳定性。关于ADC药理学的综述,包括导致载荷释放的细胞降解事件,已有提供,因此不在本次综述的范围之内。制造半胱氨酸连接的ADC主要通过马来酰亚胺-硫醇反应化学进行半胱氨酸偶联。尽管通常被认为是化学稳定的生物偶联方法,但有明确的证据表明这种偶联是可逆的,当ADC分子给药并在循环中遇到游离硫醇时,这种可逆性就会显现出来。这不是严格意义上的化学、制造和控制视角下的不稳定性,但显然已经揭示了平衡现象的存在,这从整体ADC化学稳定性的角度引起了相当大的关注。
Alley等人直接研究了暴露于血浆中的ADC的马来酰亚胺-硫醇连接的逆转。在旨在评估通过硫醚连接形成的非水解稳定连接的稳定性的研究中,观察到MMAF药物释放,并伴随着血浆中连接子药物与白蛋白的结合。使用基于MMAF的亲和捕获,通过LC-MS和肽图技术确认了修饰位点为白蛋白的Cys-34。这种白蛋白共价修饰的位点与其他系统性给药的含有马来酰亚胺的抗癌药物的观察结果一致。已经报告了假定稳定的亲电蛋白修饰的可逆性;然而,直到最近,这种现象才在提高化学稳定性的背景下进行了检查。硫醇-马来酰亚胺偶联物在中性pH下通过钼酸盐催化的水解形成水解的琥珀酰亚胺硫醚的亚胺基团的水解已经之前检查过。
Baldwin和Kiick使用模型硫醇,包括巯基苯乙酸和谷胱甘肽,进行了关键实验,建立了硫醇-马来酰亚胺可逆性的更全面视图。使用NMR、HPLC和LC-MS,实验显示了游离和偶联硫醇形式之间的交换,但也存在一个额外的机制分支,导致形成稳定的环开的琥珀酰亚胺形式的硫醇-马来酰亚胺连接。分支程度观察到取决于马来酰亚胺的取代和可用于交换和捕获的游离硫醇的浓度。
琥珀酰亚胺逆Michael反应的基本机制在图1中表示。一旦制造和纯化,硫代琥珀酰亚胺偶联物1与去偶联的马来酰亚胺2存在明显的平衡。马来酰亚胺2在循环中发现的过量游离硫醇基团存在下易于Michael加成,生成如图3所示的共价加合物。基本上,例如白蛋白的过量游离硫醇基团的存在,推动平衡向形成3的形成,以至于在溶液中没有直接观察到游离马来酰亚胺2。还展示了从偶联物1的慢分支途径,通过这种方式形成了环开的琥珀酰亚胺硫偶联物4。观察到偶联物形式4是一个抵抗进一步水解的终点物种。
在曲妥珠单抗-MMAE偶联物的额外研究中,建立了马来酰亚胺可逆性的位点依赖性组成部分。使用位点定向突变体在Fc、轻链(LC)或重链(HC)域放置游离硫醇,Shen等人观察到LC偶联物在血浆孵化后DAR减少方面最稳定。额外的半胱氨酸Fc突变体揭示了稳定性是一个位点依赖性而不是域现象。重要的是,反映在DAR随时间变化的稳定性并没有与游离MMAE浓度相关,这些浓度相对恒定。相反,如前所述,白蛋白对释放的有效载荷的捕获解释了DAR损失。此外,通过LC-MS观察到更稳定的偶联物具有额外的(+18)质量单位,支持了水解琥珀酰亚胺环开在防止逆Michael反应中的作用。
还提出了导致硫醚在硫醇-马来酰亚胺偶联物中降解的氧化过程。在这个过程中,不希望的细胞毒素释放可能通过完全硫氧化形成自由硫酸盐类似物发生,而部分氧化为亚砜可能解释了在氧化过程中效力的保持。在维持低pH的重要性在硫醚连接的氧化研究中得到强调,并且在后偶联ADC处理的背景下需要进一步的氧化研究。
先前概述的硫醚可逆性实验体和在图1中显示的实验直接揭示了通过涉及DAR或游离载荷释放的常规稳定性试验不会观察到的降解过程。最关键的化学稳定性设计涉及使用血浆孵化,然后是亲和捕获和分离的ADC 40的表征,通过HIC进行DAR分析和LC-MS进行精确分子量变化的识别。这种类型的工作流程使研究人员能够仔细研究马来酰亚胺-硫醇可逆性问题,如果直接监测游离药物或游离连接子载荷将是不成功的。
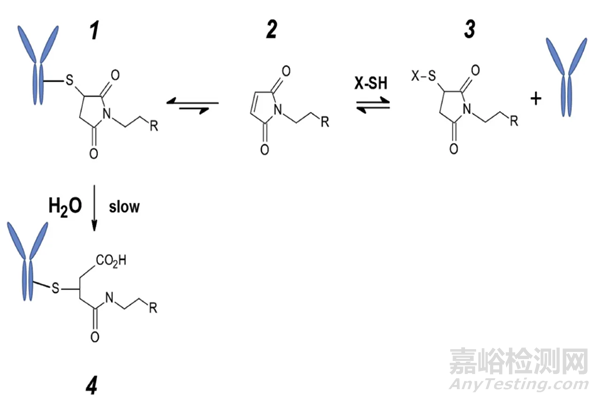
图1. 抗体药物偶联物特异性的主要化学降解途径——马来酰亚胺-硫醇反应的可逆性说明。具有马来酰亚胺功能的连接子-载荷与单克隆抗体(mAb)上的游离硫醇反应,形成琥珀酰亚胺硫醚抗体偶联物(1)。在纯化偶联物(1)后,与未偶联的马来酰亚胺(2)存在一个平衡状态,以至于在循环中的过量亲电物质(X-SH),如白蛋白或谷胱甘肽,可以经历Michael加成形成共价加合物(3),导致抗体解偶联。琥珀酰亚胺硫醚(1)也可以经历水解,形成不可逆的环开形式(4),这是一个稳定的基团,已被证明其在血浆中的半衰期明显长于典型的mAb半衰期。
Dorywalska等人在MMAE不稳定性研究中提供了ADC亲和捕获工作流程的最新演示,其中结合的MMAE分子的化学不稳定性只有在从血浆中亲和回收后才被识别出来。实验还揭示了与MMAE降解导致的效力损失相关的物种差异。更广泛地说,这些基础研究揭示了偶联稳定性和清除率、偶联位点、整体DAR以及由此产生的观察效力之间相互作用的更深层次的复杂性。也许最重要的是,这些发现有助于确定设计新一代更稳定、更有效ADC的方法,这些ADC的制造复杂性有所降低。
3.4.马来酰亚胺可逆性的潜在解决方案
针对马来酰亚胺可逆性问题的主要解决方案是通过促进永久性的琥珀酰亚胺环水解来颠覆逆Michael硫醇-马来酰亚胺反应。
最近发现,通过将溶液pH提高到9.2,可以在大约14小时内将近100%地将环开形式(图1,物种4)转化。通过仔细的LC-MS实验,确认了在LC和HC上的偶联都可以同样高效地转化为水解的环开形式。还观察到连接子类型影响了琥珀酰亚胺水解的效率,PEG连接子比马来酰亚己酰连接子更容易转化。在对自催化琥珀酰亚胺水解进行更具体的检查时,Lyon等人准备了含有靠近马来酰亚胺氮的伯胺取代基的连接子。发现一个氨基甲基取代基显著增加了琥珀酰亚胺水解速率,以至于在中性pH下不到6小时内就能实现近100%的转化。这种转化速率在LC和HC的偶联上观察到是相似的。进一步的研究证实了电子吸引基团在马来酰亚胺N取代基上加速水解琥珀酰亚胺环开和稳定化的作用。
传统马来酰亚胺化学的替代品代表了解决逆Michael问题的另一种方法。如前所述的二硫键桥接方法,作为保护游离硫醇免受不需要的副作用的一种方式,也绕过了马来酰亚胺可逆性问题,因为生成的偶联物是通过3碳烷基桥与连接子载荷形成的。类似的二硫键桥接方法旨在提供位点特异性、均匀的ADCs也已出现。其他活性化学物提供了替代马来酰亚胺靶向游离硫醇的选择,如芳丙腈或取代苯并噁二唑甲烷磺酸酯。结合抗体工程方法代表了替代基于马来酰亚胺的偶联并提供位点特异性连接子-载荷附着的另一个方向。细菌转谷氨酰胺酶已被用于催化工程谷氨酸残基与连接子-载荷分子末端的伯胺之间形成酰胺键。通过工程化含有目标谷氨酸残基的转谷氨酰胺酶识别序列,实现位点特异性偶联。抗体也可以通过非天然氨基酸进行位点特异性工程化,提供替代的生物正交化学反应能力。这种方法最先进的例子是使用对乙酰苯丙氨酸与auristatin衍生物形成肟键,或者使用工程化甲酰甘氨酸氨基酸与色氨酸功能化的载荷进行Pictet-Spengler连接。应该认识到,这些方法绕过了马来酰亚胺可逆性的具体问题,代表了下一代ADC优化的一个进步。然而,广泛认识到的是,抗体工程的更广泛挑战以及这些主要结构修改可能带来的不稳定性尚未完全检查。
4,ADC稳定性分析的实验方法
4.1.用于ADC稳定性分析的方法
药物物质和药物产品的稳定性直接与ADCs的关键质量属性(CQAs)相关,这些属性必须在ADC开发成注册产品期间进行评估。这些研究中获得的信息类型高度依赖于使用的方法,表1提供了最近ADC分析研究中使用的方法的概述。表1中包括了每种技术提供的与稳定性相关的信息的代表性文献示例。最近也对用于ADCs物理化学表征的一些技术进行了回顾。由于ADCs是非常复杂的分子,通常需要通过两个或多个技术使用适当的实验设计来检查稳定性的特定方面。
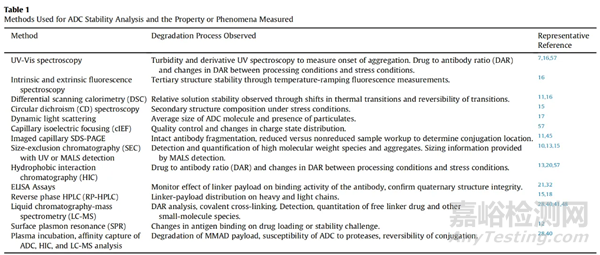
通常,通过表1中的溶液光谱技术如圆二色性、紫外-可见、荧光或动态光散射来检查物理稳定性。此外,DSC对于理解溶液稳定性至关重要,而SEC与UV或MALS检测是监测聚集存在的重要工具。最后,ELISA通常用于确认mAb支架的结合活性,因此也报告了溶液四元结构。所有这些技术都允许在ADC分子的天然溶液状态下进行分析。这些方法的典型实验设计是在通常应用热处理前后仔细记录光谱模式。
可以通过几种正交分离技术来分析ADCs以表征化学稳定性问题。HIC已成为确认半胱氨酸或相关偶联物的DAR值的中心技术,其中连接子-载荷分子为ADC增加了显著的疏水性。HIC分离后的分数也可以以更制备的方式使用,以分离单个DAR物种进行进一步表征。某些形式的高性能LC-MS,如识别H2O的添加或丢失,可以提供更精确的分子量信息。此外,基于MS的技术(MS/MS)可以用来确认偶联或化学变化的主要位点,使用将ADC消化成肽段进行序列分析的蛋白水解工作流程。质谱和HIC也是观察和表征硫醇-马来酰亚胺可逆性的重要工具,当与亲和捕获工作流程结合时。进行还原和非还原SDS-PAGE的能力也提供了一个直接的工具来表征和定位ADC偶联模式。最后,成像毛细管等电聚焦(icIEF)提供了一个机会,以确定降解ADCs的电荷状态分布的变化。
4.2.与分析测量相关的稳定性伪影
生物治疗药物的样品准备和分析表征通常需要破坏性条件,这些条件可能产生伪影降解特性。ADCs的一个关键质量属性是来源于连接子药物的小分子杂质含量。如前所述,就化学ADC稳定性而言,直接的HPLC测定药物分子本身的分析并不一定能揭示降解过程。有趣的是,最近有研究表明,来源于连接子药物的物种分析因RP-HPLC分析过程中的降解而变得复杂。这些方法通常使用低pH、30-40分钟的运行时间、高含水量以及在30°C-40°C附近的柱温度,所有这些条件都支持水解过程。通过在5°C-10°C下运行测定、在稀释溶剂中使用乙腈代替醇类,以及使用超高压液相色谱进行更快的分析,可以减缓RP-HPLC分析过程中连接子药物的降解。在更精细的实施中,这些原理被应用于使用在线二维分离技术对ADC样品中的高分子量和低分子量物种进行表征。在第一维色谱中,SEC分离了HMWS,如单体、二聚体和聚集体,并且还允许在稳定的中性pH条件下从小分子物种中分离出完整的ADC。然后,SEC维度的分数与RP-HPLC耦合,以更详细地分析ADC稳定性样品中的低分子量物种。在电泳过程中也观察到马来酰亚胺-硫醇PEG偶联物的解偶联。在这种情况下,装载前的短暂高温处理步骤与降解相关。有人假设Tumey等人提出的氧化硫醚断裂途径可能是这一观察结果的可能机制。建议使用较低的温度(60°C),在SDS-PAGE装载前进行更长时间的预处理,以最小化硫醚断裂。
5.结论
ADCs的化学和物理稳定性表征仍处于早期阶段。随着新的偶联和抗体工程方法的出现,ADC的开发和临床管道将继续增长。同样,对稳定性分析的健壮工具的需求也将增长。从这篇综述中可以收集到许多宝贵的经验。首先,从二级、三级和四元结构的角度对ADCs的生物物理分析以监测配方稳定性才刚刚开始被探索。其次,使用ADCs的亲和捕获和体外血浆孵化后的色谱和/或LC-MS分析(或扩展到其他复杂基质)是一种巨大的转化工具,将传统的储存化学稳定性与体内化学稳定性联系起来。最后,对马来酰亚胺-硫醇反应性和可逆性的应用于基础研究揭示了进一步优化ADC的机会,提供了具有改善稳定性和效力的新一代分子。

来源:药时空
关键词: ADC药物