嘉峪检测网 2024-10-25 11:15
导读:近日,MicroPort微创公布创领心律管理医疗器械(上海)有限公司的 PLATINIUM™系列植入式心律转复除颤器(ICD)正式获得国家药品监督管理局(NMPA)颁布的医疗器械注册证。
近日,MicroPort微创公布消息,全资子公司创领心律管理医疗器械(上海)有限公司(以下简称“创领心律医疗”)生产的 PLATINIUM™系列植入式心律转复除颤器(ICD)正式获得国家药品监督管理局(NMPA)颁布的医疗器械注册证,成为国内首个获批上市的国产 ICD,即将正式投入临床应用。
本次获批的植入式心律转复除颤器包括双腔 PLATINIUM DR 1540 和单腔PLATINIUM VR 1240 两个型号规格。
2017年,LivaNova(2015年由神经调节器械公司Cybernoics收购意大利索林后成立)以 1.7 亿美元现金将心律管理业务(CRM-索林品牌)出售给了微创医疗,其中包括了 LivaNova 原先开发上市的 ICD 产品 PLATINIUM™ ICD,该产品具有全球最长 14.3 年的使用寿命,可降低频繁更换 ICD 可能产生的风险。
2022年5月,由微创旗下子公司微创心律引进的 PLATINIUM™系列 ICD(DR 1540、 VR 1240)获NMPA批准(进口医疗器械注册)。
源于国家药品监督管理局
创领心律医疗由上海微创医疗器械(集团)有限公司与意大利索林集团合资成立于2014年,主要从事心律管理器械(包括起搏器、ICD及CRT等)的研发、生产和营销,微创®集团从2010年起就开始了植入式心脏起搏器项目的高强度、大投入研发工作。2015年6月,中国第一条与国际先进水准接轨的国产心脏起搏生产线在创领心律医疗落成,开辟起搏疗法由“中国制造”到“中国创造”之路。
2018年2月,微创医疗发布公告,宣布其与云锋基金共同出资约 15 亿港元(约合1.9 亿美元)收购意大利医械公司 LivaNova 旗下心律管理业务(CRM)品牌索林(Sorin),主要包括起搏器、除颤器、心脏再同步装置。

研发背景
植入型心律转复除颤器(ICD)主要用于监测和纠正心脏的严重心律失常,如伴有黑矇、晕厥等症状的室性心动过速、心室扑动和心室颤动等。这些心律失常如果不及时纠正可能导致心脏骤停和死亡。
现在临床应用的 ICD 主要有2种类型:一种是经静脉植入型心律转复除颤器(TV-ICD),就是需要通过静脉将除颤导线送至心脏;另外一种是全皮下植入型心律转复除颤器(S-ICD),无需通过静脉路径,脉冲发生器和导线都埋在皮下。
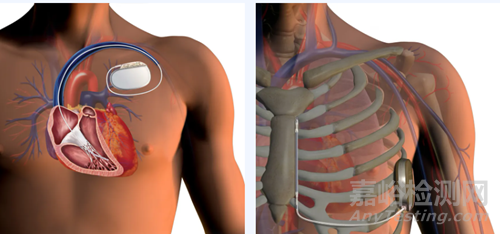
TV-ICD(左)和 S-ICD(右)
根据中华医学会心电生理和起搏分会第十五次学术双年会(CSPE2024)披露的最新数据,在中国,每年约有100万人死于心源性猝死。经循证医学证据表明,植入 ICD 是目前预防心源性猝死唯一有效的治疗手段。
ICD 由于其产品技术门槛高、系统集成复杂,对及时性、有效性和安全性有着极高的要求,又兼具起搏器提供的起搏功能,目前处在 CRM 领域研究的最前沿,被誉为“心脏全科器械皇冠上的明珠”。临床实验证明,植入 ICD 的疗效远超服用抗心律市场药物。因此,美国/欧洲/中国的相关指南或专家共识中,均将 ICD 列为治疗 SCD 的“金标准”。
长期以来,国内 ICD 疗法渗透率相较于心源性猝死高风险人群而言,尚处较低水平,且国内临床所使用的该类产品均来自进口企业,此次 PLATINIUM™ ICD 的获批,正式开启了我国心律管理领域高能量除颤细分市场的国产化之路。
产品详情
本次获批的植入式心律转复除颤器包括双腔PLATINIUM™ DR 1540 和单腔PLATINIUM™ VR 1240 两个型号规格。

▲PLATINIUM™系列植入式心律转复除颤器
产品由植入式心律转复除颤器(双腔型号 PLATINIUM DR 1540,单腔型号PLATINIUM VR 1240)、连接端(包含IS-1(双腔)、DF4)及一个扭矩扳手组成,用于提供心室抗心动过速起搏和除颤功能,对危及生命的室性心律失常进行自动治疗。
PLATINIUM™单腔 ICD 预期使用寿命超过 14 年,双腔 ICD 预期使用寿命超过 13年,较长的设备使用寿命能显著减少设备更换次数,从而降低设备置换手术带来的并发症风险。
同时该产品配有先进的基于房室关系的鉴别算法(PARAD+™),精准鉴别室上速,避免误治疗,专有的 BTO 算法允许患者在心动过速区实现生理性起搏。
产品市场概况
全球植入式心脏复律除颤器(ICD)市场在近年来呈现稳定增长的趋势。根据相关市场研究报告,2022年全球市场规模达到了数十亿美元,预计到2028年将达到更高的市场规模,年均复合增长率(CAGR)保持在个位数的百分比范围内。
在地区分布上,北美市场由于其成熟的医疗基础设施和较高的医疗保健支出,占据了较大的市场份额。亚太地区则因其快速增长的医疗需求和市场潜力,预计将成为增长最快的市场。欧洲市场也占有重要地位,尤其是在心脏病治疗方面的先进国家如德国、英国、法国和意大利。
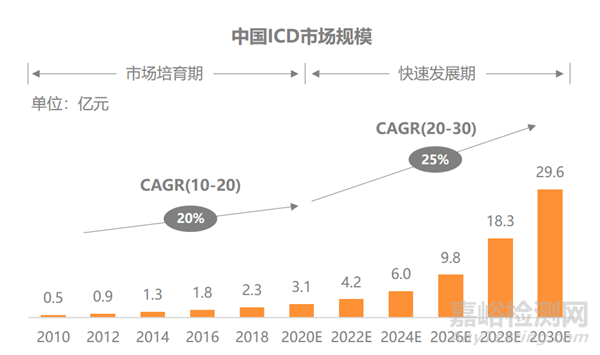
作为 CRM 最重要的细分板块,我国 ICD 市场过去五年内的复合增长率接近 20%,并有望在未来的10年内达到 25% 的复合年增速,至 2030 年达到 29.6 亿的市场规模。这一高增长率的背后是我国 ICD 行业目前仍然处在早期培育期的现状,蓝海市场清晰可见。
全球ICD市场的主要参与者包括美敦力 Medtronic、波士顿科学 Boston Scientific、百多力 Biotronik、雅培Abbott(收购了St. Jude Medical后)等公司。这些公司在技术创新、产品质量和全球分销网络方面都具有较强的竞争力。目前我国已获批的进口 ICD 产品共 13 款,国产 ICD 产品仅有创领心律 1 款获批上市。
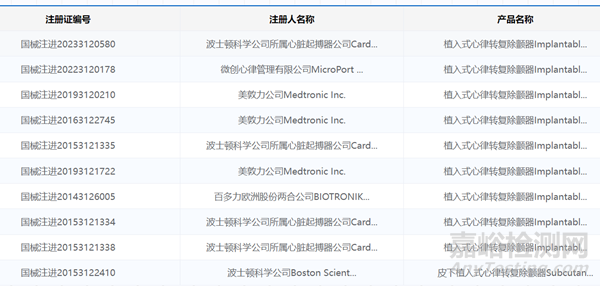
已获批的部分进口ICD产品
ICD 作为高电压产品,研发需要攻克多项高难度技术,如高效率高压充放电模块、导线的药物释放系统、程控的UI设计、感知识别算法等。
值得注意的是,TV-ICD(经静脉植入型)临床应用时间长、除颤有效,但存在血管阻塞、导线脱位、三尖瓣损伤、系统感染、导线拔除困难等问题和并发症,S-ICD(全皮下植入型)是 TV-ICD 的替代解决方案,于2009年应用于临床,S-ICD 并发症少,但存在系统耗能大、体积大、寿命短、适应范围有限等缺陷。
EV-ICD(血管外植入型)是 ICD 技术发展方向,除包含 S-ICD 功能外,还具有体积小、使用寿命长、能量低等特点。EV-ICD 可同时进行心外膜起搏、ATP治疗,适应范围更广泛。随着研究深入,EV-ICD 有效性、安全性得到了进一步验证,临床应用前景广阔。
目前,美敦力已推出血管外心律转复除颤器(EV-ICD/Aurora EV-ICD™),在发展安全有效的 ICD 技术上迈出重要一步。Aurora EV-ICD 系统是全球唯一可以同时提供心脏复律除颤、抗心动过速起搏(ATP)以及停搏预防起搏(PPP)功能的血管外植入式除颤器,也是首款将除颤电极导线置于胸骨后左缘、心包表面的 ICD。
2024年7月,在海南博鳌瑞金海南医院成功开展了全国首例 Aurora EV-ICD™ 植入术。在此之前,波士顿科学已推出具有划时代意义的全皮下植入型心律转复除颤器(S-ICD),同样不接触心脏和血管。
目前国内 ICD 领域的代表厂商是创领心律医疗和无双医疗。
创领心律医疗旗下已有心悦Rega、心韵Trefle、心兰Orchidee三款起搏器产品获得NMPA注册证。此前,母公司微创医疗在2017年收购 LivaNova 后拥有了 CRM 全套产品线,Platinium™ ICD 产品在海外市场反响良好,并以进口形式进入中国。
无双医疗成立于2017年,自主研发的植入式心律转复除颤器(安搏®ICD)临床试验已经完成了75例患者的顺利入组,预计2026年上市销售。2023年9月,无双医疗的ICD产品通过国家药监局审核,进入特别审查程序(即“绿色通道”),是首款进入创新特别审查程序的植入式心脏复律除颤器产品。该植入式心脏复律除颤器能够实现自动感知起搏、40J能量充放电、流线型设计和蓝牙遥测,可预防心脏骤停,降低医保与患者负担,更贴近亚洲人群需求。

无双医疗ICD产品
可以预见,随着医疗数字化、信息化理念的提出,在我国目前相关市场高度被进口厂商垄断的背景下,国产厂家也迎来填补国产空白,实现进口替代的黄金发展时期。
创领心律医疗
创领心律管理医疗器械(上海)有限公司成立于2014年,公司致力于研发、制造与心脏节律疾病管理相关的医疗器械,并提供相应的技术服务与咨询,同时进行医疗器械的销售与进出口业务。公司有近200名员工,其中60%以上为研发人员。目前,公司在全球累计拥有专利及专利申请超过200项。
创领心律医疗的核心产品包括多个系列的植入式心脏起搏器。其中Rega®心系列植入式心脏起搏器是国内首个具有国际品质的国产心脏起搏器,具有自动化、生理性等特点,体积仅8立方厘米,使用寿命高达10-12年。此外,公司还推出了ENO™系列植入式心脏起搏器和Vega™植入式心脏起搏电极导线,这些产品均具有磁共振条件安全功能。

来源:心未来
关键词: 除颤器