嘉峪检测网 2024-12-11 20:34
导读:建立高效液相色谱法同时测定晕可平糖浆中5-羟甲基糠醛、丹参素、原儿茶醛、咖啡酸、苯甲酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸、甘草酸9种成分的含量。
摘 要: 建立高效液相色谱法同时测定晕可平糖浆中5-羟甲基糠醛、丹参素、原儿茶醛、咖啡酸、苯甲酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸、甘草酸9种成分的含量。采用Phenomenex luna C18色谱柱(250 mm×4.6 mm,5 μm),以乙腈-0.05%三氟乙酸溶液为流动相进行梯度洗脱,流量为1 mL/min,柱温为25 ℃,检测波长分别为245 nm(苯甲酸、甘草酸)、280 nm(5-羟甲基糠醛、丹参素、原儿茶醛)和330 nm(咖啡酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸)。9种成分的质量浓度在各自范围内与对应的色谱峰面积线性关系良好,相关系数均为0.999 9,方法检出限为0.01~0.21 μg/mL,定量限为0.02~0.68 μg/mL。样品加标平均回收率为96.9%~105.0%,测定结果的相对标准偏差为1.3%~3.4%(n=6)。该方法简便可靠,重复性好,可用于晕可平糖浆的质量控制。
关键词: 晕可平糖浆; 指标成分; 高效液相色谱法
晕可平糖浆是由生赭石、夏枯草、法半夏、车前草4味中药组成的中药制剂,并加入矫味剂蔗糖、pH调节剂枸橼酸及抑菌剂苯甲酸钠,具有潜阳镇肝之功效,主治肝旺痰阻型的内耳眩晕症、头晕、目眩症。研究发现眩晕症多次发作后会影响大脑微循环,造成脑供血不足,而晕可平制剂能增强脑组织对缺血、缺氧的耐受力[1‒2]。处方中夏枯草含有酚酸类化合物丹参素、原儿茶醛、咖啡酸和迷迭香酸,这4种成分均具有抗脑缺血作用[3‒7];法半夏的入血成分有原儿茶醛和甘草酸[8],甘草酸对出血性、缺血性或缺血-再灌注性脑损伤以及化学品造成的神经损伤有显著保护作用[9];车前草含有咖啡酸、毛蕊花糖苷和异毛蕊花糖苷[10‒11],毛蕊花糖苷与异毛蕊花糖苷互为同分异构体,在煎煮或弱酸性条件下毛蕊花糖苷可转化为异毛蕊花糖苷,两者药理活性相似,均具有抗氧化和神经保护作用[12‒14]。
此外,糖浆的辅料主要有蔗糖、枸橼酸和苯甲酸钠。在酸性条件下,蔗糖溶液长时间高温加热或低温贮藏会产生5-羟甲基糠醛,且枸橼酸和晕可平糖浆中的金属离子Ca2+、Mg2+能加快蔗糖形成5-羟甲基糠醛的速率[15‒18]。5-羟甲基糠醛具有抗心肌缺血、改善血液流变性等作用,但同时也存在致突变性和遗传毒性等毒副作用,且毒性具有浓度依赖性效应[19]。另一辅料苯甲酸钠的用量不足会增加微生物污染的风险,使用过量存在蓄积毒性、生殖毒性、神经毒性和致突变的作用[20]。
晕可平糖浆现收载于《中华人民共和国卫生部药品标准》中药成方制剂第二册,标准号为WS3-B-0372-90,该标准仅有性状和检查项,无含量测定项。笔者等[21]曾对晕可平糖浆中迷迭香酸单一成分进行了测定,但单一指标的评价模式难以反映中药制剂整体质量,多指标成分测定已成为全面评价制剂质量的可靠模式[22],但目前尚未见同时测定晕可平糖浆中多种指标成分的方法。中药制剂中指标成分的测定方法主要有高效液相色谱法和液相色谱-串联质谱法。上述两种方法均具有高效、灵敏、准确、稳定的特点,其中高效液相色谱法具有操作简便、检测成本相对较低的优势,应用范围更广,因此笔者建立高效液相色谱法同时测定晕可平糖浆中5-羟甲基糠醛、丹参素、原儿茶醛、咖啡酸、苯甲酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸和甘草酸9种成分,以期为该制剂质量控制及临床疗效评价提供技术支持。
1、 实验部分
1.1 主要仪器与试剂
高效液相色谱仪:Agilent1260型,配二极管阵列检测器(DAD),安捷伦科技(中国)有限公司。
电子天平:XS205型,感量为0.01 mg,梅特勒-托利多仪器(上海)有限公司。
超纯水系统:Milli-Q Advantage A10型,默克化工技术(上海)有限公司。
超声波清洗器:B3200-T型,上海必能信超声有限公司。
5-羟甲基糠醛、丹参素钠、原儿茶醛、咖啡酸、苯甲酸钠、毛蕊花糖苷、迷迭香酸、甘草酸铵对照品:纯度(质量分数)分别为99.5%、97.8%、99.6%、99.7%、99.8%、95.2%、98.1%、96.2%,中国食品药品检定研究院。
异毛蕊花糖苷对照品:纯度(质量分数)为98%,成都克洛玛生物科技有限公司。
三氟乙酸、乙腈:色谱纯,美国TEDIA公司。
甲醇:色谱纯,国药集团化学试剂有限公司。
晕可平糖浆样品:共10批,批号分别为61200402、61200902、61201001、61201202、61210801、61220102、61220304、61220502、61220601、61221101,市售。
实验所用其他试剂均为分析纯。
实验用水为超纯水。
1.2 色谱条件
色谱柱:Phenomenex luna C18柱(250 mm×4.6 mm,5 μm,天津博纳艾杰尔科技有限公司);流动相:A相为乙腈,B相为0.05%(体积分数,下同)三氟乙酸溶液,流量为1 mL/min;洗脱方式:梯度洗脱,洗脱程序见表1;柱温:25 ℃;检测器:二极管阵列检测器(DAD);检测波长:苯甲酸、甘草酸为245 nm,5-羟甲基糠醛、丹参素、原儿茶醛为280 nm,咖啡酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸为330 nm;进样体积:10 μL。
表1 梯度洗脱条件
Tab. 1 Conditions of mobile phase in gradient elution
1.3 溶液制备
对照品储备液:精密称取各对照品适量,用75%(体积分数,下同)甲醇溶液溶解并稀释,配制成5-羟甲基糠醛、丹参素(以丹参素钠质量的0.9倍计)、原儿茶醛、咖啡酸、苯甲酸(由苯甲酸钠质量换算)、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸、甘草酸(由甘草酸铵质量换算)的质量浓度分别为1 354.20、2 262.99、1 744.00、1 138.57、16 578.82、1 060.53、981.96、4 228.11、730.90 μg/mL的对照品储备液。
混合对照品溶液:精密吸取适量各对照品储备液,置于同一只50 mL棕色容量瓶中,用75%甲醇溶液稀释至标线,配制成上述9种成分质量浓度分别为54.17、271.56、34.88、22.77、1 657.88、21.21、58.92、845.62、29.24 μg/mL的混合对照品溶液Ⅰ。另精密吸取适量各对照品储备液,置于同一只100 mL棕色容量瓶中,同法配制成上述9种成分质量浓度分别为2.71、108.62、14.82、10.82、795.78、14.85、53.03、105.70、6.58 μg/mL的混合对照品溶液Ⅱ。
系列混合对照品溶液:精密量取0.2、0.5、1、2.5、5、10 mL混合对照品溶液Ⅰ,分别置于6只10 mL棕色容量瓶中,用75%甲醇溶液稀释至标线,摇匀,得系列混合对照品溶液,9种成分的质量浓度见表2。
表2 系列混合对照品溶液9种成分的质量浓度
Tab. 2 Mass concentrations of 9 components in a series of mixed reference solutions ( μg/mL )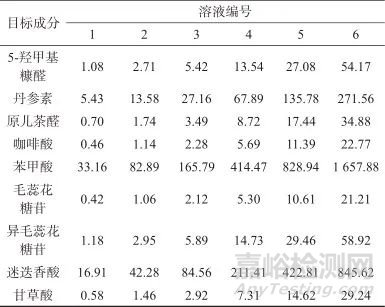
样品溶液:精密量取晕可平糖浆样品5 mL,置于25 mL棕色容量瓶中,加入75%甲醇溶液定容至标线,冰浴超声处理(功率为250 W,频率为33 kHz)5 min,用75%甲醇溶液定容至标线,摇匀,以0.45 μm微孔滤膜过滤,取续滤液,作为样品溶液。
阴性样品溶液:按照处方比例和制备工艺,分别制备不含夏枯草、不含法半夏、不含车前草、不含蔗糖和防腐剂的阴性样品,并按样品溶液制备方法同法制备阴性样品溶液。
1.4 实验方法
取混合对照品溶液Ⅰ和样品溶液,按1.2色谱条件进样测定,记录色谱图峰面积,以外标法计算样品中各指标成分的含量。
2、 结果与讨论
2.1 流动相选择
分别考察乙腈-0.1%甲酸溶液、乙腈-0.1%磷酸溶液、乙腈-0.05%三氟乙酸溶液、甲醇-0.05%三氟乙酸溶液4种流动相体系。结果发现,以乙腈-0.05%三氟乙酸溶液为流动相时,色谱图基线平稳、色谱峰形尖锐、对称,各目标成分的分离度符合要求;以其他3种溶液为流动相时,丹参素和迷迭香酸与前后杂质峰的分离度小于1.5,因此选择乙腈-0.05%三氟乙酸溶液作为流动相。
2.2 检测波长选择
采用DAD检测器在200~400 nm波长范围内对各成分进行扫描,5-羟甲基糠醛、丹参素、原儿茶醛、咖啡酸、苯甲酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸和甘草酸的最大吸收波长分别为284、280、280、322、230、330、326、330、252 nm。结合杂质干扰和指标成分灵敏度选择检测波长,确定苯甲酸、甘草酸的检测波长为245 nm,5-羟甲基糠醛、丹参素、原儿茶醛的检测波长为280 nm,咖啡酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸的检测波长为330 nm。
2.3 指标成分选择
根据《中华人民共和国药典》(2020年版)夏枯草、车前草的质量控制要求,选择糖浆中5-羟甲基糠醛、丹参素、原儿茶醛、咖啡酸、苯甲酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸、甘草酸和大车前苷10种成分进行测定。结果发现,糖浆中未检出大车前苷(检出限为0.02 μg/mL)。大车前苷属于苯乙醇苷类化合物,高温、高pH值、光照和金属离子会导致苯乙醇苷类成分降解[23],故推测大车前苷在制剂过程中发生降解,故选择5-羟甲基糠醛、丹参素、原儿茶醛、咖啡酸、苯甲酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸和甘草酸9种指标成分。
2.4 提取方法选择
分别考察冰浴超声和加热回流两种提取方式。结果发现,采用加热回流提取样品时,5-羟甲基糠醛的含量较高,与温度升高可促进5-羟甲基糠醛生成的文献报道一致[20],故选择冰浴超声提取法。
分别考察水、60%甲醇溶液、70%甲醇溶液、75%甲醇溶液、85%甲醇溶液、甲醇、75%乙醇溶液、乙醇8种溶剂的冰浴超声提取效果。结果表明,以75%甲醇溶液为溶剂时,毛蕊花糖苷和异毛蕊花糖苷的测定结果最大,各成分色谱峰形较好且杂质干扰小,故选择75%甲醇溶液作为溶剂。
以75%甲醇溶液为溶剂,分别考察超声时间为0、5、10、15、30 min时的提取效果[24‒26]。结果表明,各成分的提取效果无显著差异,为确保各成分充分溶解并节省实验时间,选择提取时间为5 min。
2.5 专属性试验
取混合对照品溶液Ⅰ、样品溶液、阴性样品溶液各10 μL,在1.2色谱条件下进样测定,可以看出,各成分色谱峰与相邻色谱峰分离度良好,样品基质无干扰,表明该方法专属性良好。
2.6 线性方程、检出限和定量限
按1.2色谱条件分别测定系列混合对照品溶液,以质量浓度为横坐标(x),以色谱峰面积为纵坐标(y)进行线性回归,得到线性回归方程及相关系数。将混合对照品溶液用75%甲醇溶液逐级稀释,按1.2色谱条件进样测定,以信噪比为3时的质量浓度为检出限,以信噪比为10时的质量浓度为定量限。9种成分的质量浓度线性范围、线性方程、相关系数、检出限和定量限见表3。由表3可知,各成分在各自质量浓度范围内与色谱峰面积线性关系良好。
表3 9种成分的质量浓度线性范围、线性方程、相关系数、检出限和定量限
Tab. 3 Linear range of mass concentration,linear equation,correlation coefficient,detection limit and quantification limit of 9 components

2.7 稳定性试验
按1.3方法制备样品溶液(批号为61200902),分别于第0、3、6、12、18、24 h时进样测定,结果见表4。由表4可知,5-羟甲基糠醛、丹参素、原儿茶醛、咖啡酸、苯甲酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸、甘草酸色谱峰面积测定结果的相对标准偏差(RSD)分别为1.0%、0.5%、1.4%、0.6%、0.6%、1.6%、0.8%、0.8%、1.2%,表明样品溶液在24 h内稳定性良好。
表4 稳定性试验结果
Tab. 4 Results of stability test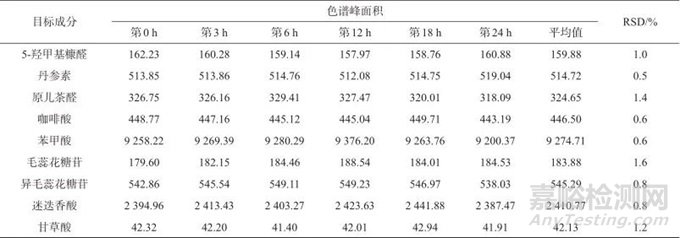
2.8 样品加标回收与精密度试验
取各成分含量已知的样品(批号为61200902) 6份,每份2.5 mL,精密加入10 mL混合对照品溶液Ⅱ,按1.3方法制备加标样品溶液,在1.2色谱条件下进样测定,计算回收率和测定结果的相对标准偏差,结果见表5。由表5可知,5-羟甲基糠醛、丹参素、原儿茶醛、咖啡酸、苯甲酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸、甘草酸的加标平均回收率分别为98.7%、105.0%、99.4%、100.1%、99.6%、103.9%、96.9%、101.2%、98.2%,测定结果的相对标准偏差分别为3.0%、1.6%、2.1%、2.0%、1.3%、2.5%、2.9%、3.1%、3.4%,表明该方法准确度和精密度较高。
表5 加标回收与精密度试验结果
Tab. 5 Results of spiked recovery and precision test
3、 结语
建立了高效液相色谱法同时测定晕可平糖浆中5-羟甲基糠醛、丹参素、原儿茶醛、咖啡酸、苯甲酸、毛蕊花糖苷、异毛蕊花糖苷、迷迭香酸、甘草酸9种成分的含量。该方法简便可靠,重复性好,可用于晕可平糖浆的质量控制,进而为其质量标准提高提供参考。
参考文献:
1 王秋月.眩晕症的病因分析及临床治疗[J].中国医药指南,2018,16(15):49.
WANG Qiuyue. Etiological analysis and clinical treatment of vertigo[J]. Guide of China Medicine,2018,16(15):49.
2 胡生俊.晕可平颗粒质量标准研究[J].亚太传统医药,2017,13(20):40.
HU Shengjun. Study on quality standard of Yunkeping granules[J]. Asia-Pacific Traditional Medicine,2017,13(20):40.
3 张金华,邱俊娜,王路,等.夏枯草化学成分及药理作用研究进展[J].中草药,2018,49(14):3 432.
ZHANG Jinhua,QIU Junna,WANG Lu,et al. Research progress on chemical constituents and pharmacological effects of Prunella vulgaris[J]. Chinese Traditional and Herbal Drugs,2018,49(14):3 432.
4 李占鹰,贾林,袁丽君,等.丹参素药理作用的研究进展[J].华西药学杂志,2021,36(5):600.
LI Zhanying,JIA Lin,YUAN Lijun,et al. Research progress on pharmacological effects of danshensu[J]. West China Journal of Pharmaceutical Sciences,2021,36(5):600.
5 杨世瑜,肖雨,安春娜,等.原儿茶醛的神经保护作用机制研究进展[J].中草药,2024,55(7):2 463.
YANG Shiyu,XIAO Yu,AN Chunna,et al. Research progress on neuroprotective mechanism of protocatechuic aldehyde[J]. Chinese Traditional and Herbal Drugs,2024,55(7):2 463.
6 商廿颍,李鑫楠,刘梦瑶,等.咖啡酸对于脑缺血损伤的保护作用及机制[J].中国药理学与毒理学杂志,2023,37(7):518.
SHANG Nianying,LI Xinnan,LIU Mengyao,et al. Protective effect and mechanism of caffeic acid on cerebral ischemic injury[J]. Chinese Journal of Pharmacology and Toxicology,2023,37(7):518.
7 刘勇,杨涛,梁艳山,等.迷迭香酸通过抑制ROS/NLRP-3炎症小体信号通路对脑缺血再灌注小鼠的保护作用[J].重庆医学,2023,52(19):2 905.
LIU Yong,YANG Tao,LIANG Yanshan,et al. Rosmarinic acid protected against brain injury in mice with cerebral ischemia reperfusion via oxidative stress and ROS/NLRP-3 signal pathway inhibition[J]. Chongqing Medical Journal,2023,52(19):2 905.
8 陶兴宝.法半夏炮制解毒机制、化痰效应及相关物质基础研究[D].南京:南京中医药大学,2022.
TAO Xingbao. Study on the detoxification mechanism by processing,phlegm-relieving effect and related material basis of Pinellae Rhizoma Praeparatum[D]. Nanjing:Nanjing University of Chinese Medicine,2022.
9 张明发,金玉洁,沈雅琴.甘草酸保护脑损伤及改善记忆功能的药理作用研究进展[J].药物评价研究,2013,36(1):59.
ZHANG Mingfa,JIN Yujie,SHEN Yaqin. Advances in pharmacologic study on encephalic injury protection and memory improvement of glycyrrhizic acid[J]. Drug Evaluation Research,2013,36(1):59.
10 许兵兵,黄碧涛,曾金祥,等.车前子及车前草中毛蕊花糖苷与异毛蕊花糖苷的含量比较[J].中国实验方剂学杂志,2016,22(18):64.
XU Bingbing,HUANG Bitao,ZENG Jinxiang,et al. Comparison of contents of verbascoside and isoverbascoside in Plantaginis Semen and Plantaginis Herba[J]. Chinese Journal of Experimental Traditional Medical Formulae,2016,22(18):64.
11 罗晶,李景辉.车前草中有机酸的含量测定[J].中国民族民间医药,2010,19(11):34.
LUO Jing,LI Jinghui. Content determination of organic acids in Plantaginis Herba by HPLC[J]. Chinese Journal of Ethnomedicine and Ethnopharmacy,2010,19(11):34.
12 田伟,甄亚钦,董秋菊,等.车前子煎煮过程中4种化学成分含量变化规律研究[J].中国新药杂志,2018,27(16):1 927.
TIAN Wei,ZHEN Yaqin,DONG Qiuju,et al. Variation of four chemical components in plantaginis semen during decoction process[J]. Chinese Journal of New Drugs,2018,27(16):1 927.
13 武改丽,霍志鹏,王玉,等. pH对毛蕊花糖苷稳定性影响及降解产物分析[J].中草药,2022,53(11):3 295.
WU Gaili,HUO Zhipeng,WANG Yu,et al. Effect of pH on tability of verbascoside and analysis degradation products[J]. Chinese Traditional and Herbal Drugs,2022,53(11):3 295.
14 谢良骐,柴智,弓强,等.毛蕊花糖苷对中枢神经系统的作用及其机制研究进展[J].中华中医药学刊,2024,42(7):179.
XIE Liangqi,CHAI Zhi,GONG Qiang,et al. Research progress on pharmacological effects and mechanism of acteoside on central nervous system diseases[J]. Chinese Archives of Traditional Chinese Medicine,2024,42(7):179.
15 丁爱华,潘富荣,谢斌,等.晕可平糖浆中19种无机元素的形态分析[J].药学与临床研究,2022,30(1):35.
DING Aihua,PAN Furong,XIE Bin,et al. Speciation analysis of 19 inorganic elements in Yunkeping Syrups[J]. Pharmaceutical and Clinical Research,2022,30(1):35.
16 张玉玉,张兴,章慧莺,等.双糖体系中5-羟甲基糠醛的形成动力学分析[J].食品工业科技,2014,35(3):93.
ZHANG Yuyu,ZHANG Xing,ZHANG Huiying,et al. Analysis of the formation kinetics on 5-hydroxymenthylfurfual in disaccharide system during thermal processing[J]. Science and Technology of Food Industry,2014,35(3):93.
17 LEE H S,NAGY S. Relative reactivities of sugars in the formation of 5-hydroxymethyl furfural in sugar-catalyst model systems[J]. Journal of Food Processing and Preservation,1990,14(3),171.
18 卢键媚,林晓蓉,陈忠正,等.反应条件对糖-酸反应体系中3-脱氧葡萄糖醛酮及5-羟甲基糠醛形成的影响[J].食品工业科技,2022,43(2):93.
LU Jianmei,LIN Xiaorong,CHEN Zhongzheng,et al. Effect of reaction conditions on the formation of 3-deoxyglucosone and 5-hydroxymethylfurfural in sugar-acid reaction system[J]. Science and Technology of Food Industry,2022,43(2):93.
19 关贵彬,张瑜,刘迪,等.中药与食品中共性成分5-羟甲基-2-糠醛的生物活性及其安全性研究进展[J].中国药师,2018,21(8):1 456.
GUAN Guibin,ZHANG Yu,LIU Di,et al. Research progress in biological activity and safety of 5-hydroxymethyl-2-furfural,a common component in traditional chinese medicine and food[J]. China Pharmacist,2018,21(8):1 456.
20 肖琦,赵培静,朱泽兵,等. HPLC同时测定舒肺糖浆中4种成分[J].中成药,2023,45(5):1 622.
XIAO Qi,ZHAO Peijing,ZHU Zebing,et al. Simultaneous determination of 4 constituents in Shufei Syrup by HPLC[J]. Chinese Traditional Patent Medicine,2023,45(5):1 622.
21 丁爱华,倪萍,支荣荣.晕可平糖浆的质量标准研究[J].首都食品与医药,2018,25(1):95.
DING Aihua,NI Ping,ZHI Rongrong,et al. Studies on the quality standard of Yunkeping Syrup[J]. Capital Food Medicine,2018,25(1):95.
22 唐乔. HPLC法测定百咳静颗粒中8个成分的含量[J].药物分析杂志,2021,41(1):147.
TANG Qiao. Simultaneous determination of eight components in Baikejing granules by HPLC[J]. Chinese Journal of Pharmaceutical Analysis,2021,41(1):147.
23 ZHOU Fei,ZHAO Yajin,LI Maiquan,et al. Degradation of phenylethanoid glycosides in Osmanthus fragrans Lour. flowers and its effect on anti-hypoxia activity[J]. Scientific Reports,2017,7(1):10 068.
24 何泽源,张妍妍,林楠,等. HPLC法同时测定复方活血胶囊中6种成分[J].中成药,2021,43(4):867.
HE Zeyuan,ZHANG Yanyan LIN Nan,et al. Simultaneous determination of six constituents in Compound Huoxue Capsules by HPLC[J]. Chinese Traditional Patent Medicine,2021,43(4):867.
25 曹旖岚,周露露,夏振江,等. HPLC法同时测定玉女煎中7种成分及化学计量学分析[J].中成药,2023,45(1):34.
CAO Yilan,ZHOU Lulu,XIA Zhenjiang,et al. Simultaneous determination of seven constituents in Yunv Decoction by HPLC[J]. Chinese Traditional Patent Medicine,2023,45(1):34.
26 杨欣怡,陈闪闪,戴国梁,等. HPLC法同时测定交泰丸水提液中7种成分[J].中成药,2023,45(1):40.
YANG Xinyi,CHEN Shanshan,DAI Guoliang,et al. Simultaneous determination of seven constituents in aqueous extract of Jiaoti Pills by HPLC[J]. Chinese Traditional Patent Medicine,2023,45(1):40.
引用本文: 丁爱华,吴士龙,葛玉松,等 . 高效液相色谱法同时测定晕可平糖浆中9种成分[J]. 化学分析计量,2024,33(9):49. (DING Aihua, WU Shilong, GE Yusong, et al. Simultaneous determination of 9 constituents in Yunkeping syrup by high performance liquid chromatography[J]. Chemical Analysis and Meterage, 2024, 33(9): 49.)

来源:化学分析计量
关键词: 晕可平糖浆