嘉峪检测网 2025-05-07 17:12
导读:本文深入探讨了胶囊用明胶生产企业中偏差管理的重要性、要求、常见问题以及优化策略,旨在为当前胶囊用明胶生产企业进行偏差管理提供方法。
本文深入探讨了胶囊用明胶生产企业中偏差管理的重要性、要求、常见问题以及优化策略,旨在为当前胶囊用明胶生产企业进行偏差管理提供方法。本文从国内现行法律法规对偏差管理的要求入手,基于行业现状分析了当下胶囊用明胶生产企业在偏差管理中面临的风险和挑战,并提出了相应的解决策略。同时,文章通过具体案例,详细介绍了胶囊用明胶生产企业在偏差管理中的关键内容。研究结果表明:对于胶囊用明胶生产企业而言,实施偏差管理规范可有效降低质量风险。最终的结论是:为了降低胶囊用明胶的质量风险,并确保生产出符合监管和注册要求、安全有效且质量可控的药品,企业应必须在预防偏差、偏差处理过程以及偏差后的管理这三个方面做好全面的偏差管理工作。
胶囊用明胶[1-2] 的质量直接关系到公众的健康和生命安全。在胶囊用明胶生产过程中,由于各种因素的影响,不可避免地会出现偏差。有效的偏差管理能够及时发现、评估、调查和处理这些偏差,从而降低胶囊用明胶质量风险,确保胶囊用明胶的质量和安全性。
随着胶囊用明胶监管的日益严格[3-6]、行业标准的不断提高以及客户要求的不断提升,胶囊用明胶生产企业对偏差管理的重视程度也越来越高。
1.偏差管理的术语和重要性
在探讨偏差管理的重要性之前,我们首先需要明确一些关键术语,这些术语是理解和实施偏差管理的基础。只有准确把握这些术语的含义,我们才能更好地理解偏差管理的重要性和作用。
1.1偏差管理的术语
接下来,我们将从偏差的定义和分类两个方面来详细阐述这些关键术语。
1.1.1 偏差的定义
偏差是指在胶囊用明胶生产、检验、储存、运输等过程中,任何偏离既定程序、标准、规范或预期结果的情况。
1.1.2 偏差的分类
根据偏差的性质和对胶囊用明胶产品质量的影响程度,可将偏差分为关键偏差、重大偏差和微小偏差[7]。
● 关键偏差:当偏差影响到胶囊用明胶的质量属性、关键工艺参数,或对过程和控制至关重要的设备或仪器时,可能会对人类健康产生影响,甚至威胁到生命安全,这种情况下,需要立即采取行动、进行调查,并由相应的标注操作程序(SOP)记录关键偏差[8];
● 重大偏差:当偏差影响到胶囊用明胶的质量属性、关键工艺参数,或对工艺或控制至关重要的设备或工具时,但不太可能对人类健康产生影响,此类偏差被归类为重大偏差。需要立即采取行动、进行调查,并由适当的作业程序进行记录;
● 微小偏差:当偏差不影响任何质量属性、关键工艺参数,或对过程和控制至关重要的设备或仪器时,将被归类为微小偏差,并按照适当的程序进行处理。
1.2偏差管理的重要性
偏差管理不仅能够保障产品质量,还能确保企业符合相关法规要求,并促进生产过程的持续改进。
1.2.1 保障胶囊用明胶质量
及时发现和处理偏差,防止不合格胶囊用明胶流入市场。
1.2.2 符合法规要求
胶囊用明胶监管机构要求企业建立有效的偏差管理体系,并将其作为《药品生产质量管理规范》《药用辅料生产质量管理规范》检查的重要内容。
1.2.3 促进持续改进
通过对偏差的分析和总结,发现生产过程中的薄弱环节,采取针对性的改进措施,不断优化生产工艺和质量管理体系。
2.偏差管理
所有胶囊用明胶生产企业都应建立《偏差管理程序》,以预防偏差的发生,并在出现偏差时进行有效处理和管理。偏差管理的详细内容请参见图1。
图1 偏差管理
2.1预防偏差的发生
各部门负责人需确保所有员工准确执行生产工艺、质量标准、检验方法和操作规程,以防止偏差的产生。因此,预防偏差的发生是偏差管理中至关重要的第一步[9]。
2.2偏差的处理
一旦发生偏差,必须按照《偏差管理程序》的规定进行处理。偏差处理的具体流程请参见图2。
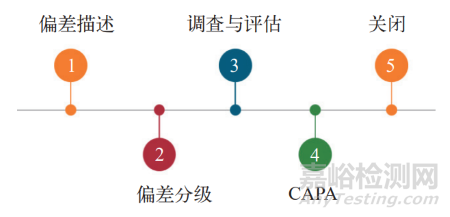
图2 偏差处理流程图
2.2.1 偏差的描述
工作过程中的任何员工都有责任发现偏差并及时向质量管理部门报告。
2.2.2 偏差的分级
对偏差的性质、范围以及对产品质量的潜在影响进行评估,以确定偏差的级别。
2.2.3 偏差的调查
成立专门的调查小组,制定调查计划,收集相关证据,并分析偏差产生的原因。
2.2.4 偏差的纠正和预防措施
根据调查结果,对产品采取相应的处理措施,如产品召回、返工、报废等;同时针 对偏差产生的根本原因,制定预防和纠正措施,以防止偏差的再次发生[10]。
2.2.5 偏差的关闭
对偏差处理、纠正和预防措施的执行情况进行跟踪和评估,确认偏差得到有效解决后,方可关闭偏差。
2.3偏差的管理
为确保产品质量和生产稳定性,我们采取了以下措施。
2.3.1 建立偏差台账
胶囊用明胶生产企业应建立偏差台账,用于管理重大偏差和关键偏差。
2.3.2 定期回顾和汇报
胶囊用明胶生产企业应按照既定的频次定期回顾偏差管理工作,并向企业高层管理者汇报。
3.偏差管理中常见的问题及其应对措施
关于偏差管理中常见的问题及其应对策略的详细信息,请参见表1。

表1 偏差管理中常见的问题及其应对措施
4.胶囊用明胶生产企业偏差管理的案例分析
胶囊用明胶生产企业根据客户需求,选择不同批次但质量指标相近的中间产品进行混合,以生产出成品。在包装完成后,产品需通过金属探测仪检查,确定产品中无超出探测精度的金属杂质。
为规范包装工序,胶囊用明胶企业制定了《包装工序管理制度》。接下来,本文将分享一起包装工序中出现的偏差案例,以及企业是如何处理和管理这一偏差的。
4.1偏差的处理
偏差的处理是一个系统化的过程,需要从多个方面进行详细的调查和分析,以确保问题得到彻底解决并防止再次发生。接下来,我们将通过一个具体的案例来展示偏差处理的全过程。
4.1.1 偏差描述
2020 年 3 月 10 日下午一点半,包装车间在包装批号为 200308 的成品时,操作工林某发现一袋产品在经过金属检测仪后,金属探测仪发出了报警信号[11]。
根据《包装工序管理制度》的规定,执行了纠正措施。发现这袋产品无法通过计划性偏差处理方法解决,于是立即通知了班长李某。李某随后向质量经理和 QA 主管报告了情况。
4.1.2 偏差分类
按照公司《偏差处理程序》,QA主管判定此偏差为重大偏差。
4.1.3 调查与评估
通过以下多方面的调查,我们逐步缩小了偏差发生的原因范围,最终确定了问题的根源。
●对操作人员的调查:操作工林某是公司的资深员工,在此岗位上已有10 年的工作经验,是一名熟练的操作工。
● 对设备的调查:将金属模块依次通过金属探测仪,结果显示金属探测仪对金属模块的报警反应正常。其他产品也依次通过金属探测仪,金属探测仪未发出报警,确认金属探测仪运行正常。
● 对产品的调查:当这袋产品通过金属探测仪时,探测仪报警,表明该产品内含有金属异物。
● 对方法的调查:产品通过金属探测仪的方式未发生改变。
● 对环境的调查:产品通过金属探测仪的环境(包装车间环境)未发生变化。
● 对测试的调查:金属探测仪的探测精度、灵敏性和电力系统均未发生变化。
拆开这袋产品的外包装袋后,更换为另一条外包装袋再次通过金属探测仪,金属探测仪未报警。而使用原来的外包装袋时,金属探测仪报警。由此确定金属异物不在内包装袋和产品中,而是在外包装袋中。
拆开这个外包装袋后,发现外包装袋内侧嵌有金属异物,确认这起金属异物是由外包装袋携带的。
回顾公司偏差数据库,确认产品外包装袋携带金属异物的情况是首次出现。QA 主管通过追溯,发现该包装袋是公司于 2019 年 12 月 24 日从 A 供应商处购入的10000条外包装袋中的1条。
在调查过程中,采用了鱼骨图分析法,并结合了“五个为什么”的方法进行深入分析。
4.1.4 制定纠正和预防措施
基于对问题的全面评估和风险考量,我们制定了以下纠正和预防措施,以防止类似情况再次出现。
4.1.4.1 制定纠正和预防措施
在发现外包装袋中含有金属异物,而内包装保持完好无损的情况下,经过风险评估,我们决定直接更换有问题的外包装袋,并将该产品与同批次其他产品一同入库。待产品通过指标检验并获得合格认证后,再进行发货处理。
QA 主管将外包装袋中发现金属异物的事件反馈给采购部门,采购部门随后向供应商提出投诉,并要求供应商采取改善措施,以从源头上加强质量管理。关于供应商的管理和评估,将另行分享。
QA 部门对《包装工序管理制度》进行了修订,新增了“在包装产品前,每个外包装袋必须先通过金属探测仪检查,确保外包装袋无金属异物后方可开始包装作业”的规定。文件修订和审批完成后,将对车间员工进行培训,并由车间执行新规定。
文件修改并培训完成后,班长李某负责组织车间员工执行新的操作要求。
4.1.4.2 建立行动计划表
采购部经理向供应商提出投诉,并要求供应商对此次事件进行原因分析,并制定相应的纠正和预防措施。供应商需在 2020 年 3 月 13 日前提供书面回复。我们设定了明确的截止日期,为 2020年 3 月 13 日。
QA 专员王某对《包装工序管理制度》进行了修改,增加了“包装车间在产品包装前,必须先使用金属探测仪检查每个外包装袋,确保外包装袋无金属异物后方可进行包装作业”的规定。文件修订、审批通过后,将对车间员工进行培训,并由车间执行新规定。我们设定了明确的截止日期,为 2020 年 3 月13 日。
班长李某在 QA 部门完成文件修改、审批和培训包装车间员工后,开始执行新的操作要求。我们设定了明确的截止日期,为 2020 年 3 月 16 日。
4.1.4.3 措施实施情况跟踪
2020 年 3 月 13 日,采购部收到供应商的书面回复后,立即转交给 QA 部门。QA 部门评估后认为供应商的原因分析、纠正和预防措施是可接受的。
2020 年 3 月 12 日,QA 部门完成了《包装工序管理制度》的修改,并在审核批准后立即对包装车间全体员工进行了培训。
2020 年 3 月 16 日,包装车间开始实施新规定,即在包装产品前,每个外包装袋必须先通过金属探测仪检查,确保了外包装袋无金属异物后方可进行包装操作。
4.1.4.4 效果验证
这批产品经过检验合格后,分别于 2020 年 3 月 30 日发给 A 客户 M 袋;2020 年 4 月 13 日发给 B 客 户 N 袋,包括更换外包装袋的产品。
从 2020 年 3 月 10 日 起 至 今, 数年时间已经过去,期间未再发生成品外包装袋检出金属异物的情况。因此,可以确认,针对此次偏差所采取的措施是有效的。
4.1.5 关闭
2020 年 4 月 10 日,确认所有措施均有效后,质量负责人在《偏差处理单》上做出最终结论,并签署关闭。按照公司《偏差处理程序》的规定,重大偏差和关键偏差均需要提交偏差报告。
2020 年 4 月 10 日,QA 主管依据偏差调查记录编写偏差报告,经质量负责人批准后,原件由 QA 保存,而复印件则转交至包装车间。
4.2偏差的管理
偏差管理是质量管理的重要组成部分,我们通过台账更新和定期汇报,确保偏差信息的透明化和可追溯性。
4.2.1 更新偏差管理台账和录入数据库
QA 主管于 2020 年 3 月 10 日更新了本工厂的偏差台账,并将此次偏差纳入其中。
2020 年 3 月 16 日,QA 主管在SharePoint 中更新了公司的偏差台账,并向事业部及总部提供。
2020 年 4 月 10 日,QA 主管再次更新了本工厂和 SharePoint 中的偏差台账状态。
4.2.2 偏差回顾和汇报
在 2021 年 1 月 19 日的公司管理层年度产品质量回顾及管理评审报告中,QA 将此次偏差情况一并汇报。
5.结 论
国内胶囊用明胶生产企业普遍也生产食品添加剂明胶,并已引入食品安全管理体系,按照 HACCP 原理进行风险管理,将偏差管理与风险管理紧密结合。
胶囊用明胶生产企业将偏差管理和风险管理结合在一起,制定偏差管理程序,并在培训后有效执行,以预防偏差的发生。一旦出现偏差,按照既定程序进行偏差处理和管理,确保偏差管理工作的有效性。
同时,胶囊用明胶生产企业应认识到偏差管理是一个持续改进的过程。企业应不断优化偏差管理体系,提升员工的质量意识和专业技能,加强与监管机构的沟通与合作,以适应日益严格的法规要求和市场竞争环境,确保为公众提供高质量、安全有效的胶囊用明胶。
参考文献
[1] 国家药典委员会 . 中华人民共和国药典:2020年版 四部[M].北京:中国医药科技出版社,2020: 720.
[2] 国家药品监督管理局 . 胶囊用明胶药用辅料标准草案公示稿[EB/OL].2024-07-03. https://www.cnppa.org/Public/editor/attached/file/20240703/20240703062715_59592.pdf#:~:text=%E9%99%84%E4%BB%B6:%E8%83%B6%E5%9B%8A%E7%94%A8%E6%98%8E%E8%83%B6%E8%8D%AF%E7%94%A8.
[3] 国家药品监督管理局 . 药品生产质量管理规范(2010 年修订)广告弗莱戈 PS25 04 药2 5484.indd 1 2025/4/27 11:18:29[S]. 卫生部令第 79 号,2011-01-17. https://www.samr.gov.cn/zw/zfxxgk/fdzdgknr/bgt/art/2023/art_d5e1dbaa8f284277a5f6c3e2fc840d00.html.
[4] 国家市场监督管理总局 . 药品生产监督管理办法 [EB/OL].2020-01-20. https://www.samr.gov.cn/zw/zfxxgk/fdzdgknr/fgs/art/2023/art_65070d0ee03a4109ac831ee7b3cee51c.html.
[5] 国家药品监督管理局综合司 . 药用辅料生产质量管理规 范( 征 求 意 见 稿 )[EB/OL].2022-05-09. https://www.nmpa.gov.cn/xxgk/zhqyj/zhqyjyp/20240718164243192.html.
[6] 国家食品药品监督管理局 . 关于加强胶囊剂药品及相关产品质量管理工作的通知 [EB/OL].2012-04-28. https://www.nmpa.gov.cn/directory/web/nmpa/xxgk/fgwj/gzwj/gzwjyp/20120428221801746.html#:~:text=%E8%8D%AF%E7%94%A8%E6%98%8E%E8%83%B6%E7%94%9F%E4%BA%A7%E4%BC%81%E4%B8%9A%E5%BA%94%E5%BD%93.
[7] 乔晓芳 . 浅析药品生产偏差管理进展及改进措施 [J]. 流程工业,2018(4): 24-27.
[8] 陈世鹏,陈世会 . 胶囊用牛骨明胶疯牛病的控制 [J]. 明胶科学与技术,2022, 42(2): 98-103.
[9] 郑文科,张磊 . 偏差流程要点分析和偏差处理成熟度的考量 [J].流程工业,2024(2): 20-24.
[10] 尚海宾,裴庆晗 . 浅析药品生产企业质量投诉管理体系的建立 [J].机电信息,2018(35): 1-5.
[11] 孙瑜 . 金属探测系统剔除装置的改 进 [J]. 中 国 科 技 信 息,2012,(09): 123.
本文作者常倩倩1、高斌2、张宁1、陈世会3、陈世鹏4,1. 河南医药健康技师学院;2. 上海雷允上药业有限公司;3. 甘肃省庆阳市正宁县西坡镇月明卫生院;4. 浙江金瑞薄膜材料有限公司,仅供交流学习。

来源:制药工艺与装备