嘉峪检测网 2025-06-12 20:19
导读:本文详细介绍了Omaveloxolone胶囊溶出区分力方法开发内容。
溶出数据显示,拟定的omaveloxolone胶囊,50毫克,在拟定溶出介质(即50 mol磷酸钠缓冲液中,pH值6.8,%1的SLS)中45min实现完全溶解。
2)溶出方法区分力
a)原料药粒径分布(PSD)的变化
申请人通过有意生产具有不同PSD原料药批次的制剂,研究了溶出方法对原料药粒度改变的区分力,如表6所示。溶出结果如图4所示,表明拟定溶出方法无区分PSD变化的能力。
表6: 无定型原料药变异PSD溶出区分力研究

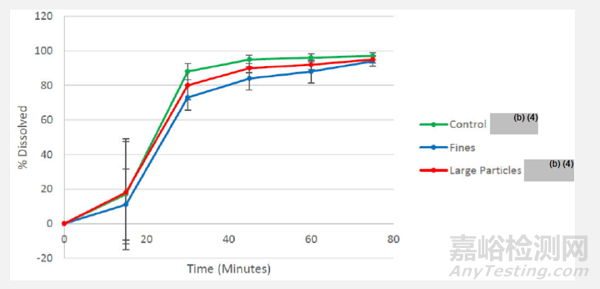
图4 Omaveloxolone胶囊的平均溶出曲线(N=18),50mg,无定型原料药粒度变化,在%1SLS的pH 6.8磷酸盐缓冲盐,100rpm转速
FDA审评:
Omaveloxolone是一种BCS IV类药物,具有中/高生物药剂学风险。FDA期望拟定溶出方法对关键物料属性(CMAs)和关键工艺参数(CPPs)具有一定的区分能力。期望该方法能够区分原料药PSD变化。然而,在上述研究中,拟定溶出方法并没有区分原料药粒径分布(PSD)变化。原因可能是三批次原料药之间的PSD差异不显著。在生物药剂学问询中,FDA进一步要求企业研究拟定溶出方法是否能区分原料药PSD的更大差异。
企业在回复FDA问询时阐述到,实际生产中,很难得到有巨大差异PSD的原料药,同时企业也同意修改原料药PSD接受标准,对D90限度进行修改,从NMT XXum 修改至NMT XXum。
c)处方变化
企业通过改变辅料的比例来特意生产以下批次,如表7. 对于这些批次,拟定的溶出方法没有展示出区分力,数据如图5.
表7:改变处方组成

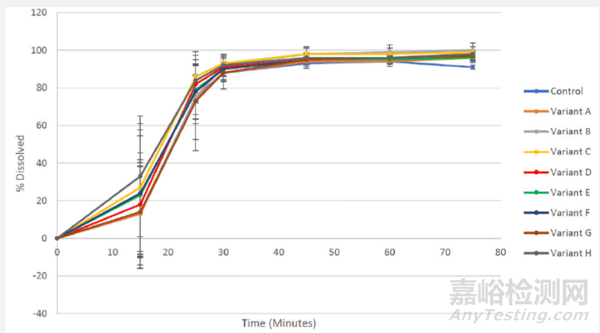
图5: Omaveloxolone 胶囊50mg规格平均溶解曲线(N=12),处方比例变化, 在1% SLS磷酸盐缓冲液pH 6.8,100 rpm转速
FDA审评意见:
由于原料药生产过程限制,企业无法得到在PSD上差异很大的不同批次制剂,以进一步研究拟定溶出方法的区分力。然而,拟定溶出方法的区分力(b)(4)当溶出接受标准为Q"= XX% XXmin" 修订为 Q"= XX% 45 min时,带有(b)(4)的批次将被拒绝,这将进一步减轻生物药剂学风险。总体而言,拟定溶出方法被认为是可以接受的。
2.溶出数据和接受标准
a)溶出数据
企业提供了10个临床批次和3个注册批次的详细信息和完整的溶出曲线数据(表8和表9)。
发现几乎所有溶出数据为6粒/批,而不是FDA要求的12粒/批的溶出数据。而且,不同批次有不同的取样时间点(比如,批170114的取样时间点:10,15,20,30,45,60min;批318136R的取样时间点:15,30,45,60min),这样的数据导致很难对比批间的溶出差异。企业对于生物药剂学IR1的回复,提供的数据见表10.
表8:所有临床批次和注册批次表
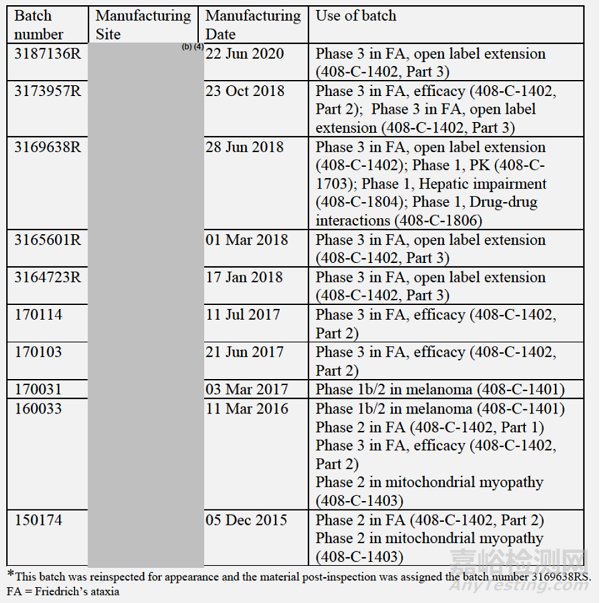
9:所有注册批次表
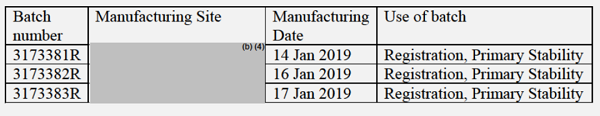
10:关键临床批次和注册批次平均溶出曲线数据(n=12)
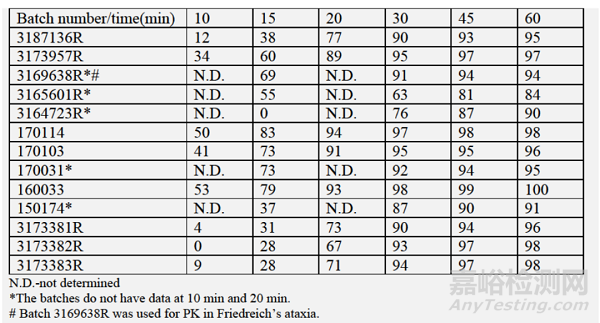
【解读】
对于具有BCS IV类特征的化合物,其具有中高生物药剂学风险,即溶出是否可以识别出那些不合格的批次样品。这些不合格的样品可能是不同工艺,或者不同CQA原料药生产得到的。FDA挑战了方法对原料药粒度的区分能力,但可惜的是,通过生产不同粒度原料药得到的制剂,溶出曲线没有表现出差异,即溶出方法对原料药粒度变化没有区分力。
企业通过变化处方中不同辅料比例得到的批次,拟定的溶出方法测试数据与不同粒度原料药一样,没有显示方法的区分力。FDA的审评意见中,可以看出溶出方法对某一参数或因素的变化,可以表现出区分力,通过修订Q值时间,区分出这些参数/因素变化的批次。
即使是BCS IV类化合物,拟定的溶出方法没有在原料药粒度或处方组成上表现出区分力,FDA在审评过程中提出了一些问询,但没有否定该溶出方法,而是希望企业提供更多的研究数据说明,以及体内的PK数据说明,拟定方法可以用于批次质量放行。
FDA指出企业提供的不同批次溶出数据有一些瑕疵,即取样时间点各有不同,无法进行批次之间的溶出曲线对比,这些批次中有用于确证性临床的,其溶出数据的对比对于溶出方法的拟定和接受标准拟定非常关键。

来源:蒲公英Ouryao
关键词: Omaveloxolone胶囊