嘉峪检测网 2019-10-14 09:12
导读:医药研发每天最新资讯汇总
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「本文共:16条资讯,阅读时长约:3分钟 」
今日头条
欧盟计划开展一项人造子宫研究。据媒体报道,欧盟“地平线2020计划”拟拨出一笔巨款(290万欧元,约合人民币2320万元)用于开展人造子宫研究。该研究将由荷兰埃因霍温理工大学、荷兰Máxima医疗中心联合开展。按照设计,这款人造子宫充满类似羊水的液体,自带血液循环系统。胎儿脐带会和人工胎盘相连,从而接受氧气和营养。此外,研究小组将在人造子宫上,安装各种传感器,模拟妈妈的体温、心跳。研究小组计划于2025年前完成相关试验并投入临床使用。
国内药讯
1.莎普爱思醋酸钠林格注射液获批上市。莎普爱思的醋酸钠林格注射液获国家药监局核发的《药品注册批件》。醋酸钠林格注射液用于补充体液,调节电解质平衡,纠正酸中毒。该原研产品由日本日研化学株式会社(2006年被兴和(株)收购)开发,商品名为“ヴィーン®F輸液”。目前,该品种国内获批的主要厂家有科伦药业、石药银湖制药、多瑞药业等。2018年醋酸钠林格注射液国内销售额约为19,435万元。
2.和铂医药干眼病滴眼液中国Ⅱ期临床结果积极。和铂医药引进品种全球创新药物HBM9036(tanfanercept)治疗中重度干眼患者的中国Ⅱ期临床达主要终点,与该药于美国开展的Ⅱ期临床(VELOS-1)结果一致。和铂医药将于2020年初开展HBM9036的Ⅲ期临床。HBM9036由HanAll公司开发,是一种经过分子工程改造的肿瘤坏死因子受体片段滴眼液。目前,HanAll正在全球开展该药物的Ⅲ期临床研究(VELOS-2)。
3.加科思1类新药JAB-3212国内进入临床。加科思启动1类新药JAB-3312治疗晚期实体瘤的中国I期临床。该研究旨在确定JAB-3312作为口服单药治疗晚期实体瘤的最大耐受剂量、II期研究推荐剂量、剂量限制性毒性以及安全性和耐受性,并初步探索JAB-3312的抗肿瘤作用。JAB-3312此前已在美获批临床,并于8月在Clinicaltrials登记首个人体I期剂量递增研究。9月29日,JAB-3312国内获批临床,适应症为治疗携带KRAS G12突变、BRAF Class3、NF1LoF、以及RTK突变、扩增或重排等基因型异常的实体瘤患者。
4.绿叶制药合作品种lurbinectin公布Ⅱ期临床数据。PharmaMar公司开发的抗肿瘤创新药lurbinectin(Zepsyre)治疗进展性恶性胸膜间皮瘤的Ⅱ期临床结果积极。52.4%的患者在用药12周时达到无进展生存期(PFS)的主要终点。Lurbinectedin是海鞘素衍生物,为RNA聚合酶II的抑制剂,此前FDA已受理其用于二线单药治疗小细胞肺癌的新药申请。绿叶制药通过授权获得其在中国开发及商业化的独家权利。目前在国家药监局官网尚未查到该产品更多信息。
5.信达生物与和黄医药合作信迪利单抗联用索凡替尼。信达生物与和黄中国医药宣布进一步拓展双方的全球临床合作,共同评估信达生物的重组全人源抗PD-1单克隆抗体达伯舒(信迪利单抗注射液)与和黄医药的索凡替尼联合治疗晚期实体瘤患者的安全性和有效性。索凡替尼是由和黄医药自主研发的一种新型的口服酪氨酸激酶抑制剂,具有抗血管生成和免疫调节双重活性。达伯舒和索凡替尼的联合疗法有望通过同时针对肿瘤微环境中的多种细胞类型和信号传导途径而带来协同的抗癌作用。据悉,新组合的临床研究将在美国和中国进行。
6.艾迪药业科创板IPO。艾迪药业拟IPO融资7.46亿元申请于科创板上市,保荐机构为华泰联合证券。艾迪药业成立于2009年,是一家致力于抗病毒、抗炎、抗肿瘤等药物研发、生产及销售的制药公司。此次融资中的59610万元将用于抗病毒、抗肿瘤领域新药研发及相关项目配套,进一步推进ACC007、ACC008、ACC006、ACC010四款在研新药的临床进程。该公司抗艾滋病新药ACC007是全新一代非核苷类逆转录酶抑制剂,目前处于Ⅲ期临床阶段,预计于明年上半年在中国递交新药上市申请。
国际药讯
1.礼来5-HT1F受体激动剂获FDA批准上市。礼来创新口服血清素(5-HT)1F受体激动剂Reyvow(lasmiditan)片剂获FDA批准作为急性疗法治疗有先兆或无先兆成年偏头痛患者。Reyvow也是获FDA批准的首款“地坦”(ditans)类药物。两项Ⅲ期临床(SAMURAI和SPARTAN)结果显示,与安慰剂组相比,Reyvow组受试者在服药2个小时后头痛完全消失的比例显著提高,Reyvow同时显著消除其它最困扰患者的偏头痛症状(恶心和声光敏感)。在对曲坦类药物反应不足的患者亚群中,Reyvow也能够产生良好的效果。
2.盐野义新型抗生素有望今年获批。盐野义开发的新型铁载体头孢菌素类抗生素药物cefiderocol在治疗医院获得性肺炎(NP)的Ⅲ期研究APEKS-NP中达主要终点。与接受高剂量meropenem治疗的活性对照组相比,cefiderocol在改良意向治疗(MITT)患者群中,在14天全因死亡率上达非劣效性标准——cefiderocol组的数值为12.4%,对照组为11.6%。在微生物学可评估患者群中,这一数据为12.4%(cefiderocol)比13%(对照组)。此外,cefiderocol还达多项关键性次要终点。此前,盐野义已向FDA递交cefiderocol的新药申请,有望在今年的11月份获批。
3.Horizon甲状腺眼病新药III期新数据出炉。Horizon 公司靶向抑制胰岛素样生长因子-1受体的IgG1单抗Teprotumumab公布验证性III期OPTIC试验的多个次要终点的新数据。与安慰剂相比,teprotumumab对活动性甲状腺眼病(TED)的几种破坏性影响有显著益处,包括复视(teprotumumab组有68%的患者复视程度较基线水平至少改善一级,安慰剂组比例为29%)、临床活动评分(CAS)(teprotumumab组有更多比例的患者CAS值达到0或1(59% vs 21%))等。目前,teprotumumab该适应症的上市申请正接受FDA的优先审查,预计2020年3月8日作出审查决定。teprotumumab有望成为首个TED治疗药物。
4.吉利德JAK1抑制剂展现长期疗效。吉利德与Galapagos公司联合开发的口服JAK1抑制剂filgotinib,在治疗中重度类风湿性关节炎(RA)的两项Ⅲ期临床(FINCH 1和FINCH 3)中获得的52周试验结果,支持filgotinib在此前公布的12周和24周数据中表现出的疗效、安全性和耐受性。此次获得的两项Ⅲ期试验完整数据是filgotinib在治疗不同类型的RA患者群体的试验结果。这些数据支持双方在年底之前向FDA递交新药申请。两项试验的52周数据将在未来的医学会议上公布。
5.尼达尼布治疗ILD获FDA突破性疗法认定。勃林格殷格翰小分子酪氨酸激酶抑制剂Ofev(尼达尼布,nintedanib)获FDA授予突破性疗法认定,用于治疗慢性进行性纤维化间质性肺病(ILD)患者。一项Ⅲ期临床INBUILD结果显示,在治疗52周后,Ofev将患者的肺功能下降幅度减少57%,达主要终点。此外,研究中Ofev延缓多种进行性纤维化间质性肺病患者的疾病进展速度。研究结果发表在《新英格兰医学杂志》(NEJM)上。Ofev于2014年已获批用于治疗特发性肺纤维化(IPF)患者。今年9月,Ofev还获FDA批准用于延缓系统性硬化症相关间质性肺病(SSc-ILD)成人患者的肺功能下降。
6.Frequency 创新再生疗法获FDA快速通道资格。Frequency 公司宣布,其拟用于促进听力恢复的在研药物FX-322获FDA授予快速通道资格,并在治疗感音神经性听力损失(SNHL)的Ⅱa期试验中实现首例患者给药。该研究将招募约96例SNHL患者,进行每周1次,共4次注射治疗。主要疗效终点是单词识别(WR),噪声中的单词识别(WIN)和标准纯音测听。已完成的Ⅰ/Ⅱ期研究结果显示,FX-322对听力功能,比如单词识别、声音的清晰度等有统计学意义的显著改善。
7.优时比收购Ra Pharma。优时比21亿美元收购Ra Pharmaceuticals公司。Ra Pharma公司拥有专有的大环肽合成技术平台ExtremeDiversity,专注于发现并开发靶向补体级联反应中关键组分的多肽和小分子疗法。Ra Pharma利用ExtremeDiversity平台开发的新型大环肽类C5补体抑制剂zilucoplan目前正被开发用于治疗全身型重症肌无力以及其他基于补体介导的罕见疾病。该在研疗法此前已获FDA授予治疗重症肌无力的孤儿药资格。根据协议,双方将继续推进zilucoplan在治疗重症肌无力(gMG)等罕见疾病方面的开发。
医药热点
1.首个脊髓性肌萎缩症治疗药物在全国开启患者治疗。渤健旗下诺西那生钠注射液在北京、上海等5个城市同步开启患者治疗。诺西那生钠注射液今年2月已获国家药监局批准用于治疗5q脊髓性肌萎缩症(SMA)患者,这也是中国首个获批治疗SMA的药物。据悉,该药物在中国的治疗费用一针接近70万,第一年年治疗费用约420万,后续维持一年210万。目前该药的援助项目也已启动,预计在全国14个省市范围开展,援助主要分为负荷剂量的援助和维持剂量援助,即使患者参加援助项目,一年治疗费用也需140万左右,后续一年100万左右。
2.国家卫健委:开展老年人友善医疗机构创建活动。国家卫健委老龄健康司司长王海东在11日的例行新闻发布会上表示,国家卫健委将推动各级医疗卫生机构开展适老化改造,开展老年友善服务,增加老年人就医便利程度;推动建立包括健康教育、预防保健、疾病诊治、康复护理、长期照护和安宁疗护六个环节的覆盖城乡、综合连续的老年健康服务体系;加强医养结合机构本身的质量管理,并于近期出台医养结合服务机构的管理指南和服务指南。
【迪瑞医疗】公司产品全自动尿液有形成分分析仪、全自动干化学尿液分析仪申报医疗器械注册获得受理。
审评动向
1. CDE最新受理情况(10月13日)
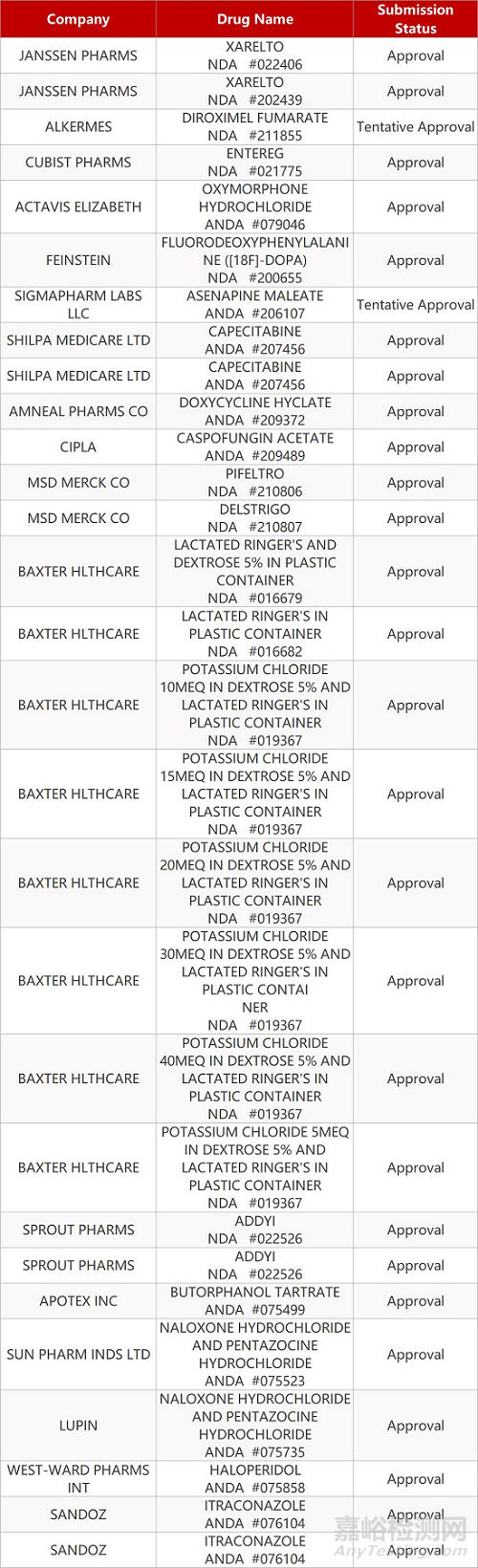
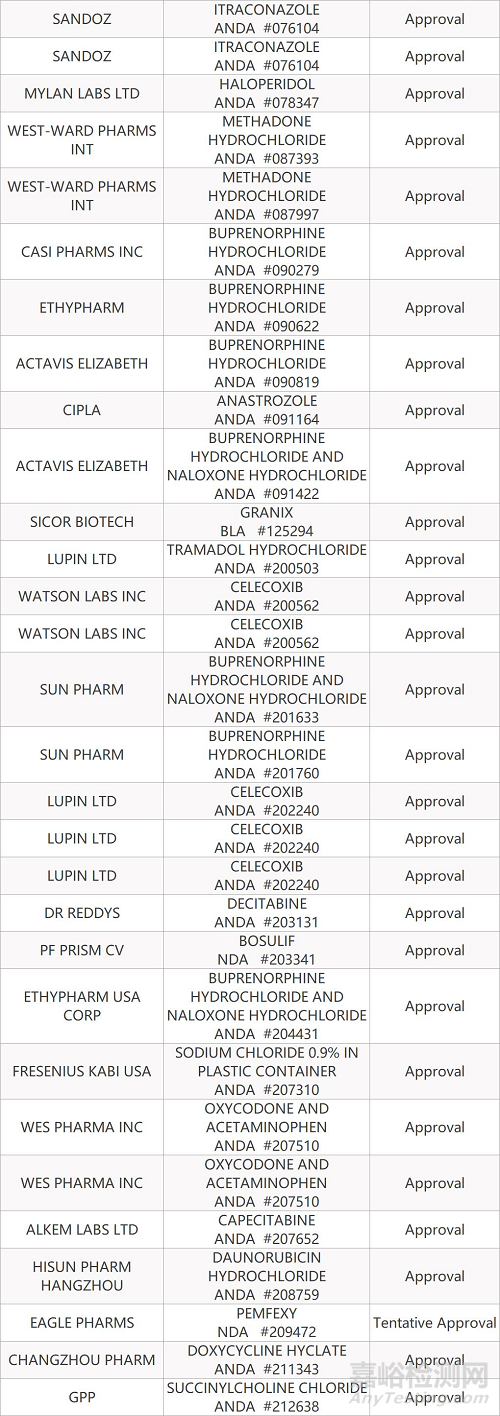
2. FDA最新获批情况(北美10月12日)


来源:药研发