嘉峪检测网 2024-10-11 20:15
导读:建立气相色谱-质谱法检测帕瑞昔布钠原料药及注射用帕瑞昔布钠中硫酸二甲酯、硫酸二乙酯和硫酸二异丙酯。
摘 要: 建立气相色谱-质谱法检测帕瑞昔布钠原料药及注射用帕瑞昔布钠中硫酸二甲酯、硫酸二乙酯和硫酸二异丙酯。用Thermo TG-5MS毛细管色谱柱(30 m×0.25 mm,0.25 μm)分离,载气为氦气,质谱离子源为电子轰击离子源,采集模式为定时选择性离子监测。3种硫酸酯质量浓度在各自范围内与色谱峰面积线性关系良好,相关系数均大于0.995,平均回收率为95.60%~107.3%,测定结果的相对标准偏差均小于5%(n=6),检出限为20.50~21.88 ng/mL,定量限为61.50~65.64 ng/mL。该法可用于帕瑞昔布钠原料药及注射用帕瑞昔布钠中3种硫酸酯类基因毒性杂质的检测。
关键词: 气相色谱-质谱法; 帕瑞昔布钠; 注射用帕瑞昔布钠; 硫酸酯类; 基因毒杂质
帕瑞昔布钠化学名为N-{[4-(5-甲基-3-苯基-4-异恶唑基)苯基]磺酰基}丙酰胺钠盐,是瑞典法玛西亚公司研发的首个可静脉注射给药和肌肉注射的可选择性抑制环氧化酶-2(COX-2)抑制剂,能抑制前列腺素合成,降低外周与中枢敏化[1],临床主要用于手术后的短期治疗[2‒4]。帕瑞昔布钠的合成工艺路线如图1所示。该线路是以5-甲基-3,4-二苯基异恶唑[5‒7]为起始物料,依次与氯磺酸和氨水反应生成,中间体1与丙酐在硫酸作用下反应生成帕瑞昔布,再经氢氧化钠乙醇溶液中成盐得帕瑞昔布钠。在其制备过程中,步骤1用到氯磺酸,与后续工艺中用到的甲醇可能会生成具有基因毒警示结构杂质硫酸二乙酯,由于乙醇中可能含有甲醇、异丙醇杂质,还可能产生硫酸二甲酯、硫酸二异丙酯;在步骤2中残留的硫酸同样会与甲醇、乙醇、异丙醇生成硫酸二甲酯、硫酸二乙酯和硫酸异丙酯如图2所示。
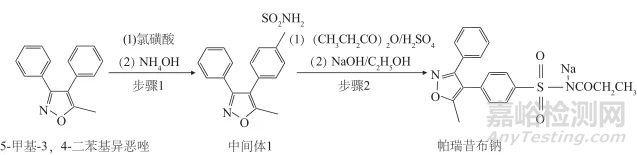
图1 帕瑞昔布钠的合成工艺路线
Fig. 1 The synthesis process route of Parexib sodium
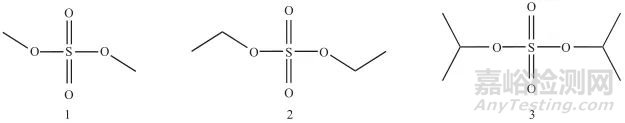
1—硫酸二甲酯;2—硫酸二乙酯;3—硫酸二异丙酯图2 3种硫酸酯基因毒杂质的化学结构式
Fig. 2 Chemical structural formulas of three sulfates genotoxic impurities
人用药品技术要求国际协调理事会(ICH)M7(R2)指导原则指出硫酸二甲酯是一种致突变性致癌物。在体内,硫酸二甲酯可使脱氧核糖核酸(DNA)甲基化,并且遗传毒性检测始终呈阳性。硫酸二甲酯虽然被国家癌症机构(IARC)列为2 A类致癌物质,但尚未有口服致癌研究数据用以推导半数致死量(TD50)及可接受摄入量(AI),因此将硫酸二甲酯的终生可接受摄入量定在1.5 μg/d的毒理学关注阈值(TTC)。硫酸二乙酯与硫酸二异丙酯的毒性均低于硫酸二甲酯,因此均按1.5 μg/d的限度进行控制[8‒10]。
目前关于硫酸酯相关检测在空气[11‒12]、土壤[13]、纺织品[14]、化妆品[15]以及药物[16‒19]等领域已有文献报道,采用的方法主要有气相色谱(GC)法、液相色谱-质联用(LC-MS/MS)法、气相色谱-质谱联用(GC-MS)法等。朱长友等[19]采用气相色谱-质谱法对塞来昔布原料药中硫酸酯类基因毒性杂质进行了测定,但尚未见关于帕瑞昔布钠及注射用帕瑞昔布钠冻干粉末中硫酸酯类化合物的相关研究。
帕瑞昔布钠虽与塞来昔布同属于COX-2强效特异性抑制剂,但是帕瑞昔布钠是伐地昔布的前体药物,需要在体内代谢水解为伐地昔布发挥镇痛作用[20]。针对帕瑞昔布钠盐和注射用帕瑞昔布钠冻干粉末制剂的特性,笔者筛选出对帕瑞昔布钠盐有高溶解度且稳定性好的提取溶剂甲醇-四氢呋喃(体积比为5∶95),对帕瑞昔布钠和注射用帕瑞昔布钠冻干粉末中的硫酸酯进行提取,采用外标法以气相色谱-质谱法同时测定硫酸二甲酯、硫酸二乙酯、硫酸二异丙酯的含量,系统平稳、快速,分析时间仅需8.5 min,该方法实现了快速、灵敏、准确的分析,为帕瑞昔布钠原料药及注射用帕瑞昔布钠制剂中硫酸酯类基因毒性杂质的潜在风险和安全性评价提供方法参考。
1、 实验部分
1.1 主要仪器与试剂
气相色谱-质谱联用仪:Trace1300 GC-ISQ 7000型,配电子轰击源(EI),美国赛默飞世尔科技公司。
电子分析天平:QUINTIX35-1CN型,感量为0.01 mg,赛多利斯科学仪器(北京)有限公司。
离心机:DMO412型,美国赛洛捷克有限公司。
四氢呋喃、甲醇:均为色谱纯,德国默克化学试剂公司。
硫酸二甲酯、硫酸二乙酯、硫酸异丙酯:纯度(质量分数)均为99%,上海贤鼎生物科技有限公司。
帕瑞昔布纳原料药样品:共3批样品,批号分别为220101、220105、220106,江苏省药物研究所有限公司。
注射用帕瑞昔布钠样品:规格为40 mg,批号分别为220814、220914、221014,江苏省药物研究所有限公司。
1.2 仪器工作条件
1.2.1 色谱仪
色谱柱:Thermo TG-5 MS毛细管柱(30 m×0.25 mm,0.25 μm,美国赛默飞世尔科技公司);程序升温:初始温度为60 °C,保持5 min,以30 °C/min升至240 °C,保持1 min;进样口温度:180 °C;载气:高纯氦气;分流流量:10 mL/min;柱流量:1.0 mL/min;分流比:10∶1;进样体积:3 μL;进样方式:直接进样。
1.2.2 质谱仪
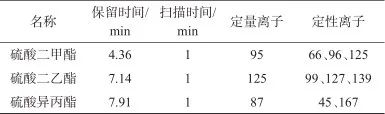
离子源:电子轰击离子源(EI);电压:负70 eV;传输线温度:250 °C;离子源温度:280 °C;采集方式:定时选择性离子监测(T-SIM);采集时间:±1 min;3种硫酸酯特征离子和质谱参数见表1。
表1 3种硫酸酯特征离子和质谱参数
Tab. 1 Characteristic ions and mass spectrometry parameters of three sulfates
1.3 溶液的配制
空白溶剂:甲醇与四氢呋喃(体积比为5∶95,下同)的混合溶液。
混合对照品储备溶液:精密称取硫酸二甲酯、硫酸二乙酯、硫酸二异丙酯对照品各50 mg,置于100 mL量瓶中,加甲醇-四氢呋喃(5∶95)溶解稀释定容至标线,摇匀。
混合对照品溶液:精密量取对照品储备溶液1 mL,置于10 mL量瓶中,甲醇-四氢呋喃(5∶95)定容至标线,摇匀。
帕瑞昔布钠原料样品溶液:精密称取帕瑞昔布钠原料细粉适量(相当于帕瑞昔布225 mg),置于20 mL量瓶中,加甲醇-四氢呋喃(5∶95)快速振摇分散溶解,并定容至标线,摇匀。
注射用帕瑞昔布钠样品溶液:取注射用帕瑞昔布纳样品10 支,每支以3 mL甲醇-四氢呋喃(5∶95)溶液复溶后,合并混匀,以3 500 r/min转速离心5 min,取上清液,待测。
1.4 实验方法
精密量取硫酸酯对照品溶液、帕瑞昔布钠原料样品溶液、注射用帕瑞昔布钠样品溶液各3 μL,分别注入气相色谱质谱联用仪,记录色谱图,量取色谱图峰面积,按照外标法计算样品中目标化合物的含量。
2、 结果与讨论
2.1 色谱条件的优化
2.1.1 进样口温度的选择
硫酸二甲酯、硫酸二乙酯和硫酸二异丙酯3种硫酸酯的沸点均在180~236 ℃范围内,帕瑞昔布钠的熔点在273~275 °C范围内。比较进样口温度分别为180、200、220 ℃条件下,对照品和样品溶液的出峰情况。经试验对比发现,进样口温度越高,则待测物质的灵敏度越高,随之样品本底质谱干扰增加,因此最终选择进样口温度为180 ℃,以减少基体的质谱干扰。
2.1.2 分流比的选择
分流比是影响目标物质出峰情况的主要因素。分流比高峰形尖锐不拖尾,但会引起待测物质灵敏度下降。对比分流比分别为5∶1、10∶1、15∶1、20∶1条件下,对照品溶液的出峰情况。试验结果表明,分流比高目标化合物响应降低,当分流比为5∶1时硫酸二甲酯峰形较差,综合考虑峰形和检测灵敏度,确定最优分流比为10∶1。
2.2 溶剂的选择
分别选取乙腈、N,N-二甲基甲酰胺、甲醇、四氢呋喃作为溶剂,考察帕瑞昔布钠在4种溶剂中的溶解度,以及3种硫酸酯在各溶剂中的稳定性。试验结果表明,帕瑞昔布钠在乙腈中完全不溶解,在四氢呋喃中的溶解度较差;帕瑞昔布钠在N,N-二甲基甲酰胺中的溶解度较好,但硫酸酯在碱性有机溶剂N,N-二甲基甲酰胺中易降解,稳定性差;帕瑞昔布钠在甲醇中的溶解度较好,但硫酸二甲酯在甲醇中不稳定。确定溶剂为甲醇与四氢呋喃的混合溶剂(体积比为5∶95),这样既能满足帕瑞昔布钠的溶解度达到限定要求,又能保证硫酸酯类化合物在混合溶剂中的稳定性,因此选择甲醇-四氢呋喃(5∶95)作为溶剂。
2.3 质谱参数优化
2.3.1 传输线温度与离子源温度选择
帕瑞昔布钠和注射用帕瑞昔布钠样品溶液直接进样,大部分样品基质停留在进样口的玻璃衬管中,还有部分物质产生汽化进入质谱,可能产生质谱干扰,提高传输线温度至250 ℃,提高离子源温度至280 ℃,可以提高检测灵敏度,降低样品本底产生的质谱检测器干扰,也可以保持离子源的清洁和高灵敏度。
2.3.2 质谱检测器离子监测模式的选择
选择Thermo ISQ7000独有的定时选择性离子监测(T-SIM)功能,无需对3种硫酸酯进行分段扫描,仪器可根据目标化合物保留时间自动进行扫描。在特定的时间段,只扫描特定的特征离子,质谱检测器会自动优化每一个特征离子的驻留时间,背景更低,专属性更强。
2.4 专属性试验
分别精密量取空白溶液、对照品溶液、帕瑞昔布钠原料样品溶液、注射用帕瑞昔布钠样品溶液各3 μL,在1.2 仪器工作条件下进样并测定,色谱图如图3所示。由图3可知,空白溶剂对硫酸二甲酯、硫酸二乙酯、硫酸二异丙酯测定无干扰,表明方法专属性良好。
图3 溶液色谱图
Fig. 3 Solution chromatogram
1—硫酸二甲酯; ;2—硫酸二乙酯;3—硫酸二异丙酯
2.5 线性关系和检出限
取对照品溶液,加甲醇-四氢呋喃(5∶95)稀释,在1.2 仪器工作条件下进样测定,以信噪比为3时 对应的质量浓度为检出限,以信噪比为10时对应的质量浓度为定量限。精密量取硫酸二甲酯、硫酸二乙酯、硫酸二异丙酯加甲醇-四氢呋喃(5∶95)稀释制成各浓度均约为10 μg/mL的储备溶液;再分别精密量取上述对照品储备溶液0.6、1.0、2.0、3.0、4.0 mL于100 mL量瓶中,加甲醇-四氢呋喃(5∶95)稀释至标线,摇匀,制成硫酸二甲酯、硫酸二乙酯、硫酸二乙丙酯的质量浓度均分别为60、100、200、300、400 ng/mL系列标准工作溶液,依法进样,记录质谱图。以3种硫酸酯的质量浓度(x)为横坐标,其色谱峰面积(y)为纵坐标进行线性回归,3种硫酸酯类化合物的线性范围、线性方程、相关系数、检出限和定量限见表2。
表2 3种硫酸酯的线性范围、线性方程、相关系数、检出限和定量限
Tab. 2 Linear equation,correlation coefficient, detection limit and quantification limit of three sulfates

由表2可知,3种硫酸酯的质量浓度在各自范围内与质谱峰面积具有良好的线性关系,线性相关系数均大于0.995,表明该方法检出限和定量限均满足检测要求,灵敏度较高。
2.6 加标回收与精密度试验
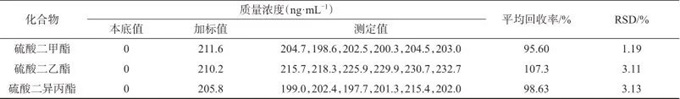
精密称取帕瑞昔布钠原料药225 mg,置于20 mL量瓶中,加含硫酸二甲酯、硫酸二乙酯和硫酸二异丙酯混合对照溶液(2 μg/mL)2.0 mL,加甲醇-四氢呋喃(5∶95)快速振摇溶解,并定容至标线,摇匀,作为帕瑞昔布钠原料加标样品溶液,平行配制6份,依法测定,试验结果见表3。由表3可知,3种硫酸酯化合物在帕瑞昔布钠原料样品的平均加标回收率为95.60%~107.3%,测定结果的相对标准偏差均小于5%(n=6),满足技术要求,表明该方法准确度、精密度良好。
表3 帕瑞昔布钠原料样品加标回收与精密度试验结果
Tab. 3 Recovery and precision test results of Parecxib sodium with spiking
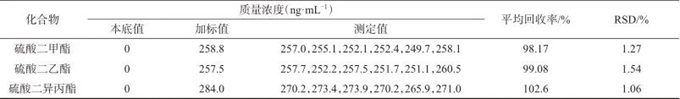
取注射用帕瑞昔布钠样品10支,每支分别以含硫酸二甲酯、硫酸二乙酯和硫酸二异丙酯混合对照溶液(250 ng/mL)3.0 mL复溶,合并溶液,离心,取上清液作为注射用帕瑞昔布钠加标样品溶液,平行配制6份,依法测定,试验结果见表4。由表4可知,3种硫酸酯化合物在注射用帕瑞昔布钠制剂样品的平均加标回收率为98.17%~102.6%,测定结果的相对标准偏差均小于5%(n=6),满足技术要求,表明该方法准确度、精密度良好。
表4 注射用帕瑞昔布钠样品加标回收与精密度试验结果
Tab. 4 Recovery and precision test results of Parecxib sodium for injection with spiking
2.7 溶液稳定性试验
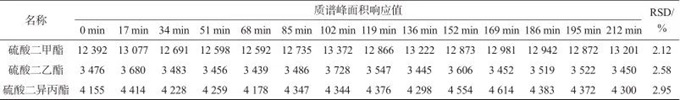
取质量浓度为200 ng/mL的混合对照品溶液在避光且室温低于20 ℃环境条件下,分别连续进样14针,每针进样间隔17 min,记录质谱图,量取峰面积见表5。由表5可知,212 min内测定结果的相对标准偏差为2.12%~2.95%,说明3种硫酸酯在避光且低于20 ℃环境条件下,于甲醇-四氢呋喃(5∶95)溶剂中3.5 h内稳定。
表5 3种硫酸酯溶液稳定性试验结果
Tab. 5 The stability results of 3 sulfates solution
2.8 安全性评价
3种硫酸酯均具有较强基因毒性和致癌性,但尚未有口服致癌研究数据用于推导AI限量,根据ICH M7(R2)指导原则以1.5 μg/d作为单个硫酸酯类基因毒杂质的限度,查阅注射用帕瑞昔布钠说明书,用于手术后疼痛的短期治疗时每天总剂量不超过80 mg,基于每日最大用量计算帕瑞昔布钠原料药中硫酸酯类化合物的限度为18.75 μg/g,注射用帕瑞昔布钠(规格为40 mg)冻干粉末中硫酸酯类化合物的限度为0.75 μg/支。
按照1.2仪器工作条件对自制帕瑞昔布钠原料药和注射用帕瑞昔布钠中硫酸二甲酯、硫酸二乙酯、硫酸二异丙酯进行检测。结果显示帕瑞昔布钠原料药中3种硫酸酯的检出量均小于0.09 μg/g,注射用帕瑞昔布钠冻干粉末中3种硫酸酯的检出量均小于0.006 μg/支,3个硫酸酯的检出量均低于硫酸酯类基因毒杂质限度水平的30%,说明自制的帕瑞昔布钠原料和制剂产品不会产生显著的硫酸酯类基因毒杂质安全风险,该试验结果可作为产品风险分析的参考依据。
3、 结语
建立了气相色谱-质谱联用同时检测帕瑞昔布钠原料药和注射用帕瑞昔布钠制剂中硫酸二甲酯、硫酸二乙酯和硫酸二异丙酯的方法,筛选出甲醇-四氢呋喃(5∶95)混合溶剂,既可以保证原料药的溶解度提高进样浓度提高检测灵敏度,又可以去除注射剂辅料引起的质谱干扰,采用了定时选择性离子监测模式进行测定,使该方法具有较高的检测灵敏度和良好的专属性,操作简便快速,3种硫酸酯的检出限均低于单个硫酸酯类基因毒杂质限度水平30%,该方法可满足帕瑞昔布钠和注射用帕瑞昔布钠中痕量硫酸酯类化合物的检测要求,可应用于帕瑞昔布钠和注射用帕瑞昔布钠中硫酸酯类基因毒杂质监控和安全性评价。
参考文献:
1 李蓓蓓,王力甚.帕瑞昔布钠在围术期中应用的研究进展[J].巴楚医学,2020,3(4):117.
LI Beibei,WANG Lishen . Research progress on the application of Parexib sodium in the perioperative period [J].Bachu Medical Journal,2020,3(4):117.
2 萧红燕,傅丹云,贾继娥.对比分析3种非甾体类药物在耳内镜手术中的镇痛效果[J].复旦学报(医学版),2022,49(1):94.
XIAO Hongyan,FU Danyun,JIA Ji'e. Comparison of the analgesic effect of three nonsteroidal drugs in otoendoscopic surgery [J]. Fudan University Journal of Medical Sciences,2022,49(1):94.
3 武若杰,刘睿,张一粟,等.帕瑞昔布钠改善腹腔镜下直肠癌根治术患者的炎症微环境并促进患者恢复:基于下调CXCL8-CXCR1/2表达 [J]. 南方医科大学学报, 2024, 44(2):363.
WU Ruojie, LIU Rui,ZHANG Yisu, et al. Parecoxib sodium down-regulates CXCL8-CXCR1/2 to improve inflammatory microenvironment and promote patient recovery following laparoscopic radical resection of rectal cancer[J].Journal of Southern Medical University, 2024, 44(2):363.
4 赵琦, 付莉莉, 刘晓云, 等. 帕瑞昔布钠用于乳腺癌改良根治术超前镇痛的临床研究[J]. 中国临床药理学杂志, 2024, 40(1):7.
ZHAO Qi,FU Lili,LIU Xiaoyun, et al. Clinical trial on preemptive analgesia of parecoxib sodium for modified radical resection of breast cancer[J]. The Chinese Journal of Clinical Pharmacology,2024,40(1):7.
5 沈晓敏.帕瑞昔布钠原料药的质量标准研究[D]. 南京:南京师范大学,2018.
SHEN Xiaomin. Study on the quality standards of parexib sodium API [D]. Nanjing:Nanjing Normal University,2018.
6 刘彦龙,胡中元,邢磊,等.帕瑞昔布钠的合成工艺改进[J].中国医药工业杂志,2019,50(2):182.
LIU Yanlong, HU Zhongyuan, XING Lei, et al. Improved synthesis of parecoxib sodium[J].Chinese Journal of Pharmaceuticals,2019, 50(2):182.
7 王凯,宋率华,金琪,等.帕瑞昔布钠合成路线图解[J].中国医药工业杂志,2013,44(8):836.
WANG Kai, SONG Shuaihua, JIN Qi, et al. Graphical synthetic routes of parecoxib sodium[J]. Chinese Journal of Pharmaceuticals, 2013,44(8):836.
8 ICH HARMONISED GUIDELINE. Assessment and control of dna reactive ( mutagenic) impurities in pharmaceuticals to limit potential carcinogenic risk M7( R2) [Z]. 2023-04-03.
9 EICHLER D R, PAPADANTONAKIS G A. Activation barriers for methylation of DNAbases by dimethyl sulfate [J]. Chemical Physics Letters, 2017, 689:8.
10 CHADT J, SYKORAD, NILSSON R, et al. Monitoring of dimethyl sulphate-induced N3-methyladenine,N7-methylguanine and O6-methylguanine DNA adducts using reversed-phase high performance liquid chromatography and mass spectrometry[J]. Journal of Chromatography B, 2008, 867(1):43.
11 张耕,许兵,梅勇.柱前衍生气相色谱法测定工作场所空气中的硫酸二甲酯[J].现代预防医学,2018,45(12):2 137.
ZHANG Geng, XU Bing, MEI Yong. Determination of dimethylsulfate in workplace air by gas chromatography with precolumn derivatization[J]. Modern Preventive Medicine, 2018,45(12):2 137.
12 李小娟,马永建.工作场所空气中硫酸二甲酯的气相色谱快速测定[J].中国工业医学杂志,2010,23(4):301.
LI Xiaojuan,MA Yongjian. Rapid determination of dimethyl sulfate in air of work place with gas chromatography[J]. Chinese Journal of Pharmaceuticals,2010,23(4):301.
13 冯萌萌,王虹,陈佩瑾.气相色谱-质谱法测定土壤中硫酸二甲酯和硫酸二乙酯的残留量[J].广东化工,2020,47(9):186.
FENG Mengmeng, WANG Hong, CHEN Peijin, et al.Determination of dimethyl sulfate and diethyl sulfate residues in soil by gas chromatography-mass spectrometry[J].Guangdong Chemical Industry,2020,47(9):186.
14 林君峰,麦志喜,王成云,等.超声萃取-气相色谱-串联质谱法测定纺织品中硫酸二甲酯和硫酸二乙酯的残留量[J].福建分析测试,2017,26(1):7.
LIN Junfeng,MAI Zhixi,WANG Chengyun,et al. Simultaneous determination of residual dimethyl sulfate and diethyl sulfate in textiles by gas chromatography-tandem mass spectrometry coupled with ultrasonic extraction[J] Fujian Analysis & Testing,2017,26(1):7.
15 吴楚森,王斌,王莉,等.气相色谱-质谱联用测定化妆品中硫酸二甲酯与硫酸二乙酯[J].分析测试学报,2018,37(1):70.
WU Chusen,WANG Bin,WANG Li, et al. Determination of dimethyl sulfate and diethyl sulfate in cosmetics by GC-MS[J]. Journal of Instrumental Analysis,2018,37(1):70.
16 施燕,何志高. LC-MS/MS法测定药物中硫酸二甲酯的残留量[J].中国临床药学杂志,2016,25(3):164.
SHI Yan,HE Zhigao. Determination of residue of dimethyl sulfate in drug by LC-MS/MS[J]. Chinese Journal of Clinical Pharmacy,2016,25(3):164.
17 鲍美玲,陈海霞,秦琴,等. GC-MS法同时测定9-氨基米诺环素盐酸盐中的硫酸二甲酯和硫酸二异丙酯[J].海峡药学,2018,30(9):51.
BAO Meiling,CHEN Haixia,QIN Qin,et al. Simultaneous determination of dimethyl sulfate and diisopropyl sulfate in 9-amino minocycline hydrochloride by GC-MS[J]. Strait Pharmaceutical Journal,2018,30(9):51.
18 杨诗易,邓双炳,孙飞,等.喜炎平注射液中硫酸二乙酯和硫酸二甲酯限量分析方法[J].沈阳药科大学学报,2023,40(6):738.
YANG Shiyi,DENG Shuangbing,SUN Fei, et al. Method for limit analysis of diethyl sulfate and dimethyl sulfate in Xiyanping injection[J]. Journal of Shenyang Pharmaceutical University,2023,40(6):738.
19 朱长友,罗文. GC-MS法测定塞来昔布中硫酸酯类基因毒性杂质[J].海峡药学,2022,34(10):26.
ZHU Changyou,LUO Wen.Determination of sulfates of genotoxic impurities in celecoxib by GC-MS[J].Strait Pharmaceutical Journal, 2022,34(10):26.
20 阮浩神.帕瑞昔布钠在术后镇痛中应用的研究进展[J].大医生,2023,8(13):141.
RUAN Haoshen. Research progress on the application of Parexib sodium in postoperative analgesia[J]. Doctor,2023,8(13):141.
引用本文: 崔萍,曹庆丰,丁逸梅 . 气相色谱-质谱法测定帕瑞昔布钠中3种硫酸酯类基因毒性杂质[J]. 化学分析计量,2024,33(8):56. (CUI Ping, CAO Qingfeng, DING Yimei. Determination of three sulfates genotoxic impurities in Parecoxib sodium by GC-MS[J]. Chemical Analysis and Meterage, 2024, 33(8): 56.)

来源:化学分析计量
关键词: 基因毒性杂质